| Скачать .docx |
Реферат: Стадия обжига колчедана в производстве серной кислоты
Содержание
1 Серная кислота: применение, свойства. 3
2.Выбор и обоснование источников сырья. 6
4. Расчет материального баланса. 13
5. Выбор и обоснование конструкции основного аппарата. 16
6. Экологическая оценка производства. 22
Серная кислота – важнейший продукт основой химической промышленности. Среди минеральных кислот она по объему производства и потребления занимает первое место, поэтому изучение свойств и методов получения серной кислоты весьма актуально.
Серную кислоту применяют в различных отраслях народного хозяйства, поскольку она обладает комплексом особых свойств, облегчающих ее технологическое использование. Серная кислота не дымит, в концентрированном виде не корродирует черные металлы, способна образовывать многочисленные устойчивые соли и является дешевым сырьем для различных производств.
Крупнейшим потребителем серной кислоты в настоящее время является промышленность фосфорных и азотных минеральных удобрений, таких как сульфат аммония, аммофос, суперфосфат и др. Простой суперфосфат получают обработкой апатитов и фосфоритов серной кислотой. Применение минеральных удобрений способствует повышению урожайности сельскохозяйственных культур и содержания в них полезных веществ.
Кроме того, серная кислота применяется для производства некоторых кислот (фосфорной, соляной, уксусной), сульфатов, искусственных волокон, лаков, красок, пластмасс, моющих средств, взрывчатых веществ, лекарственных препаратов, ядохимикатов, а также при производстве цветных и редких металлов, спиртов, эфиров. Она расходуется на очистку нефтепродуктов, в качестве электролита в кислотных аккумуляторах, в машиностроении – на подготовку поверхности металлов при нанесении гальванических покрытий. В металлообрабатывающей промышленности серная кислота и ее соли применяют для травления стальных изделий [5].
Целью данной работы является изучение стадии обжига серного колчедана при производстве серной кислоты.
1 Серная кислота: применение, свойства
1.1 Применение серной кислоты и олеума
Области применения серной кислоты и олеума весьма разнообразны. Значительная часть ее используется в производстве минеральных удобрений (30 – 60%), производстве красителей (2 – 16%), химических волокон (5 – 15%), в металлургии (2 – 3%). Она применяется для различных технологических целей в текстильной, пищевой и других отраслях промышленности и народного хозяйства (рисунок 1.1).
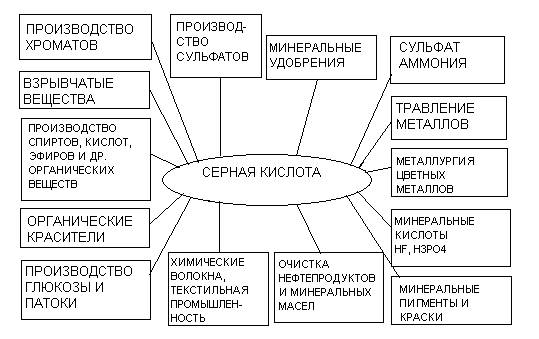
Рисунок 1.1 – Применение серной кислоты
1.2 Физические свойства серной кислоты
Безводная серная кислота – бесцветная тяжелая, маслянистая жидкость без запаха. Очень сильная двухосновная кислота, способная вызывать ожоги кожи. Плотность при 20°С 1,84 г/см3 . Температура кристаллизации 10,37°С. Температура кипения моногидрата 296,2°С. При нагревании выше температуры кипения начинает разлагаться:
H2 SO4 → SO3 + H2 O
Смешивается с водой и SO3 во всех соотношениях, образуя гидраты H2 SO4 ·nH2 O, где n = 1, 2, 3, 4, 5 и 6. Вследствие образования гидратов при разбавлении водой происходит сильное разогревание серной кислоты.
Температура кипения серной кислоты зависит от ее концентрации. С повышением концентрации водной серной кислоты температура кипения ее возрастает и достигает максимума 336,5°С при концентрации 98,3%, что соответствует азеотропному составу, после чего снижается (таблица 1.1) [1].
Таблица 1.1

1.3 Химические свойства концентрированной серной кислоты
Концентрированная серная кислота является сильным окислителем. Окисляет HI и частично НВг до свободных галогенов, углерод – до СО2 , S – до SO2 , окисляет многие металлы. Проведение окислительно-восстановтельных реакций с участием H2 SO4 обычно требует нагревания. Часто продуктом восстановления является SO2 :
S + 2 H2 SO4 = 3SO2 ↑+ 2H2 O
C + 2 H2 SO4 = 2SO2 ↑+ CO2 ↑+ 2H2 O
H2 S + H2 SO4 = SO2 ↑+ 2H2 O + S↓
Сильные восстановители превращают H2 SO4 в Sили H2 S.
Концентрированная серная кислота при нагревании реагирует почти со всеми металлами (исключая Au, Pt, Be, Bi, Fe, Mg, Co, Ru, Rh, Os, Ir), например:
Cu + 2 H2 SO4 = CuSO4 + SO2 ↑+ 2H2 O
Серная кислота образует соли – сульфаты (Na2 SO4 ) и гидросульфаты (NaHSO4 ). Нерастворимы соли – PbSO4 , CaSO4, BaSO4 и др.:
H2 SO4 + BaCl2 = BaSO4 ↓ + 2HCl
Холодная серная кислота пассивирует железо, поэтому ее перевозят в железной таре. Безводная серная кислота хорошо растворяет SO3 и реагирует с ним, образуя пиросерную кислоту, получающуюся по реакции:
Н2 SO4 + SO3 =H2 S2 O7
Растворы SO3 в серной кислоте называются олеумом. Они образуют два соединения: H2 SO4 ·SO3 и H2 SO4 ·2SO3 [5].
1.4 Химические свойства разбавленной серной кислоты
Окислительные свойства для разбавленной серной кислоты нехарактерны. Разбавленная серная кислота обладает химическими свойствами, характерными для всех кислот: взаимодействует с основаниями, с основными и амфотерными оксидами, с солями:
H2 SO4 + 2NaOH = Na2 SO4 + 2H2 O
H2 SO4 + CaO = Ca SO4 + H2 O
H2 SO4 + СaCO3 = Ca SO4 + CO2 ↑+ H2 O
При взаимодействии разбавленной серной кислоты с металлами, стоящими в ряду стандартных электродных потенциалов левее водорода, образуются соли серной кислоты (сульфаты) и выделяется водород:
Zn + H2 SO4 = ZnSO4 + H2 ↑
Свинец не растворяется в разбавленной серной кислоте вследствие образования на его поверхности нерастворимого сульфата свинца [6].
2.Выбор и обоснование источников сырья
Для получения серной кислоты используют серу или содержащие серу соединения, из которых может быть получен сернистый ангидрид.
Один из распространенных видов сырья для получения серной кислоты — пирит, или серный колчедан FeS2 .
Встречается соединение серы с двумя металлами, например с медью и железом (халькопирит). Серу содержат сульфаты: гипс (сульфат кальция), мирабилит (сульфат натрия), глауберит (сульфат натрия и кальция) и др. Сера есть в угле, нефти, горючих и топочных газах.
Много серы в виде сернистого ангидрида имеется в составе отходящих газов металлургических печей. Сера содержится и в сероводороде, получающемся при коксовании угля или содержащемся в генераторном газе, газах нефтепереработки, попутных нефтяных газах и природном газе. Иногда для производства серной кислоты используют отходы некоторых производств, применяющих серную кислоту. Это кислые гудроны, травильные растворы, фосфогипс и др.
В разных странах соотношение различных видов сырья, применяемого для производства серной кислоты, неодинаково. Большинство стран в качестве основного сырья использует серный колчедан, в США серную кислоту получают преимущественно из серы. Следует, од-, нако, отметить, что доля колчедана в общем балансе се-русодержащего сырья уменьшается из-за все более широкого использования серы.
Серный колчедан
Основные залежи колчедана имеются в России (главным образом на Урале), в Испании, Японии, Канаде, Индии, Португалии, Италии, Норвегии.
Серный колчедан FeS2 содержит 53,4% S и 46,6% Fe.
Существуют следующие сорта колчедана: рядовой, флотационный и пиритный концентрат. Рядовой колчедан добывают в рудниках в виде кусков размером 50— 400 мм. Флотационный колчедан получается как отход при флотационном обогащении руд, содержащихся в качестве примесей к рядовому колчедану. Пиритный концентрат получают при вторичной флотации колчедана с отделением пустой породы.
Флотационный метод обогащения основан на различной смачиваемости зерен отдельных минералов водой. Частицы несмачиваемого (гидрофобного) минерала, не преодолевая сил поверхностного натяжения воды, остаются на ее поверхности. Частицы смачиваемого (гидрофильного) материала обволакиваются пленкой жидкости и увлекаются на дно аппарата. Минерал, плавающий на поверхности, снимают, отделяя от руды.
Флотацию проводят во флотационных машинах различного типа. Процесс флотации заключается в смешивании раздробленного колчедана с водой и флотореагентами — пенообразующими веществами (деготь, хвойные масла и др.)» и продувании воздуха. Гидрофобные частицы отделяемой примеси колчедана (например, медь) прилипают к воздушным пузырькам и всплывают с ними (это концентрат), а колчедан осаждается на дно (флотационный колчедан, или флотохвосты). Вторичная флотация флотохвостов с применением другого флотореагента дает пиритный концентрат. Пиритный концентрат часто называют тоже флотационным колчеданом.
Перед отправкой потребителю флотационный колчедан высушивают до содержания в нем влаги 3,8%.
Серный колчедан может содержать примеси соединений меди, цинка, свинца, мышьяка, никеля, кобальта, селена, висмута, теллура, кадмия, карбонаты и сульфаты кальция и магния, а также золото и серебро. Содержание селена составляет до 220 г/т, золота до 4 г/т, серебра до 40 г/т, мышьяка до 0,4%, фтора до 0,02%.
Флотационный колчедан содержит те же примеси, но в меньших концентрациях. Средние данные о химическом составе флотационного колчедана, поступающего на сернокислотные заводы, следующие:
| Компоненты | Содержание, % | Компоненты | Содержание, г/т |
| Сера | 40-45 | Золото | 1-5 |
| Железо | 35-39 | Серебро | 20-25 |
| Медь | 0,3-0,5 | Кадмий | 5,5-8,1 |
| Свинец | 0,01-0,2 | Кобальт | 50-200 |
| Цинк | 0,5-0,6 | Селен | 30-60 |
| Мышьяк | 0,07-0,09 | Теллур | 25-40 |
| SiО2 | 14-18 | ||
| Н2 О | 3,8 |
В качестве сырья для серной кислоты может «быть применен также углистый колчедан. Он получается путем отделения от углей (сортировкой и грохочением) и содержит до 18% углерода (именно с этим связано его название).
Первой стадией процесса является окисление сырья с получением обжигового газа, содержащего диоксид серы.
4FeS2 +11O2 = 2Fe2 O3 + 8SO2 (I)
При протекании реакции (I) помимо газообразного продукта реакции SO2 образуется твердый продукт Fe2 O3 , который может присутствовать в газовой фазе в виде пыли. Колчедан содержит различные примеси, в частности соединения мышьяка и фтора, которые в процессе обжига переходят в газовую фазу. Присутствие этих соединений на стадии контактного окисления диоксида серы может вызвать отравление катализатора. Поэтому реакционный газ после стадии обжига колчедана должен быть предварительно направлен на стадию подготовки к контактному окислению (вторая стадия), которая помимо очистки от каталитических ядов включает выделение паров воды (осушку), а также получение побочных продуктов (Se и Te).
На второй стадии протекает обратимая экзотермическая химическая реакция контактного окисления диоксида серы:
SO2 + 1/2O2 ↔ SO3 (III)
Последняя стадия процесса – абсорбция триоксида серы концентрированной серной кислотой или олеумом.
Важнейшей задачей в производстве серной кислоты является повышение степени превращения SO2 в SO3 . Помимо увеличения производительности по серной кислоте выполнение этой задачи позволяет решить и экологические проблемы – снизить выбросы в окружающую среду вредного компонента SO2 .
Обжиг FeS2 производят в печикипящего слоя на воздушном дутье. При этом протекает необратимая реакция:
4FeS2 + 11О2 = 2Fe2 O3 + 8SO2 + 13476 кДж.
Продукты окислительного обжига колчедана – обжиговый газ и огарок, состоящий из оксида железа Fe2 O5 , пустой породы и невыгоревшего остатка сульфида железа. Огарок после соответствующей подготовки может быть использован для производства чугуна. Состав обжигового газа зависит от природы сырья, состава и избытка воздуха при обжиге. В него входят сернистый ангидрид, кислород и азот [4].
Печные газы, получаемые при обжиге колчедана, содержат много пыли, для улавливания которой применяют циклоны и электрофильтры. В циклонах пыль оседает под действием центробежной силы пылинок в завихряющемся потоке газа. Электрофильтры представляют собой конденсаторы высоко напряжения. Запыленный газ проходит между пластинками электрофильтра, где пылинки заряжаются и оседают на противоположно заряженных пластинах. При встряхивании пластин осевшая пыль падает в бункер электрофильтра, из которого выгружается.
Далее газ проходит через две промывные башни, две ступени мокрых электрофильтров. После осушки в сушильной башне его газодувкой подают через систему теплообменников в контактный аппарат (см. рисунок 3.1). Конверсия идет аналогично производству серной кислоты из серы.
Производство серной кислоты могут осуществлять и в одну стадию катализа, при этом степень превращения SO2 в SO3 не превышает 98,5%. Перед отправкой на склад кислота разбавляется до ~ 93% H2 SO4 в соответствии с требованиями ГОСТа. Производительность современных установок достигает 1500–3100 тонн серной кислоты в сутки [8].
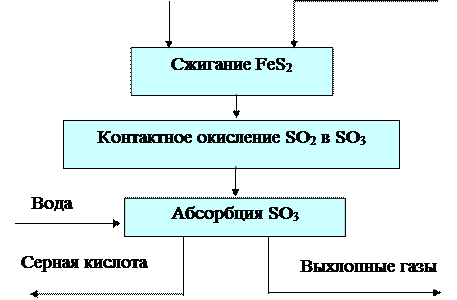
Блок-схема производства
|
|||
 |
|||
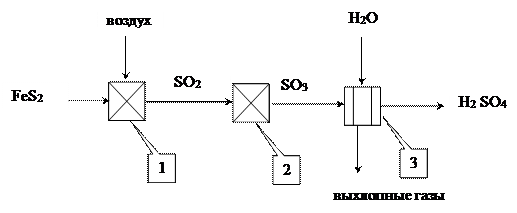 |
Операторная схема процесса
1 - печь, 2- контактный аппарат, 3- абсорбер
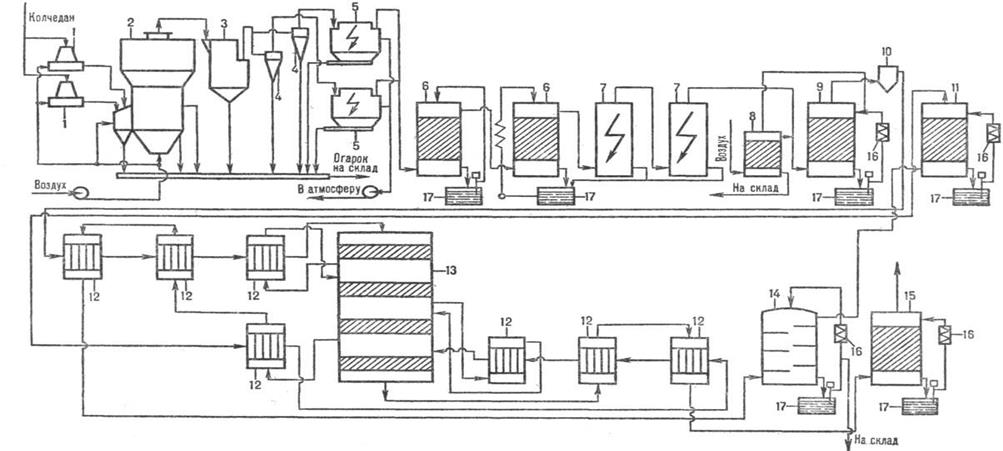
Рисунок 3.1.– Схема производства серной кислоты из колчедана
1 – тарельчатый питатель; 2 – печь; 3 – котел-утилизатор; 4 – циклоны; 5 – электрофильтры; 6 – промывные башни; 7 – мокрые электрофильтры; 8 – отдувочная башня; 9 – сушильнаябашня; 10 – брызгоуловитель; 11, 15 – моногидратные абсорберы; 12 – теплообменники; 13 – контактный аппарат; 14 – олеумный абсорбер; 16 – холодильники.
4. Расчет материального баланса
Расчет материального баланса является основным этапом. На основе материального баланса определяется целый ряд важнейших техноэкономических показателей: расход сырья и вспомогательных материалов для обеспечения заданной производительности; тепловой баланс и, соответственно, расход энергии, и теплообменную аппаратуру; экономический баланс производства, себестоимость продукции и, следовательно, рентабельность производства.
Исходные данные:
1. В печь поступает колчедан 40 т/сут.
2. Состав колчедана, % масс:
FeS2 – 70%;
песок (глина) –25%;
влага – 5%.
3. Содержание FeS2 в огарке – 2 %.
4. Коэффициент избытка воздуха α = 1,5. Состав воздуха кислород-21%об. , азот-79%об. .
Решение:
4FeS2 + 11O2 →8SO2 +2Fe2 O3
1. Рассчитаем, сколько пирита содержится в колчедане:
40 · 0,7 = 28 т/сут
2. Рассчитаем, сколько песка содержится в колчедане:
40 · 0,25 = 10 т/сут
3. Рассчитаем, сколько влаги содержится в колчедане:
40 · 0,05 = 2 т/сут
4. Молярная масса компонентов реакционной смеси : Mr(FeS2 ) = 120 кг/кмоль, Mr(O2 ) = 32 кг/кмоль, Mr(Fe2 O3 ) = 160 кг/кмоль, Mr(SO2 ) = 64 кг/кмоль.
5. Рассчитаем, сколько диоксида серы по массе получится при обжиге 40 т колчедана, содержащего 28 т пирита:
(28 т/сут · 8 · 64 кг/кмоль) /(4 · 120 кг/кмоль) = 29,87 т/сут
6. Рассчитаем массу образовавшегося огарка:
(28 т/сут · 160 кг/кмоль · 2)/(4 · 120 кг/кмоль) = 18,67 т/сут.
7. Рассчитаем содержание FeS2 в огарке:
18,67 т/сут · 0,02 = 0,37 т/сут
8. Рассчитаем содержание Fe2 O3 :
18,67 т/сут – 0,37 т/сут = 18,3 т/сут
9. Рассчитаем массу кислорода, израсходованного на получение 29,87 т/сут SO2 :
(29,87 т/сут · 11 · 32 кг/кмоль) /(8 · 64 кг/кмоль) = 20,54 т/сут
10. Рассчитаем массу кислорода с учетом коэффициента избытка воздуха
α =1,5:
20,54 т/сут · 1,5 = 30,81 т/сут
11. Рассчитаем объем кислорода:
(20,54 т/сут · 22,4 м3 /кмоль) / 0,032 т/кмоль =14378 м3 /сут
12. Рассчитаем объем кислорода с учетом коэффициента избытка воздуха
α =1,5:
14378 м3 /сут · 1,5 = 21567 м3 /сут
13. Рассчитаем объем воздуха, поступившего на окисление:
21567 м3 /сут / 0,21 = 102700 м3 /сут.
14. Рассчитаем массу воздуха, поступившего на окисление:
(102700 м3 /сут · 0,02884 т/кмоль) / 22,4 м3 /кмоль = 132,23 т/сут.
15. Рассчитаем массу отработанного воздуха:
(132,23 т/сут – 30,81 т/сут) + (30,81 т/сут – 20,54 т/сут) = 111,7 т/сут.
16. Рассчитаем массу вышедшего кислорода:
30,81 т/сут. – 20,54 т/сут. = 10,27 т/сут.
Таблица 3.1 – Материальный баланс процесса окисления пирита (FeS2 ) кислородом воздуха
| Приход | |||||
| Исходное вещество | кг/ч | т/сут. | т/мес. | т/год | %масс |
| Колчедан, в т.ч.: | 1666,7 | 40,0 | 1200,0 | 14400 | 23,22 |
| - пирит | 1166,7 | 28,0 | 840,0 | 10080,0 | |
| - влага | 83,3 | 2,0 | 60,0 | 720,0 | |
| - песок (глина) | 416,7 | 10,0 | 300,0 | 3600,0 | |
| Воздух, в т.ч.: | 5509,6 | 132,23 | 3966,9 | 47602,8 | 76,78 |
| - О2 | 1283,8 | 30,81 | 924,3 | 11091,6 | |
| - N2 | 4225,8 | 101,42 | 3042,6 | 36511,2 | |
| Всего | 7176,3 | 172,23 | 5166,9 | 62002,8 | 100 |
| Расход | |||||
| продукт | кг/ч | т/сут | т/мес. | т/год | %масс |
| SO2 | 1244,6 | 29,87 | 896,1 | 10753,2 | 17,34 |
| Пиритный огарок, в т.ч.: | 1277,9 | 30,67 | 920,1 | 11041,2 | 17,81 |
| - Fe2 O3 | 762,5 | 18,3 | 549 | 6588 | |
| - пирит | 15,4 | 0,37 | 11,1 | 133,2 | |
| - песок (глина) | 416,7 | 10,0 | 300,0 | 3600,0 | |
| - влага | 83,3 | 2,0 | 60,0 | 720,0 | |
| Отработанный воздух, в т.ч.: | 4653,75 | 111,69 | 3350,7 | 40208,4 | 64,85 |
| - О2 | 427,9 | 10,27 | 308,1 | 3697,2 | |
| - N2 | 4226,3 | 101,42 | 3042,9 | 36514,8 | |
| Всего | 7176,3 | 172,23 | 5166,9 | 62002,8 | 100 |
Рассчитано, что для получения 1т сернистого ангидрида нужно затратить 1,3391 т. сырья; при использовании 1т сырья выход диоксида серы составляет 0,7467 т.
5. Выбор и обоснование конструкции основного аппарата
Для обжига колчедана существуют печи различных конструкций: -механические полочные (многоподовые), вращающиеся цилиндрические, печи пылевидного обжига, печи для обжига в кипящем слое.
В механических полочных печах обжиг колчедана ведут на нескольких полках (сводах, подах), расположенных этажами друг над другом. Перемешивание и перемещение колчедана с пода на под производится механически.
Вращающиеся цилиндрические печи представляют собой вращающийся барабан, установленный наклонно. Колчедан подают с верхнего конца, огарок выгружают через нижний конец печи.
Печи пылевидного обжига получили свое название в связи с тем, что колчедан в них сжигается в виде тонко измельченной взвеси (пыли), подаваемой через форсунки в шахту печи, представляющую собой вертикальный полый цилиндр.
Печи для обжига колчедана в кипящем, или, как принято говорить, во взвешенном слое (псевдоожнжен-иом состоянии), характеризуются тем, что колчедан в печи находится во взвешенном состоянии, напоминающем кипение. Это достигается продуванием через слой с большой скоростью воздуха.
Производительность печей выражают в количестве условного колчедана, содержащего 45% серы, сжигаемого в печи в 1 сутки. Для определения производительности печей введено понятие интенсивность.
Интенсивность работы печи характеризуется количеством колчедана, сжигаемого в сутки на 1 м2 поверхности рабочих подов печи, в 1 м3 объема печи или на 1 м2 сечения шахты печи, т. е. для каждого типа печи принято свое выражение (размерность) интенсивности (напряженности) работы печи.
В качестве реакторов для обжига колчедана могут применяться печи различной конструкции: механические, пылевидного обжига, кипящего слоя (КС).
Кипящий слой называют также взвешенным, псевдоожиженным слоем. Внешне такой слои находится как бы в состоянии кипения. Это достигается тем, что через слой измельченного сырья (например, колчедана), находящегося на решетке с отверстиями, подают воздух с такой скоростью, что колчедан не проваливается через решетку и не лежит на ней, а находится в состоянии беспорядочного движения. Это наглядно показано на рис. 5.1. При кипении объем слоя увеличивается: первоначальная высота его (в покое) Н0 меньше, чем высота Н, соответствующая состоянию кипения.

Рис. 5.1. Схема идеального кипящего слоя:
а - неподвижный слой, б - кипящий слой; 1 - аппарат постоянного поперечного сечения, 2 - распределительная решетка, 3 - твердые частицы
Интенсивность обжига серусодержашего сырья определяется:
1) скоростью окисления серы в сырье,
2) скоростью передвижения кислорода из газового потока к поверхности сжигаемого сырья (диффузией),
3) диффузией образовавшегося SO2 в газовую смесь,
4) скоростью теплоотдачи от поверхности сырья газовому потоку (процесс теплоотдачи). Таким образом, интенсивность обжига зависит от процессов массопередачи и теплоотдачи. Скорости этих процессов возрастают при интенсивном перемешивании сырья и при увеличении поверхности соприкосновения фаз (воздуха с сырьем). Именно поэтому интенсивность обжига в «печах пылевидного обжига сырья выше, чем в механических печах. Еще больше она в печах кипящего слоя, так как частицы сырья перемешиваются еще более интенсивно благодаря турбулентности потока.
В настоящее время новые сернокислотные системы оборудуются преимущественно печами КС. Механические печи на действующих заводах постепенно заменяются печами этого типа.
Существенными достоинствами метода обжига колчедана в печах КС являются:
а) возможность получения концентрированного сернистого газа (12 15% SO2 ) с низким содержанием серного ангидрида и мышьяка в обжиговом газе,
б) высокая интенсивность печей. Так, интенсивность печей КС [в кг/(м2 сут)] в 80 раз выше интенсивности механических печей и в 4 раза — печей пылевидного обжига.
Содержание мышьяка в сернистом газе после печей КС зависит от температуры обжига и от концентрации SО2 . Возможность получать при определенном режиме обжига газ с незначительным содержанием мышьяка позволила применить такие печи в системе с упрощенной очисткой газа.
Печи с взвешенным (кипящим) слоем представляют собой цилиндрическую футерованную камеру с решеткой, на которую непрерывно поступает колчедан. Под решетку подается воздух со скоростью, обеспечивающей переход частиц во взвешенное состояние, но не достаточной для их уноса из печи. Частицы колчедана находятся в непрерывном движении, напоминающем кипение жидкости. Время пребывания частиц колчедана в печи составляет несколько секунд. Постоянный приток воздуха обеспечивает почти полное выгорание серы из колчедана. Взвешенный слой имеет высоту, определяемую расположением патрубка для вывода огарка. Частицы огарка свободно вылетают через патрубок благодаря высокой подвижности взвешенного слоя (рисунок 5.2).
Печи КС отличаются высокой интенсивностью (до 10000 кг/м2 ∙сут), обеспечивают более полное выгорание дисульфида железа и контроль температуры, облегчают процесс утилизации теплоты реакции обжига. К недостаткам печей КС следует отнести повышенное содержание пыли в газе обжига, что затрудняет его очистку. В настоящее время печи КС полностью вытеснили печи других типов в производстве серной кислоты из колчедана.
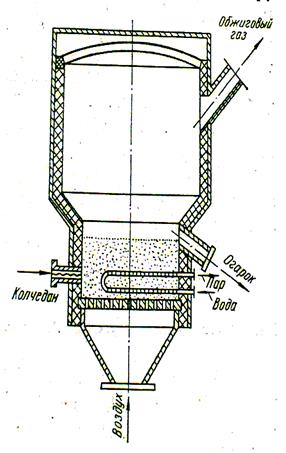
Рисунок 5.2 – Печь для обжига колчедана в кипящем слое [7]
Существуют печи КС с одинарным и двойным кипящим слоем. На рис. 5.3 представлена печь КС для обжига колчедана с одним кипящим слоем. Кожух шахты печи стальной, внутри футерованный огнеупорным кирпичом. В нижней части печи находится решетка (подовая плита) 6 с большим числом отверстий. Колчедан поступает в загрузочную камеру 9, огарок выводится через бункер 7. Первичный воздух подается под решетку 6, вторичный — из коллектора 1, расположенного на 'Некоторой высоте от верхнего уровня кипящего слоя колчедана. Для использования тепла горения в кипящий слой колчедана помещены охлаждающие элементы 5 — трубы -из углеродистой стали, по которым циркулирует вода. Нагретая вода поступает в паровой котел-утилизатор. В загрузочной камере также находятся охлаждающие элементы 8, соединенные с системой котла-утилизатора. Топочные газы выходят из печи в трубу 10. Для разжигания печи есть форсунка 2, работающая на газе или мазуте.
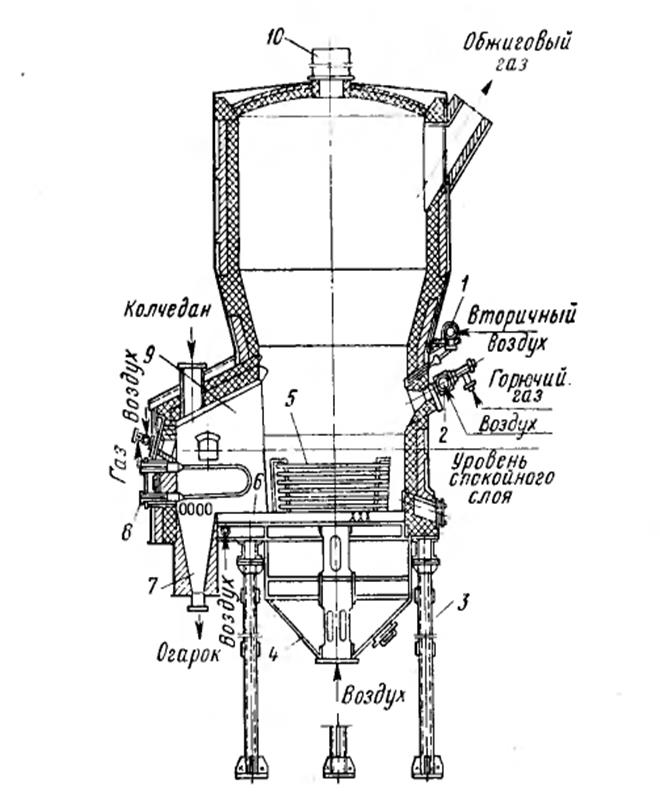
Рис. 5.3. Печь КС для обжига колчедана:
1-коллектор для вторичного воздуха. 2-форсунка, 3-опорная рама,4-конус,5,8- охлаждающие элементы. 6 - решетка (подовая плита). 7 -бункер под провальной решеткой загрузочной камеры. 9 - загрузочная камера. 10 - выхлопная труба
6. Экологическая оценка производства
В производстве серной кислоты вредными веществами являются: серная кислота, оксиды серы, олеум. Серная кислота и олеум представляют собой агрессивные жидкости, которые действуют разрушающим образом на растительные, животные ткани и вещества, отнимая у них воду, вследствие чего они обугливаются.
Аэрозоль серной кислоты. ПДК аэрозоля серной кислоты в воздухе:
ПДКр.з. = 1,0 мг/м3 (рабочей зоны),
ПДКм.р. = 0,3 мг/м3 (максимально разовая),
ПДКс.с. = 0,1 мг/м3 (среднесуточная).
Поражающая концентрацияпаров серной кислоты 0,008 мг/л (экспозиция 60 мин), смертельная 0,18 мг/л (60 мин). Класс опасности 2. Аэрозоль серной кислоты может образовываться в атмосфере в результате выбросов химических и металлургических производств, содержащих оксиды серы, и выпадать в виде кислотных дождей [10].
Оксид серы (IV) и взвешенные частицы. Основной процесс, приводящий к образованию взвешенных частиц и диоксида серы, – это процесс горения, осуществляемый в печи сжигания серы. Диоксид серы – бесцветный газ. Источники те же, что и для взвешенных частиц. Вступает в каталитические или фотохимические реакции с другими загрязняющими веществами с образованием SO3 , серной кислоты и сульфатов [6].
Класс опасности (токсичности) диоксида серы 3. ПДКр.з. = 10,0 мг/м3 , ПДКм.р. = 0,5 мг/м3 , ПДКс.с. = 0,03 мг/м3 .
Частицы, образующиеся в результате сгорания – сажа, копоть, пыль, – обычно имеют размер менее 1 мкм, так что они могут легко приникать в легочные альвеолы. Они также могут содержать опасные вещества, такие как асбест, тяжелые металлы, мышьяк. Оксиды металлов являются основным классом неорганических частиц в атмосфере. Они образуются в любых процессах, связанных со сжиганием топлива, содержащего металлы.
Класс опасности сажи 3. ПДКр.з. = 4,0 мг/м3 , ПДКм.р. = 0,15 мг/м3 , ПДКс.с. = 0,05 мг/м3 .
Класс опасности нетоксичной пыли 4. ПДКр.з. = 6,0 мг/м3 , ПДКм.р. = 0,5 мг/м3 , ПДКс.с. = 0,15 мг/м3 .
В промышленных районах концентрация диоксида серы обычно достигает 0,05-0,1 мг/м3 ; в сельских районах она в несколько раз меньше, а над океаном меньше в 10-100 раз. В сельской местности фоновая концентрация близка к 0,5 мкг/м3 , а концентрация в городах в 50-100 раз выше. Из-за химических превращений время жизни диоксида серы в атмосфере невелико (порядка нескольких часов). В связи с этим возможность загрязнения и опасность воздействия непосредственно диоксида серы носят, как правило, локальный, а в отдельных случаях региональный характер.
Термин «взвешенные частицы» относится к ряду тонкодисперсных твердых веществ или жидкостей, диспергированных в воздухе в результате процессов горения, производственной деятельности и естественных источников. До 20 % общего количества взвешенных частиц может состоять из серной кислоты и сульфатов (частицы до 1 мкм в диаметре состоят из них на 80 %) [7].
Влияние на окружающую среду . Высокие концентрации диоксида серы вызывают серьезное повреждение растительности. Острое повреждение, вызванное диоксидом серы, отражается в появлении белесых пятен на широколистных растениях или обесцвеченных некротических полос на листьях с продольным жилкованием. Хронический эффект проявляется как обесцвечивание хлорофилла, приводящее к пожелтению листьев, появлению красной или бурой окраски, которая в нормальных условиях маскируется зеленой. Независимо от формы проявления, результатом является снижение продуктивности и замедление роста. Лишайники особенно чувствительны к SO2 и используются как биоиндикаторы при определении его избыточных количеств в воздухе. Однако диоксид серы не всегда вызывает повреждение: в сульфатдефицитных местностях дополнительные небольшие уровни SO2 могут благотворно влиять на растения, однако происходящее параллельно некоторое подкисление почвы может потребовать дополнительного известкования [7].
Предложения по уменьшению количества выбросов вредных веществ в окружающую среду
В процессе производства серной кислоты некоторая часть серы уходит в атмосферу в виде диоксида серы SO2 . Неполное окисление SO1. Амелин А.Г. Производство серной кислоты. – М.: Химия, 1964. – 247с.
2. Васильев Б. Т., Отвагина М. И., Технология серной кислоты. – М.:Химия, 1985. – 352с.
3. Малин К.М., Аркин И.А., Боресков Г.К., Слинько М.Г. Технология серной кислоты. – М.: Госхимиздат, 1984. –380с.
4. Соколов Р.С. Химическая технология. Учеб. пособие для вузов. Т.1. – М.: Гуманитарный издательский центр ВЛАДОС, 2000. – 368с.
5. Производство серной кислоты: Учебник для проф.-техн. учеб. заведений.—2-е изд., перераб. и доп. — М.: Высш. школа, 1980. — 245 с, ил.
6. Протасов В.Ф. Экология, здоровье и охрана окружающей среды в России/ Учебн. и справочное пособие. – М.: Финансы и статистика. – 2001. – 672с.
7. Степеновских А.С. Охрана окружающей среды/ Учебник для вузов. – М.:Юнити-Дана, 2000. – 559с.
8. Малкин И.З./ ЭКиП//Утилизация сернокислых промышленных отходов. – 2003. – №6. – с. 10-14.