| Скачать .docx |
Реферат: Одно и многоатомные спирты
Одно- и многоатомные спирты .
Алифатические спирты - это соединения, содержащие гидроксильную группу (-ОН), связанную с sp3 -гибридизованным атомом углерода. Спирты можно разделить на три большие группы: простые спирты, стерины и углеводы. Рассмотрим простые спирты, с общей формулой Cn H2 n +1 OH.
методы получения спиртов
1. Гидролиз галогеналканов в водных растворах щелочей
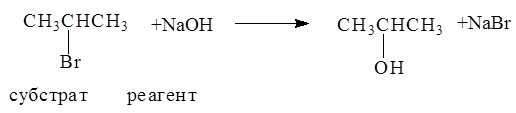
Реакция замещения галогена на ОН-группу протекает по механизму нуклеофильного замещения SN . В зависимости от строения субстрата замещение протекает по SN 1 (мономолекулярное замещение):
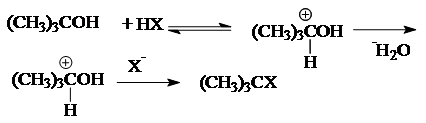
или SN 2 (бимолекулярное):
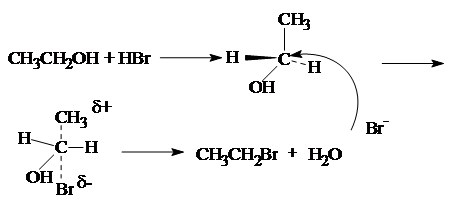
Атакующий агент – анионы (SH - , OН - , I - , Br - , С l - , F - , RO - , CH3 COO - , ONO2 - ) или молекула (ROH, HOH, NH3 , RNH2 ). По увеличению реакционной способности анионы располагаются в следующий ряд:
HS - , RS - > I - > Br - > RO - > Cl - > CH3 COO - > ONO2 -
Анионы более сильные нуклеофилы, чем сопряженные кислоты:
OH - > HOH, RS - > RSH, RO - > ROH, Cl - >HCl
Нуклеофил – атом (или частица), который может отдать пару электронов любому элементу, кроме водорода. Механизм бимолекулярного нуклеофильного замещения (SN 2 ) включает образование промежуточного комплекса.
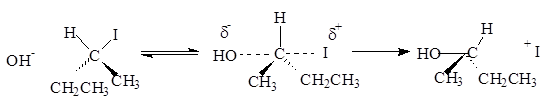
Представленная реакция является реакцией замещения, так как нуклеофил (ОН - ) вытесняет уходящую группу (I- ).
Механизм мономолекулярного нуклеофильного замещения (SN 1 ) состоит из двух стадий:
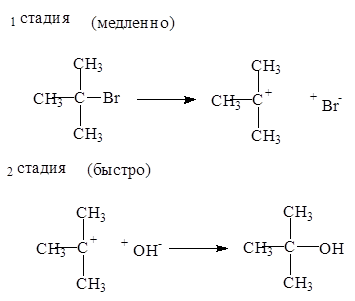
Реакции замещения по механизму SN 1 в тех случаях, когда образуется стабильный катион. Первичные галогеналканы реагируют по механизму SN 2 , а третичные - по механизму SN 1.
2. Гидратация алкенов.
Присоединение воды к алкену протекает в присутствии кислотных катализаторов (H2 SO4 , H3 PO4 , оксид алюминия и другие носители, обработанные кислотами).
Реакция протекает по карбоний-ионному механизму:
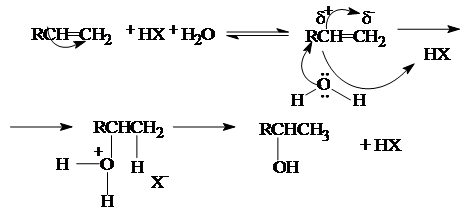
3. Восстановление карбонильных соединений (кетонов и альдегидов)
Альдегиды и кетоны легко восстанавливаются водородом в присутствии катализаторов (например, Ni, Pd, Pt) в соответствующие первичные и вторичные спирты:
CH3 -CH2 -COH + H2 ® CH3 -CH2 -CH2 -OH
пропионовый альдегид пропанол-1
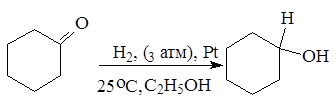
циклогексанон циклогексанол
Для восстановления карбонильной группы используются комплексные гидриды металлов - борогидрид натрия NaBH4 (растворитель - вода, этанол) или алюмогидрид лития LiAlH4 (растворитель - абсолютный эфир):
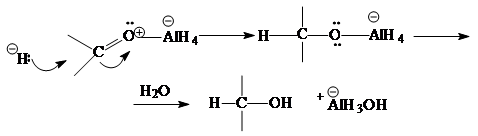
CH3 COCH3 + LiAlH4 ® (CH3 )2 -CHOH
CH3 -CHO + NaBH4 ® CH3 -CH2 -OH
Сложные эфиры также восстанавливаются алюмогидридом лития, причем оба фрагмента эфира превращаются в спирты:
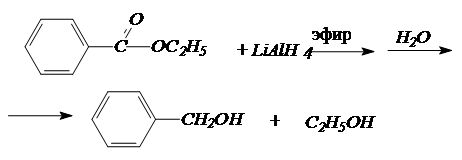
4. Синтезы спиртов с использованием реактивов Гриньяра.
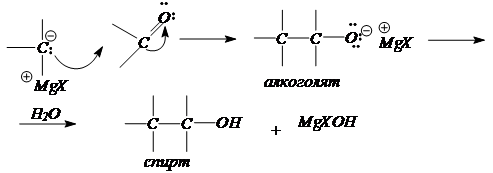
RMgHal + H2 C=O (формальдегид) ® RCH2 O - Mg+ Hal + H2 O ® R-CH2 -OH
RMgHal + R’HC=O (альдегид) ® R( R’)CHO - Mg+ Hal + H2 O ® R(R’)CH-OH
RMgHal + (R’)2 C=O (кетон) ® R( R’)2 CO - Mg+ Hal + H2 O ® R(R’)2 C-OH
По механизму это реакция нуклеофильного присоединения к карбонильной группе.
Промышленные методы получения спиртов.
1. Окисление алканов (синтез спиртов С10 -С20 ).
3 RCH2 -OH + B(OH)3 « B(OHC2 R)3 + 3 H2 O
2. Гидратация алкенов .
R-CH=CH2 + H2 O « R-CH (OH)-CH3
CH2 =CH2 + H2 O ® CH3 CH2 OH
из пропилена и н-бутилена - изопропиловый и н-бутиловый спирты:
CH3 -CH=CH2 + H2 O ® CH3 -CH (OH)-CH3
CH3 -CH2 -CH=CH2 + H2 O ® CH3 -CH2 -CH (OH)-CH3
а из изобутилена - трет-бутиловый спирт:
(CH3 )2 C=CH2 + H2 O ® (CH3 )3 C-OH
Электрофильный механизм гидратации определяет уже отмеченное выше направление присоединения (правило марковникова), а также изменение реакционной способности алкенов в ряду, определяемом сравнительной стабильностью образующихся карбокатионов:
(CH3 )2 CH=CH2 >> CH3 -CH2 -CH=CH2 > CH3 -CH=CH2 >> CH2 =CH2
3. Синтез спиртов по методу Фишера-Тропша .
СО + 2Н2 « СН3 ОН
4. Процесс оксосинтеза .
CH2 =CH2 + CO + H2 ® CH3 -CH2 -CHO
Химические свойства спиртов
Обусловлены способностью гидроксильной группы образовывать межмолекулярные водородные связи.
1. Кислотные и основные свойства спиртов.
CH3 -OH + HNO3 ¨ CH3 -ONO2 + H2 O
CH3 CH2 OH + H2 SO4 ® CH3 CH2 OSO3 H + H2 O
CH3 CH2 OH + (CH3 CO)2 O ® CH3 COOC2 H5 + CH3 COOH
Это – реакции замещения водорода на кислотный остаток.
2. Замещение гидроксильной группы на галоген.
CH3 CH2 OH + HBr « CH3 CH2 Br + H2 O
Реакция протекает по механизму нуклеофильного замещения.
CH3 CH2 -OH + SOCl2 ® CH3 CH2 -Cl + SO2 + HCl
3CH3 CH2 -OH + PCl3 ® 3CH3 CH2 -Cl + H3 PO4
Ниже приводится механизм взаимодействия спирта с тионилхлоридом:
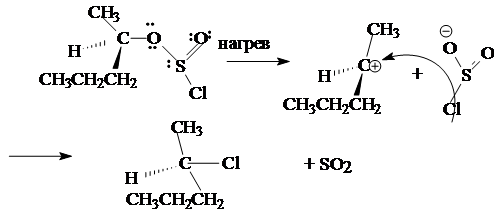
Этот механизм обозначается символом Sni (замещение нуклеофильное внутримолекулярное).
Реакции отщепления
CH3 CH2 OH ® CH2 =CH2
В качестве катализаторов используют минеральные кислоты (серная, фосфорная), кислые соли (KHSO4 ), ангидриды кислот (Р2 О5 ), оксид алюминия и т.д.
R-OH + R’-OH ® ROR (ROR’, R’OR’) + H2 O
Порядок отщепления воды в большинстве случаев определяется
правилом зайцева : при отщеплении воды наиболее легко отщепляет водород от соседнего наименее гидрированного атома углерода.
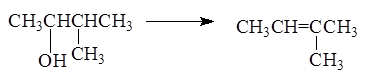
Реакция отщепления воды от спиртов протекает через стадию образования карбкатиона:
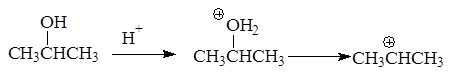
В зависимости от строения спирта образуются первичные, вторичные и третичные карбкатионы:
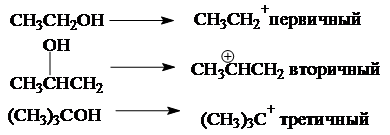
По увеличению стабильности катионы располагаются в следующий ряд: CH3 CH2 + < CH3 CH+ CH3 < (CH3 )3 C+
Любое влияние, делокализующее положительный заряд карбкатиона, ведет к его стабилизации. Мы имеем дело в данном ряду с индукционной стабилизацией:
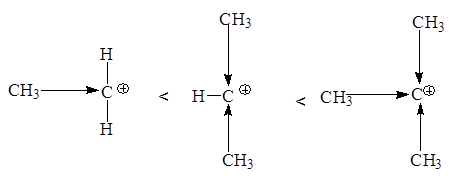
Образующиеся катионы в зависимости от их строения способны к перегруппировкам:
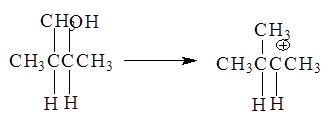
3-Метил-2-бутанол - в 2-метил-2-бутильный катион, склонный к перегруппировке в более стабильный:
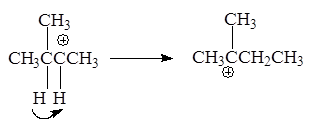
Образование последнего 2-метил-2-бутильного катиона связано с гидридным перемещением (Н- ) из положения 3 в положение 2.
В перегруппировке может участвовать и алкильная группа:
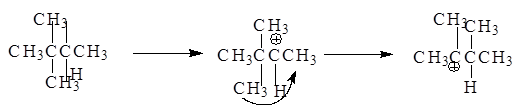
Основное различие между тремя типами реакционных интермедиатов (карбкатионы, карбанионы и свободные радикалы) состоит в том, что карбкатионы имеют тенденцию изомеризоваться в более устойчивые частицы.
Окисление . Первичные и вторичные спирты могут быть окислены соответственно до альдегидов и кетонов. Третичные спирты устойчивы к окислению в мягких условиях.
Первичные спирты окисляются до альдегидов под действием окислителей, содержащих Cr(VI). Это обычно хромовая кислота H2 CrO4 :
R-CH2 -OH + H2 CrO4 ® R-CHO + H2 CrO3 (неустойчива) + H2 0
Окисление первичного спирта начинается с образования эфира хромовой кислоты RCH2 -O-Cr(O)2 -OH. На следующей стадии эфир претерпевает реакцию отщепления, в результате которой образуется двойная связь С=О.
Альдегиды можно также получить окислением первичных спиртов реагентом Саретта (комплекс CrO3 с пиридином).
В относительно мягких условиях происходит окисление спирта разбавленным раствором оксида хрома (VI) в разбавленной серной кислоте (окисление по Джонсу).
Вторичные спирты легко окисляются до кетонов под действием K2 Cr2 O7 +H2 SO4 +H2 0 , CrO3 +CH3 COOH+H2 O и KMnO4 в кислой среде:
(R )2 CH-OH + [O] ® R-CO-R + H2 O
Механизм окисления вторичных спиртов подобен окислению первичных спиртов в альдегиды, поэтому для получения кетонов пригодны методы, описанные выше.
Дегидрирование спиртов . Этим способом получают многие альдегиды и кетоны:
2R-CH2 -OH ® R-COH + H2
2(R)2 -CH-OH ® (R)2 -CO + H2
В качестве катализатора используются металлическая медь и серебро. В промышленности этот процесс реализован для получения формальдегида из метанола.
Многоатомные спирты
Обычно названия двухатомных спиртов производятся от названия двухатомного радикала с прибавлением слова гликоль, например этиленгликоль, пропиленгликоль. По Женевской номенклатуре пользуются окончанием -ол, но указывают число гидроксильных групп - диол, -триол, -тетрол и т.д.
В двухатомных спиртах гидроксилы могут быть соединены с первичными, вторичными и третичными атомами углерода, поэтому различают гликоли двупервичные, первично-вторичные и т.д.
Синтез гликолей осуществляется в основном теми же способами, что одноатомных спиртов, кроме того, окислением соответствующих алкенов перманганатом калия в щелочной среде (реакция Вагнера)
R-CH=CH2 + [O]® R-CH(OH)CH2 -OH
Для окисления используют разбавленные водные растворы перманганата калия.
Практически наиболее важным промышленным методом получения гликолей является гидратация соответствующих a-оксидов:
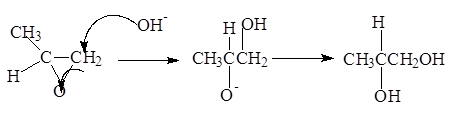
Из этиленоксида получают три важных класса соединений: целлозольвы, карбитолы и карбоваксы .
Целлозольвы (соединения типа ROCH2 CH2 OH) образуются в результате реакции алкоголята и этиленоксида. Название “целлозольв” относится к 2-этоксиэтанолу. Бутилцеллозольв - хороший растворитель; он используется в гидравлических тормозных жидкостях и добавляется к авиационному топливу в качестве антифриза:
CH3 CH2 CH2 CH2 ONa + (CH2 )2 O + H2 O® CH3 CH2 CH2 CH2 -O-CH2 CH2 OH
Карбитолы , являющиеся моноалкиловыми эфирами диэтиленгликоля, применяются в качестве растворителей, а также при изготовлении лаков. Их получают реакцией целлозольва с эквивалентным количеством этиленоксида.
Этиленгликоль и пропиленгликоль широко используют в производстве антифризов:
C3 H5 (OCOR)3 + 3 NaOH ® HOCH2 -CHOH-CH2 OH + 3 RCOONa
Синтетический глицерин получают исходя из пропилена:
CH3 -CH=CH2 + Cl2 ® Cl-CH2 -CH=CH2 ® OH- CH2 -CH=CH2 ®
® OH- CH2 -CH(Cl)-CH2 OH ® OH- CH2 -CH(OH)-CH2 OH;
CH3 -CH=CH2 ® CH2 =CH-COH + H2 O2 ® OH-CH2 -CH(OH)-COH ®
® OH- CH2 -CH(OH)-CH2 OH.