| Скачать .docx |
Курсовая работа: Участие аналогов убихинона в переносе электронов в дыхательной цепи митохондрий
Московский Государственный Университет
им. М. В. Ломоносова
Факультет Биоинженерии и Биоинформатики.
Курсовая работа студента IV курса Салимоновой Татьяны на тему:
Участие аналогов убихинона в переносе электронов в дыхательной цепи митохондрий.
Научный руководитель: кбн Высоких Михаил Юрьевич
Содержание
Митохондрии.............................................................................................................................................. 3
Локализация митохондрий в цитозоле разных типах клеток......................................................... 3
Взаимодействие митохондрий с цитоскелетом................................................................................ 4
Морфология митохондрий.................................................................................................................. 6
Митохондриальный матрикс................................................................................................... 6
Митохондриальный геном ....................................................................................... 7
Эволюционное происхождение митохондрий......................................................... 8
Внутренняя митохондриальная мембрана............................................................................. 9
Межмембранное пространство............................................................................................ 13
Внешняя митохондриальная мембрана................................................................................. 13
Внешняя и внутренняя мембраны - транспорт белков в митохондрию........................... 13
Метаболические функции митохондрий.............................................................................. 14
Дыхательная цепь................................................................................................................................... 16
Открытие дыхательной цепи............................................................................................................ 16
Организация дыхательной цепи....................................................................................................... 17
Комплекс I или НАДН-убихинон-редуктаза.......................................................................... 18
Комплекс II (или сукцинатдегидрогеназа)............................................................................ 20
Кофермент Q........................................................................................................................... 21
Метаболизм кофермента Q ..................................................................................... 21
Функции кофермента Q: ..................................................................................... 22
Физико-химические свойства кофермента Q......................................................... 23
Комплекс III (комплекс bc1 или убихинол цитохром с оксидоредуктаза)......................... 26
Цитохром с.............................................................................................................................. 28
Комплекс IV (цитохромоксидаза).......................................................................................... 28
Н+-АТФ-синтаза..................................................................................................................... 30
Антиоксиданты и механизм образования активных форм кислорода в клетке......................... 32
Механизм образования активных форм кислорода............................................................. 32
Антиоксиданты...................................................................................................................... 38
Аналоги убихинона........................................................................................................................... 44
Список литературы:............................................................................................................................... 51
Митохондрии - это органеллы размером с бактерию (около 1*2 мкм). Они представляют собой окруженные двойной мембраной органеллы, специализирующиеся на синтезе АТФ (рис. 5). В среднем на клетку приходится примерно 2000 митохондрий, общий объем которых составляет до 25% от объема клетки. Количество митохондрий в клетке зависит от ее функции и размеров - например, в гепатоците содержится примерно 800 митохондрий, в ооците человека - около 100000 митохондрий, а в сперматозоиде - всего несколько.
Митохондрии не имеют строго фиксированной формы, размера и локализации в клетке, которые могут различаться у разных типов клеток. Так, например, у гепатоцитов и фибробластов митохондрии вытянутые, а размер их составляет 3-4 m в длину и 1 m в ширину.
Локализация митохондрий в цитозоле разных типах клеток
В больших и ассиметричных клетках митохондрии обычно сосредоточены в местах повышенного потребления АТФ. В сперматозоиде митохондрии собраны в спираль вокруг аксонемы (это осевая нить жгутика сперматозоида - сложноорганизованный цитоскелетный комплекс), что обеспечивает его движение .
В скелетных мышцах митохондрии образуют митохондриальный ретикулум – единую митохондриальную сеть. На уровне z-дисков миофибрилл располагаются гигантские разветвленные митохондрии (рис.2), которые окружают каждую миофибриллу и снабжают ее АТФ, необходимым для мышечного сокращения. Таким образом, получаются “пласты” или “этажи” митохондрий, повторяющиеся дважды на каждый саркомер. Между “этажами ” вдоль миофибрилл располагаются нитчатые митохондрии, соединяющие эти пласты. Тем самым создается трехмерная картина митохондриального ретикулума, проходящего через весь объем мышечного волокна.
Интересно, что в клетках сердечной мышцы обнаружены митохондрии двух типов: одни локализованы непосредственно под сарколеммой, а другие между миофибриллами (субсарколеммарные митохондриии окисляют субстраты в 1,5 раза эффективнее межмиофибриллярных). Эти митохондрии так же образуют сеть.
 |
 |
Рисунок 2 .Распределение митохондрий в скелетных мышцах между саркомерами: м - митохондрия, ф - фибрилла, с - саркомер
Высоко регулярное распределение митохондрий также присуще поперечно-полосатым летательным мышцам насекомых. В палочковидной зрительной клетке (анализатор сетчатки) митохондрии сконцентрированы в протопласте ближе к выступающей в стекловидное тело глаза части клетки (рис.3).
В круглых дрожжевых клетках или в гаметах Chlamydomonas митохондрии распределены по периферии клеток, возможно для максимально эффективного доступа кислорода.
Таким образом, митохондрии локализуются в клетке в местах повышенного потребления АТФ, но способны перемещаться при изменении АТФ/АДФ градиента.
Взаимодействие митохондрий с цитоскелетом
Взаимодействие с цитоскелетом было описано только с применением индивидуальных флуоресцентных меток для митохондрий и микротрубочек [2,3]. После этого подобные взаимодействия были описаны для различных типов клеток млекопитающих [4].
Цитоплазма эукариотических клеток пронизана трехмерной сеткой из белковых нитей (филаментов), называемой цитоскелетом. В зависимости от диаметра филаменты разделяются на три группы: микрофиламенты (6-8 нм), промежуточные волокна (около 10 нм) и микротрубочки (около 25 нм). Все эти волокна представляют собой полимеры, состоящие из субъединиц особых глобулярных белков.
Микрофиламенты (актиновые нити) состоят из плотно упакованной спирали из ориентированных глобулярных (G) актиновых мономеров [56]. В мышцах млекопитающих обнаружен α-актин , а β- и γ-актины составляют микрофиламенты немышечных клеток.
Структурными элементами промежуточных волокон являются белки, принадлежащие к пяти родственным семействам и проявляющие высокую степень клеточной специфичности [62]. Все эти белки имеют в центральной части базовую стержневую структуру, которая носит название суперспирализованной α-спирали.
Микротрубочки построены из глобулярного белка тубулина, представляющего собой димер α и β-субъединиц (53 и 55 кДа) [65]. Протофиламенты – это линейные цепочки, образованные α и β- гетеродимерами. Эти протофиламенты образуют кольца (по 13 штук в каждом), которые полимеризуются в длинную трубку.Микротрубочка (МТ) представляет собой высоко динамичную полярную структуру, имеющую минус-конец, локализованный на центросоме, вблизи ядра, и медленно растущий или быстро разбирающийся плюс-конец.
Цитоскелет служит клетке механическим каркасом и “рельсами” для транспорта органелл и других крупных комплексов внутри клетки. Митохондрии перемещаются вдоль цитоскелетных фибрилл с помощью молекулярных моторов. Структурные белки, входящие в состав молекулярных моторов, относятся к трем семействам: кинезины, цитоплазматические динеины и миозины.
Одним из наиболее изученных клеточных моторов является кинезин. Молекула кинезина представляет собой димер, образованный двумя одинаковыми полипептидными цепями. с одной стороны каждой полипептидной цепи кинезина формируется глобулярная головка, соединенная со сравнительно длинным хвостом. Хвосты двух мономерных цепей сплетены вместе, а наклоненные в разные стороны головки образуют своеобразную рогатину, которая непосредственно взаимодействует с глобулярными мономерами микротрубочки, вдоль которой перемещается кинезин (рис. 4).
Каждая из двух головок кинезина обладает АТРазной активностью. Связывание и гидролиз молекулы АТФ в активном центре кинезина, а также последующие события, вызванные диссоциацией AДФ и Фн, сопровождаются изменением положения головок относительно тубулиновых мономеров, в результате чего кинезин перемещается вдоль микротрубочки. Работа головок кинезина хорошо скоординирована: связывание и гидролиз молекулы АТФ одной головкой димерного комплекса способствует освобождению молекулы АДФ из активного центра другой головки. Головки кинезина попеременно связываются с мономерными звеньями микротрубочки. За одну секунду кинезина делает приблизительно 100 шагов, перемещаясь за это время на расстояние 800 нм [5].
В митохондриях можно выделить четыре субкомпартмента: митохондриальный матрикс, внутреннюю мембрану, межмембранное пространство и внешнюю мембрану, обращенную к цитозолю (рис. 5).
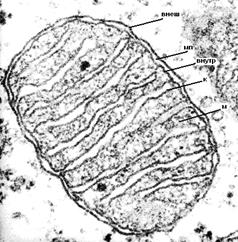
Рисунок 5: Митохондрии из цетроацинозной клетки поджелудочной железы: внеш – внешняя мембрана, мп – межмембранное пространство, внутр – внутренняя мембрана, к – криста митохондрии, м –матрикс митохондрии.
Матрикс - это внутреннее пространство митохондрий, ограниченное внутренней митохондриальной мембраной (рис.5). Оно является местом локализации важнейших ферментов и ферментативных путей, предопределяющих роль митохондрий в общем клеточном обмене. Прежде всего, следует упомянуть о цикле ди- и трикарбоновых кислот (цикл Кребса), занимающем центральное место в обмене благодаря интеграции процессов деградации и биосинтеза клеточных компонентов и сопряжения их с запасанием значительных количеств энергии.
Еще в митохондрии локализовано бета-окисление жирных кислот, но это характерно только для животного царства [6], а в дрожжах, грибах и растениях бета- окисление сосредоточено в микротелах, главным образом в пероксисомах. В матриксе присутствуют пируватдегидрогеназный комплекс, ферменты окисления аминокислот и множество других ферментов, АТФ, АДФ, Pi, Mg2+, Ca2+, K+ и множество метаболических интермидиатов.
В матриксе митохондрий находятся рибосомы, по многим характеристикам отличающиеся от эукариотических рибосом. На них синтезируется не более 5% от всех митохондриальных белков, а большинство белков кодируется клеточной ДНК и поступает в митохондрии из цитозоля. Как правило, кодируемые мтДНК белки, сильно гидрофобны и локализованы на внутренней мембране митохондрий со стороны матрикса. В целом же рост и функционирование митохондрии невозможны без импорта белков, кодируемых ядерным геномом и синтезированных на цитоплазматических рибосомах (так называемых белков-предшественников). Каждый поступивший белок должен достичь определенного субкомпартмента, в котором он функционирует. Таким образом, рост митохондрий возможен за счет импорта цитоплазматических белков, включающего последовательный избирательный перенос белков через одну или две мембраны.
Митохондриальный геном
Подавляющее большинство описанных митохондриальных геномов представляет собой кольцевые суперспирализованные двуцепочечные молекулы ДНК. У некоторых растений наряду с кольцевыми формами имеются и линейные, а у некоторых простейших, например инфузорий, в митохондриях обнаружены только линейные ДНК [46]. Как правило, в каждой митохондрии содержится несколько копий ее генома. Так, в клетках печени человека около 2 тыс. митохондрий, и в каждой из них — по 10 одинаковых геномов. В фибробластах мыши 500 митохондрий, содержащих по два генома, а в клетках дрожжей S.cerevisiae — до 22 митохондрий, имеющих по четыре генома.
Размер генома митохондрий разных организмов колеблется от менее 6 тыс. пар нуклеотидов у малярийного плазмодия (в нем, помимо двух генов рРНК, содержится только три гена, кодирующих белки) до сотен тысяч пар нуклеотидов у наземных растений (например, у Arabidopsis thaliana из семейства крестоцветных 366924 пар нуклеотидов). При этом 7—8-кратные различия в размерах мтДНК высших растений обнаруживаются даже в пределах одного семейства. Длина мтДНК позвоночных животных отличается незначительно (табл.1).
Таблица 1: Размеры мтДНК млекопитающих.
| организм |
человек |
свинья |
дельфин |
шпорцевой лягушки Xenopus laevis |
карп |
| Размер генома (пар нуклеотидов) |
16569 |
16350 |
16330 |
17533 |
16400 |
Эти геномы сходны также и по локализации генов, большинство которых располагаются встык; в ряде случаев они даже перекрываются, обычно на один нуклеотид, так что последний нуклеотид одного гена оказывается первым в следующем. В отличие от позвоночных, у растений, грибов и простейших мтДНК содержат до 80% некодирующих последовательностей. У разных видов порядок генов в геномах митохондрий отличается [47].
Количество генов, кодируемых мтДНК разных организмов, колеблется от 37 (у млекопитающих) до 97 (у простейших) (табл.2). Все митохондриальные геномы кодируют две рРНК, двадцать две или более тРНК, тринадцать или более белков комплекса Таблица 2: дыхательной цепи и дополнительные митохондриальные гены (нет у млекопитающих).
Таблица 2: Количество генов кодируемых мтДНК у разных организмов
| организмы гены, кодируемые мтДНК |
Простейшие (Reclinomonas americana ) |
млекопитающие и большинство грибов |
растения |
| Белки электрон-транспортной цепи и аппарата окислительного фосфорилирования |
23 |
13 |
13 |
| рРНК |
3 (5S РНК, 12S рРНК, 16S рРНК) |
2 (12S рРНК, 16S рРНК) |
более 2х (12S рРНК, 16S рРНК и другие рРНК) |
| 5S РНК |
1 |
не найдены |
не найдены |
| тРНК |
27 |
22 |
22 |
| РНК компонент рибонуклеазы Р (РНК процессинг)- |
1 |
не найдены |
не найдены |
| мультисубъединичной РНК полимеразы - аналога эукариотичекой полимеразы |
4 |
Похоже, что гены эубактериальной мультисубъеди-ничной рнк-полимеразы потерялись из всех прочих митохондрий и заменились на одно-субъединичный фермент, который кодируется ядерным геномом. |
|
| миторибосомальные белки |
18 |
не найдены |
несколько |
| всего |
97 генов (геном в 69034 пар оснований) |
37 генов |
более 37 генов |
Кроме того, все мтДНК обладают интересным свойством - они не метилируются, в отличие от ядерных и прокариотических ДНК [48].
Эволюционное происхождение митохондрий
Существуют две основные теории, объясняющих происхождение органелл с собственным не ядерным геномом.
Теории первой группы предполагают, что геном органелл происходит от ядерного генома. Предполагается, что часть ядерного генома оказалась механически отделена мембранами от основной части ядерного генома и постепенно приобрела способность к независимому функционированию.
Теории второй группы предполагают симбиотические события и то, что геномный материал органелл имеет внеклеточного происхождения. Факультативные прокариотические симбионты, попавшие в клетку хозяина путем эндоцитоза, с течением времени потеряли часть своих генов и стали облигатными симбионтами. Постепенно за ними закрепилась и определенная функция внутриклеточного метаболизма.
Одним из доказательств эндосимбиотической теории стало открытие митохондриальной ДНК [17] и обнаружение таковой во всех эукариотических митохондриях. Но мтДНК слишком мала, чтобы содержать информацию о свободноживущем организме. Это говорит о том, что часть митохондриального генома была утеряна и, скорее всего, недостающие промитохондриальные гены частично были перенесены в ядро, а частично безвозвратно утеряны. Еще в пользу симбиотической теории говорят многочисленные факты:
- совпадают размеры и формы митохондрий и свободно живущих аэробных бактерий; те и другие содержат кольцевые молекулы ДНК, не связанные с гистонами (в отличие от линейных ядерных ДНК);
- по нуклеотидным последовательностям рибосомные и транспортные РНК митохондрий отличаются от ядерных, демонстрируя при этом удивительное сходство с аналогичными молекулами некоторых аэробных грамотрицательных эубактерий;
- митохондриальные РНК-полимеразы, хотя и кодируются в ядре клетки, ингибируются рифампицином, как и бактериальные, а эвкариотические РНК-полимеразы нечувствительны к этому антибиотику; ингибирование рибосом стрептомицином
- белковый синтез в митохондриях и бактериях подавляется одними и теми же антибиотиками, не влияющими на рибосомы эвкариот: ингибирование рибосом стрептомицином, зависимость транскрипции от рифамицина и ее устойчивость к циклогексимидину, участие в начале транскрипции формилметионин, прокариотическая структура промотера
- в митохондрии, как и в бактериях, полиаденилирование мРНК отсутствует или выражены слабо
- липидный состав внутренней мембраны митохондрий и бактериальной плазмалеммы сходен, но сильно отличается от такового наружной мембраны митохондрий, гомологичной другим мембранам эвкариотических клеток;
- кристы, образуемые внутренней митохондриальной мембраной, являются эволюционными аналогами мезосомных мембран многих прокариот;
Результаты сиквенса митохондриальных генов свидетельствуют о монофилетическом происхождении митохондрии из эубактериального предка, относящегося к подразделу a-протеобактерий. В течение последних лет были определены полные последовательности большого числа митохондриальных и эубактериальных геномов. Эти результаты свидетельствуют о том, что митохондриальный геном эволюционировал из единого предка, общего для всех существующих в настоящее время эукариот, и что митохондриальная и ядерная компоненты эукариотной клетки возникли одновременно [45].
Внутренняя митохондриальная мембрана
Внутренняя мембрана митохондрий отличается от прочих клеточных мембран своим белково-липидным составом. Так, в большинстве мембран клетки соотношение белков и липидов составляет 50:50, в рамках концепции “белков, плавающих в липидном море”, когда как во внутренней митохондриальной мембране это соотношение равно 75:25, предполагая сравнительно плотную упаковку белков. Тем не менее, внутренняя мембрана, вероятно, находится в текучем, а не в твердом состоянии[7,8].
Белки внутренней мембраны, кодируемые мтДНК, образуют субъединицы белковых комплексов, другие компоненты которых кодируются ядерными генами и поступают из цитозоля. Образование таких гибридных агрегатов требует сбалансированного синтеза этих двух типов субъединиц; каким образом координируется синтез белка на рибосомах разных типов, разделенных двумя мембранами, остается загадкой.
Внутренняя митохондриальная мембрана легко проницаема для О2, СО2, Н2О и некоторых других соединений и слабо проницаема (в силу специфики белково-липидного состава) для нуклеотидов, сахарозы, ионов водорода, калия, натрия, кальция, магния и т. д. Связь внутреннего компартмента митохондрий с цитоплазмой осуществляется через сеть специфических белков-переносчиков, обеспечивающих активный избирательный транспорт необходимых веществ: неорганических анионов и катионов, моно-, ди- и трикарбоновых кислот, аминокислот, жирных кислот, адениновых нуклеотидов.
Наиболее изучен транслокатор адениновых нуклеотидов (АДФ/АТФ - переносчик) (рис.9). АДФ/АТФ-переносчик катализирует высокоспецифичный электрогенный обмен цитоплазматического АДФ на внутримитохондриальный АТФ, образующийся в результате окислительного фосфорилирования. Это наиболее характерный компонент митохондрий, эукариотической клетки, его содержание составляет до 15-20% от общей белковой массы внутренней митохондриальной мембраны. Фосфатный переносчик, расположенный на внутренней мембране, поставляет, фосфат для синтеза АТФ [9].
Белки дыхательной цепи также расположены во внутренней мембране (рис.7 и ниже).
Внутренняя мембрана образует регулярные складчатые структуры – кристы, за счет которых площадь ее поверхности очень сильно возрастает. Криста состоит из ламеллярной и соединенной с внутренней мембранной более узкой трубковидной частей ([10]). Т.е. внутренняя мембрана, смежная с наружной мембраной, и внутренняя мембрана ламеллы соединены посредством структуры, названной кристоножкой (pedicula cristae). Топологически межмембранное пространство все еще продолжается внутри ламеллы. Можно выделить три типа организации крист:
- ламеллярные (плоские) кристы, подразделяющиеся также на подтипы: лентовидные, листовидные, многослойные цилиндрические и шаровидные (дисковидные и пластинчатые) структуры
- везикулярные кристы, включающие пузырьковидные, колбовидные и мешковидные
- трубчатые кристы (рис.6Б).
Эти типы крист встречаются во всех эукариотических царствах. Митохондриальные кристы растений и высших животных в основном относится к ламеллярному типу, хотя в некоторых тканях обнаружены митохондрии с везикулярными и трубчатыми кристами.
Среди остальных эукариот везикулярные кристы распространены так же широко, как ламеллярные и трубчатые. Так у Ciliophora- только трубчатые кристы, а у Cryptophyta -только ламеллярные. У некоторых организмов (Euglenophyta, Chlorophyta, Chrysophyta, Mycetozoa ) вообще отличный от вышеперечисленных тип крист. У других (Sporozoa, Myxospora и Ascetospora. ) же вообще встречаются смешанные типы.
Рисунок 6 A: Митохондрия с ангулярными кристами из сердечной мышцы. Б: Митохондрия с трубчатыми кристами из амебы. В: Митохондрия из коры надпочечника. Г: Митохондрия из астроцита. Д: Митохондрия из псевдобранхии рыбы. Е: Митохондрия из коры надпочечника (из клеток, секретирующих стероиды).
Количество и морфология крист отражают изменение активности митохондрий в зависимости от потребности клетки в энергии. Так, например, сильно складчатые ламеллярные кристы с обширной площадью поверхности характерны для интенсивно дышащих тканей, таких как мышечная и нервная.
Но может быть и так, что морфологические изменения митохондрий не обязательно связаны с дыхательной функцией митохондрий. В клетках, секретирующих стероиды, таких как клетки Лейдига (железистые клетки [гландулоцит] яичка), митохондрии могут очень сильно изменяться в размерах (что не характерно для митохондрий многоклеточных организмов), и порядок расположения в них крист так же своеобразен (рис.6 Е). [11].
Кристы могут также располагаться параллельно, гексагонально, образуя треугольники на поперечном сечении. Примером подобной структуры могут быть митохондрии сердечной мышцы (рис.6А), кристы которых на протяжении все длины образуют острые углы по направлению к соседней.
Наружная мембрана имеет постоянную площадь поверхности и поэтому может поддерживать фиксированные границы, в то время как внутренняя мембрана с огромной площадью поверхности вынуждена образовывать складки (выпячиваться), чтобы поместиться в имеющийся в распоряжении объем.
Межмембранное пространство разделяет внешняя и внутренняя мембраны, ширина его составляет около 10-20 нм. Здесь накапливаются различные киназы и протоны (рис.8), переносимые сюда из матрикса митохондрии при дыхании, создавая протонный градиент ΔμН, за счет электрохимической энергии которого образуется АТФ.
Внешняя митохондриальная мембрана
Во внешней мембране локализованы белки порины (рис. 7), обеспечивающие свободную проницаемость мембраны для неорганических ионов и метаболитов, а так же для белковых молекул, размер которых не превышает 10 кДа. Для больших по размеру белков внешняя мембрана является барьером и поэтому помогает удержать белки межмембранного пространства от утечки обратно в цитозоль.
Внешняя и внутренняя мембраны - транспорт белков в митохондрию
Белки, импортируемые в митохондриальный матрикс, обычно поступают из цитозоля в течение одной - двух минут после их отделения от полирибосом. Белки переносятся в матрикс митохондрии через зоны слипания, связывающие внешнюю и внутреннюю мембраны. Для этого переноса требуется гидролиз ATP, а также электрохимический градиент на внутренней мембране. Этот градиент образуется в процессе транспорта электронов по мере того, как протоны откачиваются из матрикса в межмембранное пространство.
Транспортируемый белок разворачивается, когда пересекает митохондриальные мембраны. Поскольку в развернутом состоянии и водорастворимые, и гидрофобные белки имеют сходную структуру, они могут быть перенесены с помощью общего механизма.
Белки, импортируемые в митохондриальный матрикс, почти всегда несут на N-конце сигнальный пептид длиной от 20 до 80 аминокислотных остатков. После поступления белка в митохондрию сигнальный пептид быстро удаляется при помощи специфической протеазы (сигнальной пептидазы) матрикса и затем, вероятно, деградирует в матриксе до аминокислот. Сигнальный пептид может быть исключительно простым. На втором этапе транспорта белок может переноситься во внутреннюю мембрану. Для этого он должен иметь еще гидрофобный сигнальный пептид; этот пептид открывается после удаления первого сигнала.
Импорт кодируемых ядерным геномом белков в митохондрии - сложный мультистадийный процесс [12,13,14]. Наряду с основным направлением импорта белков - в матрикс митохондрий - существуют пути импорта белков в другие митохондриальные субкомпартменты. Транслокация предшественников кодируемых ядерным геномом белков в митохондрии осуществляется как котрансляционная (импорт белков происходит одновременно с их синтезом, т. е. в процессе элонгации), так и посттрансляционная (включение их в мембрану митохондрий происходит только после окончания процесса их синтеза: белок-предшественник отделяется от полисомы и лишь после этого импортируется в митохондрию).
Метаболические функции митохондрий
В митохондриях за счет окислительной деградации питательных веществ синтезируется большая часть необходимых клетке АТФ. В митохондрии локализованы следующие метаболические процессы: превращение пирувата в ацетил-КоА, катализируемое пируватдегидрогеназным комплексом; цитратный цикл; дыхательная цепь, сопряженная с синтезом АТФ (сочетание этих процессов носит название окислительное фосфорилирование); расщепление жирных кислот путем β-окисления и частично цикл мочевины (рис.8). Митохондрии также поставляют клетке продукты промежуточного метаболизма и действуют на ряде с ЭР (эндоплазматическим ретикулюмом) как депо ионов Ca, которое с помощью ионных насосов поддерживает концентрацию Ca2+ в цитоплазме на постоянном низком уровне (ниже 1 мкмоль/л).
Главной функцией митохондрий является захват богатых энергией субстратов (жирные кислоты, пируват, углеродный скелет аминокислот) из цитоплазмы и их окислительное расщепление с образованием СО2 и Н2О, сопряженное с синтезом АТФ.
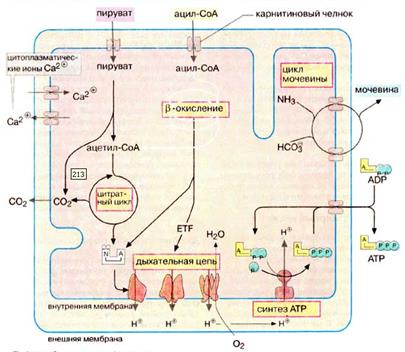
Рисунок 8: Метаболические функции митохондрии (схематическое изображение [55]).
Реакции цитратного цикла приводят к полному окислению углеродсодержащих соединений (СО2) и образованию восстановительных эквивалентов, главным образом в виде восстановленных коферментов. Большинство этих процессов протекает в матриксе. Ферменты дыхательной цепи, которые реокисляют восстановленные коферменты, локализованы во внутренней мембране митохондрий. В качестве доноров электронов для восстановления кислорода и образования воды используются НАДН и связанный с ферментом ФАДН2. Это высоко экзергоническая реакция является многоступенчатой и сопряжена с переносом протонов Н+ через внутреннюю мембрану из матрикса в межмембранное пространство. В результате на внутренней мембране создается электрохимический градиент. В митохондриях электрохимический градиент используется для синтеза АТФ из АДФ и неорганического фосфата при катализе АТФ-синтазы. Электрохимический градиент является также движущей силой ряда транспортных систем.
Началом изучения дыхания принято считать классические опыты А. Лавуазье, который еще в 1777 году показал, что “чистый воздух, войдя в легкие, выходит из них частично в виде связываемого воздуха или меловой кислоты. Следовательно, чистый воздух, проходя через легкие, претерпевает такое же разложение, которое имеет место при горении угля”. Теперь мы знаем, что меловая кислота это ни что иное, как углекислый газ (CO2).
К началу XX века уже было известно, что ткани млекопитающих катализируют окисление органических кислот кислородом воздуха. Тунберг и Виланд предположили существование в тканях дегидрогеназ (активаторов атомов водорода в молекулах субстратов). Варбург же считал, что катализ обусловлен железосодержащим ферментом (дыхательным ферментом), активирующим химически инертный кислород. Оба оказались правы. В тоже время Кейлин обнаружил в тканях пигменты (цитохромы), окраска которых зависела от наличия кислорода в клетке и от активности дыхательного фермента Варбурга. В 50х годах стало ясно, что некоторые дегидрогеназы, цитохромы Кейлина и дыхательный фермент Вырбурга (дыхательная цепь) прочно связаны с внутренними мембранами митохондрий. В 60х годах Грин разработал методы разделения, выделения и очистки компонентов дыхательной цепи.
Уже в 30х годах была установлена тесная связь между процессами окисления (поглощения кислорода) и образования АТФ (фосфорилирование), но вот природа это связи была непонятна вплоть до 60х годов.
В 1961 году Митчелл предложил идею хемиосматического энергетического сопряжения в дыхательной цепи. Можно выделить три основных положения принципа хемиосматического сопряжения [54]:
1. Внутренняя мембрана митохондрий, где происходят окислительно-восстановительные реакции дыхания, непроницаема для ионов водорода (Н+ ) (точнее, протон диффундирует через двойной фосфолипидный слой очень медленно по сравнению со скоростью потребления кислорода). В то же время мембраны хорошо проницаемы для воды и благодаря электролитической диссоциации Н2 О D Н+ + ОН- запас протонов в водных растворах неограничен.
2. Внутренняя мембрана митохондрий ассиметрична: одни компоненты дыхательной цепи контактируют с матриксом (например, активный центр комплекса I), другие расположены внутри мембраны (например, убихинон), третьи контактируют с межмембранным пространством (например, цитохром с ).
3. Разрушение мембраны не препятствует окислению НАДН кислородом, а даже ускоряет дыхание. Энергетическое сопряжение (синтез АТФ) при этом полностью прекращается: происходит разобщение процессов переноса электронов и запасания энергии. Для разобщения необязательно полностью разрушать мембрану – достаточно, сохраняя ее структуру, добавить вещества, резко повышающие проницаемость мембраны для протонов.
Спустя примерно двадцать лет хемиосмотическая концепция сопряжения транспорта электронов и образования АТФ в дыхательной цепи стала общепринятой теорией. И по сей день продолжаются работы по изучению и детальной расшифровки всех участников дыхательной цепи.
Дыхательная цепь является частью процесса окислительного фосфорилирования. Компоненты дыхательной цепи катализируют перенос электронов НАДН+Н+ или восстановленного убихинона (QH2) на молекулярный кислород. Из-за большой разности окислительно-восстановительных потенциалов донора (НАДН+Н+ и, соответственно, QH2) и акцептора (О2) реакция является высоко экзергонической. Большая часть выделяющейся при этом энергии используется для создания градиентов протонов и, наконец, для образования АТФ с помощью АТФ-синтазы.
Дыхательная цепь включает три белковых комплекса (комплексы I III IV), встроенных во внутреннюю митохондриальную мембрану, и две подвижные молекулы-переносчики – убихинон (кофермент Q) и цитохром с (рис. 9). Сукцинатдегидрогеназа, принадлежащая собственно к цитратному циклу, также может рассматриваться как комплекс II дыхательной цепи. АТФ-синтаза иногда называется комплексом V, хотя она не принимает участие в переносе электронов.
Комплексы дыхательной цепи построены из множества полипептидов и содержат ряд различных окислительно-восстановительных коферментов, связанных с белками. К ним принадлежат флавин (ФМН) или ФАД, в комплексах I и II, железосерные центры (в I, II и III) и группы гемма (II, III и IV).
Электроны поступают в дыхательную цепь различными путями. При окислении НАДН+Н+ комплекс I переносит электроны через ФМН и Fe/S- центры на убихинон. Образующиеся при окислении сукцината, ацил-КоА и других субстратов электроны переносятся на убихинон комплексом II или другой митохондриальный дегидрогеназой через связанный с ферментом ФАДН2 или флавопротеин. При этом окисленная форма кофермента Q восстанавливается до ароматического убигидрохинона. Последний переносит электроны на комплекс III, который поставляет их через два гемма b , один Fe/S- центр и гемм с1 на небольшой геммсодержащий белок цитохром с. Последний переносит электроны к комплексу IV, цитохром с-оксидазе. Цитохром с-оксидаза содержит для осуществления окислительно-восстановительных реакций два медьсодержащих центра. (Cua и Cub) и геммы а и а3, через которые электроны, наконец, поступают к кислороду. При восстановлении О2 образуется сильный основной анион О2-, который связывает два протона и переходит в воду. Поток электронов сопряжен с образованными комплексами I, III и IV протонным градиентом.
Рассмотрим теперь по подробнее все комплексы, составляющие дыхательную цепь.
Комплекс I или НАДН-убихинон-редуктаза.
Комплекс I (НАДН-убихинон-редуктаза) (рис. 10) катализирует транспорт восстановительных эквивалентов от НАДН к убихинону, чувствительный к действию ротенона и пиерицидина и сопряженный с запасанием энергии. Это самый большой и сложно устроенный комплекс дыхательной цепи. Он состоит из 14 (у бактерий)-45 разных полипептидов с общей молекулярной массой 600-900 кДа, ФМН-содержащего флавопротеида, 16-24 атомов негемового железа и эквивалентного количества лабильного сульфида [27].По форме НАДН-дегидрогеназа напоминает “старый башмак”, он не помещается в мембране и частично торчит “голенищем” наружу. Или НАДН-дегидрогеназа имеет L-образную форму и частично выдается из мембраны.
![]()
![]()
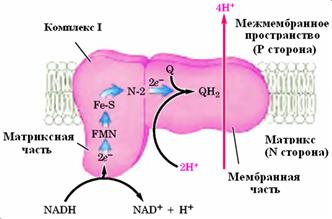
Рисунок 10: Комплекс I (NADH-убихинон-редуктаза).
7 пептидов комплекса I кодируются митохондриальным геномом [28], остальные - ядерным (импортируються из цитозоля в митохондрии). Большинство редокс-центров связано с двумя фрагментами комплекса: флавопротеином (Фп) (или НАДН-дегидрогеназой) и железобелком (IP). Первый содержит ФМН и некоторые из FeS-кластеров, в то время как в состав второго входят только железосерные центры.
Флавопротеин состоит из трех полипептидов в соотношении 1:1:1 (массы 51, 24 и 10 кДа). Он катализирует окисление НАДН некоторыми искусственными акцепторами электронов (но не природным акцептором KoQ). Тяжелая субъединица связывает НАДН, она содержит ФМН (рис.11) и четыре атома железа. Перенос водорода от НАДН к ФМН специфически тормозится реином .
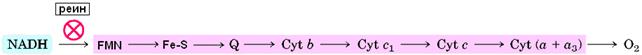
Средняя субъединица, скорее всего, содержит FeS-кластер с двумя атомами железа (рис. 12). FeS-кластеры FeSI 1a и FeSI 1b связаны с большой субъединицей Фп (их потенциалы -0,37 и -0,22 соответственно). В мембране Фп не доступен для гидрофобных модификаторов белка, а, значит, прикрыт другими белковыми субъединицами или фосфолипидами.
Фрагмент IP содержит 6 полипептидов (75, 49, 30, 18, 15 и 13 кДа) и 12 атомов железа. FeS-кластеры содержат по четыре атома железа, два из них ассоциированы с 75 и 49 кДа-полипептидами, которые пересекают мембрану и обращены в водную фазу. Третий кластер ассоциирован с эквимолярным комплексом субъединиц 30 и 13 кДа. Редокс-потенциалы всех кластеров похожи - около – 0,24 В. Один из кластеров (FeSI 3) локализован вблизи ФМН.
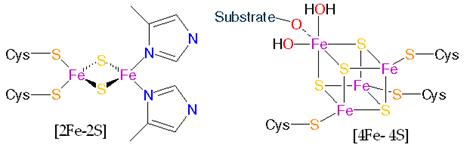
Рисунок 12: Fe-S кластеры.
На долю Фп и IP приходиться около 30% от общего количества белка комплекса I, а остальной белок содержит FeSI 2-кластер (-0,02 В), который играет роль восстановителя убихинона (рис.11). Между FeSI 2 и KoQ локализован участок торможения комплекса ротеноном, пирицидином, барбитуратами (например, амптал) и некоторыми аналогами KoQ.
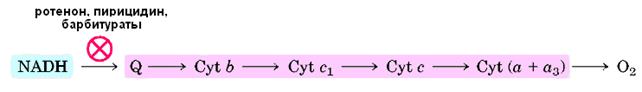
Таким образом, с НАДН электроны передаются на ФМН, после чего через цепь FeS-кластеров доходят до FeSI 2, где происходит восстановление убихинона до убихинола.
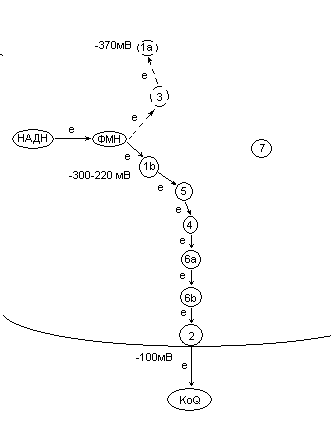
Рисунок 13: Схема передачи электронов от ФМН через FeS-кластеры на убихинон.
Также убихинон является акцептором электронов в реакции окисления сукцината до фумарата, которую катализирует комплекс II дыхательной цепи.
Комплекс II (или сукцинатдегидрогеназа).
Комплекс II меньше и проще устроен, чем комплекс III. Это фермент класса оксидоредуктаз; он состоит из 4 субъединиц (с молекулярными массами около 70, 30, 14 и 12 кДа) и содержит в качестве окислительно-восстановительных групп флавинадениндинуклеотид (рис. 11) (ФАД ковалентно связан с самой тяжелой субъединицей) и 3 Fe-S-кластера (рис. 14) (ассоциированы с 30 кДа субъединицей). Малые субъединицы (С и D) сукцинатдегидрогеназы высших организмов (и фумаратредуктазы микроорганизмов) содержит гем группы b и сайт связывания убихинона, который является конечным акцептором электронов. Субъединицы С и D интегрированы в мембрану, субъединицы А и В (большие субъединица) расположены в матриксе. Активный центр (содержит остатки аргинина, цистеина и гистидина), связывающий сукцинат, локализован на самой тяжелой субъединице А. Субъединица А также содержит ФАД. Fe-S центры локализованы в субъединице B. Сукцинатдегидрогеназа проявляет оптимальную каталитическую активность при рН 7,5-8 [29].
Таким образом, электроны с сукцината передаются на ФАД, с которого переносятся на Fe-S центры, а потом уже достигают CoQ (этот путь по длине равен 40А, тогда как 11 А - максимальное расстояние для быстрого транспорта электронов) (рис.14).
Исследование коэнзим Q (CoQ) началось с 1955 год, когда Фестенштейн выделил и охарактеризовал его [30]. Уже через два года Крейн показал, что убихинон является компонентом дыхательной цепи митохондрий [31], а спустя год после этого, Вольф выявил и его химическую структуру (рис.15) [32]. Первое время кофермент Q рассматривался только как переносчик электронов от комплексов I и II к комплексу III. Позже в ряде работ была доказана незаменимая роль CoQ как переносчика дыхательной цепи - извлечение и последующее добавление коэнзим Q в субмитохондриальные частицы приводило к инактивации, а затем реактивации комплексов I и II [33]. В 1975 году Митчелл [34] предложил механизм (названный «петля Митчелла»), по которому осуществляется транспорт электронов с митохондриальных дегидрогеназ на комплекс III дыхательной цепи.
Метаболизм кофермента Q
Гибсон изучил путь биосинтеза CoQ на мутантных штаммах E. Coli [36] путем введения мутаций по восьми ubi генам (А-Н), ответственным за ферменты биосинтеза CoQ. Вообще, убихинон (UQ) представляет собой молекулу, в состав которой входит 2,3-диметокси-5-метил-бензохиноновое кольцо, соединенное в шестом положении с гидрофобным изопреноидным хвостом (от 6 до 10 звеньев). В клетке изопреноидная цепь синтезируется в составе полипренилпирофосфата через мевалонатный путь. Предшественник же хиноидного кольца– р-гидроксибензоат– синтезируется из аминокислот тирозина или фенилаланина. Специальная трансфераза (ubi A) «сшивает» эти молекулы, и затем происходит декарбоксилирование, гидроксилирование и метилирование кольца в определенных положениях. В аэробных условиях в гидроксилировании задействован молекулярный кислород, а в анаэробных – вода. Метилирование идет за счет аденозилметионина. Похожие механизмы синтеза были обнаружены для дрожжей и клеток печени крыс, где основные различия процессов касаются порядка и типа модификаций бензохинонового кольца [37].
Функции кофермента Q:
Исследования последних лет показали, что помимо основной своей функции переносчика электронов в дыхательной цепи, кофермент Q выполняет еще ряд немаловажных функций.
Так, кофермент Q и его метаболиты являются важнейшими естественными гидрофобными антиоксидантами, предотвращающими перекисное окисление липидов, карбонилирование белков и накопление токсичных продуктов. Предотвращение опосредованного окислительным стрессом повреждения внутриклеточных структур, в первую очередь митохондрий, препятствует инициации гибели клеток по апоптотическому пути и тканевой дисфункции, приводящей к развитию ряда нейродегенеративных заболеваний, ишемии сердца и других патологических проявлений, а также при старении. CoQ участвует и в различных транспортных системах.
В эукариотических клетках существует специальная система транспорта электронов через плазматическую мембрану. НАДН-зависимая CoQ-редуктаза на внутренней стороне плазмалеммы восстанавливает убихинон, который, в свою очередь, переносит электроны на фермент НАДН-оксидазу (NOX локализованна на внешней стороне мембраны). NOX называется так, потому что раньше думали, что она функционирует как фермент, окисляющий экзогенный НАДН. А на самом деле основными терминальными акцепторами электронов, восстанавливаемыми NOX, являются внеклеточные радикалы аскорбата, молекулярный кислород (до воды или супероксида O2 . – ) и белковые дисульфидные связи.
Предположительно, CoQ-зависимая NOX участвует в процессах регуляции уровня NADH в цитозоле, а также может быть связана с регуляцией клеточного роста и дифференцировки. Крейн предполагает возможное участие локализованного в плазмалемме CoQ в активации тирозин киназы и запуске ряда сигнальных путей, приводящих к ранней экспрессии генов [10]. В результате окисления убисемихинона образуется перекись водорода, индуцирующая тирозин киназу (H2 O2 скорее всего выполняет сигнальную роль).
CoQ также участвует в экстра-митохондриальном электронном транспорте. Лизосомы тоже содержат НАДН-зависимую CoQ редуктазу, которая, возможно, участвует в образовании кислой среды лизосомального люмена. В этом случае восстановление CoQ рассматривается как два последовательных одноэлектронных процесса, с участием ФАД и цитохрома b5 , а молекулярный кислород выступает в роли терминального акцептора [37].
CoQ принимает участие в регуляции физико-химических свойств мембран, проницаемости митохондриальных мембран (взаимодействует с РТР, permeability transition pore) и в активации митохондриальных разобщающих белков (uncoupling proteins, UCP).
Во внутренней мембране митохондрий локализован ряд белков-разобщителей (uncoupling proteins, UCPs), которые способны транслоцировать протоны из межмебранного пространства внутрь митохондрий [38]. Создаваемый дыхательной цепью протонный градиент оказывается разобщенным с процессом окислительного фосфорилирования, и запасаемая в виде ΔμH энергия частично рассеивается, не переходя в энергию макроэргических связей АТФ.
Известно пять различных белков-разобщителей в митохондриях многих растений и животных (гены ucp 1-5 для человека). Наиболее изученный белок UCP1 локализован в буром жире, он активно функционирует и ответственен за термогенез. В остальных тканях, где разобщение не играет такой масштабной роли, белки-разобщители представлены в небольших количествах. Помимо термогенеза, предполагается участие UCPs в подавлении генерации кислородных радикалов, а также их причастность к таким болезням, как ожирение и диабет. Эчтай (Echtay) использовал липосомы со встроенными в них бактериальными UCPs и показал, что CoQ является облигатным кофактором для этих белков [12]. Добавление CoQ в смеси с жирными кислотами к липосомам активировало транспорт протонов разобщающими белками, и наоборот, транспорт прекращался в отсутствие коэнзима Q. При этом CoQ с маленькой длиной изопреноидного хвоста (0-2 единицы) практически не взаимодействуют с UCPs, максимальная же активность наблюдается при введении CoQ10. Предполагается следующая схема участия CoQ в функционировании UCP: протон с жирных кислот переносится молекулой CoQ на некоторую акцепторную группу белка-переносчика, который уже переправляет его в матрикс.
Внутренняя мембрана митохондрий малопроницаема для различных ионов и небольших молекул. Транспорт необходимых веществ осуществляется через специальные белковые транспортеры и ионные каналы. Такая непроницаемость необходима для формирования протонного градиента, но иногда, вследствие явления неспецифической проницаемости мембраны (мембрана теряет свои барьерные функции и становится проницаемой для всех молекул с молекулярной массой до 1,5 кДа), протонный градиент теряется, нарушается баланс ионов, происходит гидролиз АТФ [21].
Кроме того, показана критичность резкого изменения проницаемости внутренней митохондриальной мембраны при апоптозе, одной из начальных стадий которого является выход проапоптических белков из митохондрий в цитоплазму (цитохром с , прокаспаза-9 и др.) [22]. Такая неспецифическая проницаемость связана с особым внутренним митохондриальным комплексом РТР (permeability transition pore) [13]. На комплекс РТР влияет целый ряд факторов (более 40), в том числе концентрация ионов кальция в матриксе, скачки мембранного потенциала, рН матрикса, циклоспорин А, окисленные глутатион и пиридиновые нуклеотиды, образующиеся при оксидативном стрессе, коэнзим Q и его гомологи (и как ингибиторы, и как индукторы). Предполагается, что хиноны влияют на РТР через взаимодействие с неким сайтом связывания, а не через характерные окислительно-восстановительные реакции [23]. Похоже, что в случае использования аналогов CoQ играет роль не тип заместителей в бензохиноновом кольце, а длина и степень насыщенности изопреноидной цепи. Коэнзим Q (как ингибитор) способен предотвращать деполяризацию внутренней митохондриальной мембраны, выход цитохрома с и активацию каспазы-9 в кераноцитах в ответ на апоптические стимулы, в связи с чем можно предположить его ингибирующий эффект на открытие неспецифической митохондриальной поры.
Также CoQ участвует в модуляции количеств β2-интегринов, презентируемых на поверхности моноцитов крови и в восстановлении функций эндотелия в случае их нарушения. Еще он окисляет сульфид в дрожжах и принимает участие в образование дисульфидных связей в бактериях.
Физико-химические свойства кофермента Q
Кофермент Q является редокс-компонентом митохондриальной или бактериальной электрон-транспортной цепи. Он существует преимущественно в двух формах – окисленной (убихинон) и восстановленной (убихинол) (рис.15). Убихинон (UQ) – это 2,3-диметокси-5-метил-бензохиноновое кольцо, соединенное в шестом положении с гидрофобным изопреноидным хвостом (от 6 до 10 звеньев). Бензохиноновое кольцо обладает относительной полярностью по сравнению с длинной боковой цепью (является чем-то вроде полярной головки), но при этом и достаточно гидрофобно, потому что включено в мембранный бислой. Принимая два элетрона и два протона от митохондриальных убихинон-редуктаз, UQ восстанавливается до ароматического убихинола (UQH2 ).
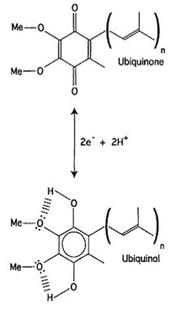
Рисунок 15: Кофермент Q и его редокс-формы (убихинон/убихинол)(James et. al, 2004).
Как убихинон, так и убихинол хорошо растворимы в обычных липидных растворителях: ацетоне, диэтиловом эфире, хлороформе, этаноле, петролейном эфире,- которые и используются для экстракции CoQ из мембран. Коэффициенты распределения хинолов в системе циклогексан/ вода обычно ниже, чем для хинонов, поскольку появляются два доступных для формирования водородных связей протонов. При этом метокси-группы в положениях 2 и 3 у CoQ в достаточной степени выравнивают эти коэффициенты, так как образуется внутримолекулярная водородная связь (рис.15), и протон гидроксильной группы становится гораздо менее доступным для образования внешних водородных связей. Коэффициенты распределения в системе октанол/вода для хинонов и хинолов также схожи, поскольку водородные связи с октанолом образуются в равной степени для обеих редокс-форм. Таким образом, окисленная и восстановленная формы CoQ будут, в грубом приближении, одинаково распределяться в мембранном бислое: как в его центре, схожем по гидрофобности с циклогексаном, так и ближе к поверхности, схожей с октанолом [35].
Помимо двух основных наиболее стабильных форм, кофермент Q имеет еще и другие короткоживущие нестабильные протонированные и окисленные формы, участвующии в процессах последовательного одноэлектронного переноса электронов в клетке (рис. 16)
Так, в реакции окисления UQH2 до UQH2 + убихинол представляет собой весьма слабый восстановитель (> 850 мВ), тогда как образующийся при потере протона анион UQH– (1) уже более активен (~190 мВ), и может отдать электрон мягким клеточным окислителям (2). Получившийся убисемихинон-радикал UQH* отдает второй протон (3), образуя убисемихинон радикал анион UQ– , который является сильным восстановителем (j~ -240 ¸ -230 мВ); последний отдает электрон и превращается в убихинон UQ (4).
Обратная реакция восстановления убихинона до анионной формы радикала может быть осуществлена только сильными восстановителями (5), при этом последующая стадия образования аниона UQ2- проходит легко (6). Анион же, в свою очередь, присоединением двух протонов превращается в убихинол. В данном случае в ходе восстановления убихинона происходит последовательное присоединение сразу двух электронов, тогда как при окислении убихинола перенос электронов разделен акцептированием протонов.
Содержание CoQ в митохондриях различных тканей неодинаково (1-4.5 нмоль CoQ на мг белка (у грызунов)). Так больше всего CoQ на мг белка приходиться на клетки сердечной и скелетных мышц, а на клетки мозга и печени приходиться всего 1 нмоль CoQ на мг белка. Кофермент Q свободно перемещается в билипидном слое внутренней мембраны. Изопреноидный хвост располагается в центре бислоя параллельно поверхности, заякоривая молекулу внутри мембраны. Бензохиноновое кольцо также погружено в мембрану, но способно менять свою пространственную ориентацию, тем самым, обеспечивая перенос электронов: кольцо может располагаться как в середине бислоя параллельно поверхности, так и вдоль ацильных цепей перпендикулярно поверхности, но не ближе1-2 нм к поверхности. Таким образом, CoQ не взаимодействует с растворенными в матриксе восстановителями типа глутатиона и аскорбата.
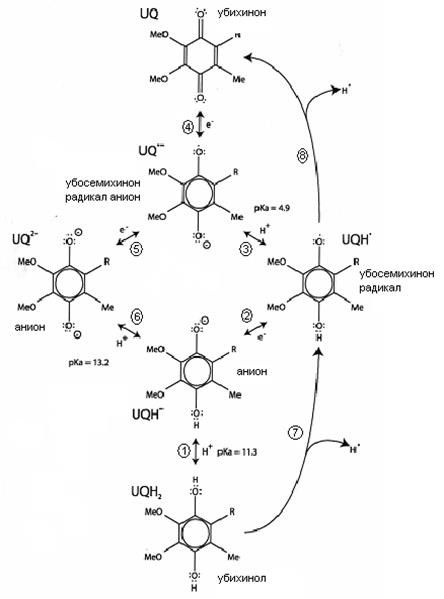
Рисунок 16: Редокс-формы СoQ и их взаимопревращения
Для гомологов CoQ c достаточно длинной боковой цепью молекулярная динамика и минимизация энергии показали свернутую структуру молекулы: последняя изопреноидная единица находится в тесном контакте с бензохиноновым кольцом. То же показано для анионных и радикальных интермедиатов с помощью EPR [9].
Таким образом, убихинон объединяет в себе свойства донора двух электронов и акцептора одного электрона, подобно другим важным переносчикам в цепи - флавопротеинам [35].
Вообще перенос восстановительных эквивалентов представляет собой векторный процесс, в результате которого создается ΔμH. К дегидрогеназам, принимающим восстановительные эквиваленты от различных субстратов и переносящим их на СоQ, относятся: комплекс I (НАДН -убихинон оксидоредуктаза – входит в состав), комплекс II (сукцинатдегидрогеназа), дигидрооротат дегидрогеназа, глицерол-3-фосфат дегидрогеназа, а также ряд растительных и дрожжевых НАДН-дегидрогеназ, не участвующих в создании протонного градиента. Эти ферментативные комплексы восстанавливают убихинон до убихинола, а он, в свою очередь, окисляется комплексом III (в клетках млекопитающих) или рядом альтернативных оксидаз (дрожжи, растения). Комплекс III осуществляет векторный транспорт электронов от убихинола к цитохрому с .
Комплекс III (комплекс bc1 или убихинол цитохром с оксидоредуктаза)
Комплекс III представляет собой димер из двух идентичных мономеров, состоящих из 11 белковых субъединиц. Функциональное ядро каждого мономера состоит из трех субъединиц: цитохрома b (содержит два гема bh (566) и bl (562) ), белка Риске с железосерными кластерами 2Fe-2S и цитохрома с1 с одним гемом с (рис 17).
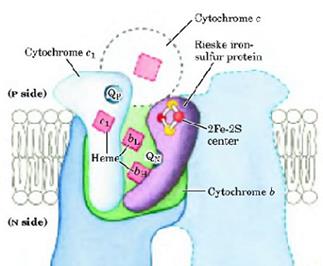
Рисунок 17: Функциональное ядро комплекса III.
Цитохром b – белок массой около 45 кДа - погружен в мембрану и состоит из 9 α-спиралей, 8 из которых пересекают мембрану (трансмембранные). Это полипептид кодируется мтДНК. Цитохром b (рис. 20) содержит два гемма - bh и bl , которые расположены между 2ой и 5ой α-спиральными колоннами и связаны с белком по крайней мере тремя связями. Две из них образуются имидазольными группами остатков гистидина белка и железом гемма, а третья – положительно заряженной группой остатков аргинина или лизина белка и отрицательно заряженной пропионатной группой гемма. Гемм bl , расположен ближе к межмембранному пространству, а bh - ближе к цитозолю (рис. 19).
FeSIII белок (белок Риске или фактор Слейтера) – полипептид массой 21,5 кДа (состоит из 199 аминокислот), который содержит один 2Fe-2S кластер (рис. 12). BAL и Zn сильно тормозят перенос электронов с Fe-2 кластера на цитохром с .
Цитохром с1 , белок массой 28 кДа, содержит один гем с (рис. 19), который вместе с железо-серным белком комплекса III образует место связывания с цитохром с на обращенной в межмембранное пространство стороне внутренней мембраны.
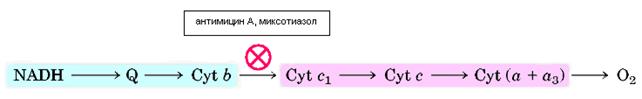
В комплексе bc1 есть два сайта взаимодействия с коэнзимом Q - QN и Qp (рис. 17). Субъединицы комплекса III взаимодействуют между собой с образованием двух «карманов», где и происходят реакции Q-цикла. Сайт QN находится ближе к обращенной к матриксу стороне мембраны (сторона N), и именно с ним связывается ингибитор дыхания антимицин А , блокируя перенос электрона с гема bh на убихинон. Сайт Qp находится ближе к межмембранному пространству (сторона Р), и с ним связывается другой ингибитор– миксотиазол , блокируя перенос электрона с убихинола на железосерный кластер.
Общее соотношение UQH2 /UQ в CoQ пуле определяется интенсивностью дыхания клетки. В состоянии 4, когда митохондрия не синтезирует АТФ, уровень дыхания низкий, и пул CoQ относительно восстановлен. В состоянии же 3, когда происходит активный синтез АТФ, дыхание идет быстро, приводя к окислению пула CoQ. В изолированных митохондриях доля восстановленной формы в случае низкой интенсивности дыхания составляет 75-90%, а в случае высокой– 50-60% (молекула CoQ изменяет свой редокс-статус каждые 50 мсек) [35]. Ингибирование комплексов III и IV и добавление субстратов для комплекса I или II сдвигает соотношение UQH2 /UQ в сторону восстановленной формы, и наоборот.
В ходе Q-цикла две молекулы UQH2 окисляются в Р-сайте, высвобождая в межмембранное пространство по два протона на каждую молекулу; один электрон от каждой молекулы UQH2 идет на цитохром с1 , а второй– на расположенную в N-сайте молекулу UQ через гемы цитохрома b. Таким образом, принимая последовательно два электрона от двух молекул UQH2 и два протона, одна молекула UQ восстанавливается, при этом промежуточным интермедиатом является убисемихинон анион радикал:
UQH2 +UQ′ + Сyt c1 ( ox) → UQ′.– + 2H+ p + Сyt 1 (red) + UQ,
UQH2 + UQ′.– + 2H+ N + Сyt c1 (ox) → UQH′2 + UQ + 2H+ p + Сyt с1 (red)
Несмотря на сложность процесса, результирующая реакция проста, и отражает перенос электронов с убихинола на цитохром c1 и транспорт протонов через мембрану:
UQH2 + 2 Сyt c1 (ox) + 2H+ N → Q + 2 Сyt c1 (red) + 4H+ p .
В ходе данного процесса происходит миграция молекул CoQ в толще мембранного бислоя между сайтами Qp и QN и образование в этих сайтах убисемихинон радикалов.
С цитохрома c1 электрон передается на цитохром с , который восстанавливает цитохромоксидазу.
Цитохром с является относительно небольшим (масса 12кДа, состоит из 104 аминокислот) водорастворимым белком, локализованным на межмембранной поверхности внутренней митохондриальной мембраны. Он содержит гемм с (рис. 19), ковалентно связанный с апобелком. Цитохрома c совершает челночные движения между цитохромом c1 и цитохромоксидазой, перемещаясь вдоль поверхности мембраны. Кардиолипин участвует в связывании цитохрома с с мембраной.
Комплекс IV (цитохромоксидаза).
Это последний комплекс дыхательной цепи, передающий электроны от цитохрома с на молекулярный кислород, окисляя его до Н2 О. Цитохромоксидаза - это большой фермент (масса 240 кДа) внутренней мембраны митохондрий, состоящий из 13 субъединиц у млекопитающих, и 3 или 4 - у бактерий. Функциональное ядро содержит четыре редокс-центра: два гемма а -типа (гемм а и гемм а3 ) (рис. 20) и два атома меди (CuA и CuB ) (рис.21).
10 регуляторных субъединиц комплекса кодируются ядерным геномом и синтезируются в цитоплазме: IV (17 кДа), V (12,5 кДа), VIa (10,5 кДа), VIb (9,5 кДа), VIc (8,5 кДа), VII (10 кДа), VIIIa (5,5 кДа), VIIIb (5 кДа), VIIIc (6 кДа).
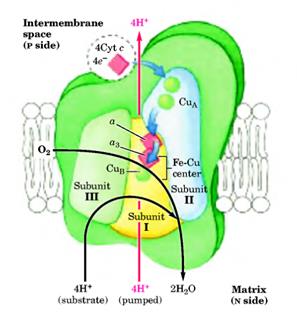
Рисунок 21: Комплекс IV.
Три субъединицы этого комплекса кодируются митохондриальным геномом. Субъединица III (30 кДа) 7 раз пересекает мембрану. Субъединица II (26 кДа) содержит CuA -центр, состоящий из двух ионов Cu в комплексе с –SH группами двух Cys (похож на 2Fe-2S-центр). Кроме того, в субъединице II находятся две гидрофобные последовательности, два раза пересекающие мембрану. Субъединица I (57 кДа) содержит остальные редокс-центры, как-то: две группы геммов а и а3 и CuB -центр. Гемм а3 и CuB формируют второй двуядерный центр, который принимает электроны с гемма а и передает их на О2 , связанный с геммом а3 . Таким образом, электрон с цитохрома с передается на CuA -центр, далее на гемм а , а после на гемм а3 - CuB –центр. С CuB –а3 – центра электрон переноситься на кислород. Ингибиторами этой реакции являются KCN, CO, H2S и азид.
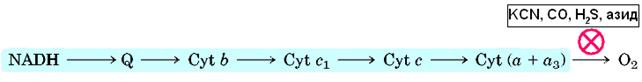
На каждые четыре электрона, проходящие через комплекс, фермент принимает четыре субстратные Н+ из матрикса (N-side) для восстановления О2 в Н2 О. Так же фермент использует энергию этой реакции для переноса через мембрану в межмембранное пространство одного Н+ на каждый перенесенный электрон.
Суммарная реакция, катализируемая цитохромоксидазой:
4 Cyt c ( red) + 8 Н+ N + О2 →4 Cyt c ( ox) + 4 Н+ p + Н2 О
Это четырехэлектронное восстановление О2 затрагивает редокс центры, которые несут только по одному электрону, что вызывает образование интермидиатов (перекиси водорода и гидроксильного радикала), которые связываются комплексом до образования воды.
В итоге, на каждую пару электронов, переносимую на молекулу О2 приходиться четыре Н+ , выкаченных комплексом I, четыре – комплексом III и два – комплексом IV (рис. 22).
Векторное уравнение этого процесса можно записать следующим образом:
NADH + 11 Н+ N + 1/2О2 → NAD+ + 10 Н+ p + Н2 О
Таким образом, перенос двух электронов от NADH к О2 сопровождается переносом через мембрану 10 Н+ , в результате чего протоны в межмембранном пространстве накапливаются, создавая протонный градиент. Н+ -АТФ-синтаза – фермент, катализирующий фосфорилирование АДФ неорганическим фосфатом с образование АТФ за счет электрохимическая энергия протонного градиента ΔμН. Синтез АТФ сопряжен с обратным потоком протонов из межмембранного пространства в матрикс.
Первой была открыта и изучена бактериальная Н+ АТФ-синтаза, митохондриальная Н+ АТФ-синтаза имеет аналогичное строение.
Н+ -транслоцирующая АТФ-синтаза E. coli состоит из двух субкомплексов: встроенного в мембрану протонного канала (F0 ) и каталитической субъединицы (F1 ), выступающей в матрикс (рис.23). Фактор F0 состоит из трех типов субъединиц (а (30 кДа), b (17 кДа), с (8 кДа)), а фактор F1 -из пяти (α (55 кДа), β (50 кДа), γ (31,5 кДа), δ (19,5 кДа), ε (15 кДа)) (рис. 25). Так, «головка» каталитической части образована тремя α- и тремя β- субъединицами, между которыми расположены три активных центра. "Ствол" структуры образуют полипептиды F0 -части и γ-, δ- и ε-субъединиц головки.
Митохондриальная Н+ АТФ-синтаза гомологична бактериальной, но несколько тяжелее и сложнее устроена. Так, в Н+ АТФ-синтазе митохондрий присутствуют пять полипептидов, которые отсутствуют у бактерий: ε-субъединица фактора F1 (5,5 кДа), субъединица AL6 фактора F0 (22 кДа), фактор F6 (9 кДа), белковый ингибитор фактора F1 (9,5 кДа), субъединица правильного связывания F1 с F0 (18,5 кДа). Белок OSCP – это белок, обусловливающий чувствительность к олигомицину. Он необходим для правильного связывания F1 с F0. Крупные α- и β- субъединицы очень консервативны (70% сходства), а белок OSCP гомологичен частям δ- и b- субъединиц E. coli , субъединица 9 гомологична субъединице с E. coli .
У животных и дрожжей все субъединицы фактора F1 кодируются ядерным геномом и синтезируются в цитоплазме; у растений, α-субъединица закодирована в мтДНК, а β- субъединица – в ядре, другие сведения отсутствуют.
Н+ АТФ-синтаза – это очень массивный белковый комплекс, локализованный во внутренней мембране митохондрий. Н+ АТФ-синтаза сильно выдается своей каталитической частью (фактором F1) в матрикс митохондрии. Каталитический цикл (рис.26) подразделяется на три фазы, каждая из которых проходит поочередно в трех активных центрах. Вначале происходит связывание АДФ и Фн (1), затем образуется фосфоангидридная связь (2) и, наконец, освобождается конечный продукт реакции – АТФ (3). При каждом переносе протона через белковый канал F0 , в матрикс все три активных центра катализируют очередную стадию реакции.
Согласно хемиосмотической концепции, движение электронов по дыхательной цепи является источником энергии для транслокации протонов через митохондриальную мембрану. Возникающая при этом разность электрохимических потенциалов (ΔμH+ ) приводит в действие АТФ-синтазу, катализирующую реакцию АДФ+ Фн D АТФ.
В дыхательной цепи есть только 3 участка, где перенос электронов сопряжен с накоплением энергии, достаточным для образованияАТФ, на других этапах возникающая разность потенциалов для этого процесса недостаточна. Максимальная величина коэффициента фосфорилирования, таким образом, составляет 3, если реакция окисления идет с участием НАД+ , и 2, если окисление субстрата протекает через флавиновые дегидрогеназы. Теоретически еще одну молекулу АТФ можно получить в трансгидрогеназной реакции (если процесс начинается с восстановленного НАДФ):
НАДФН + НАД+ D НАДФ+ + НАДН + 30 кДж/моль.
Обычно в тканях восстановленный НАДФ используется в пластическом обмене, обеспечивая разнообразные синтетические процессы, так что равновесие трансгидрогеназной реакции сильно сдвинуто влево.
Эффективность окислительного фосфорилирования в митохондриях определяется как отношение величины образовавшегося АТФ к поглощенному кислороду: АТФ/О или Р/О (коэффициент фосфорилирования). Экспериментально определяемые значения Р/О, как правило, оказываются меньше 3. Это свидетельствует о том, что процесс дыхания не полностью сопряжен с фосфорилированием. Действительно, окислительное фосфорилирование, в отличие от субстратного, не является процессом, в котором окисление жестко сопряжено с образованием макроэргов. Степень сопряжения зависит главным образом от целостности митохондриальной мембраны, сберегающей разность потенциалов, создаваемую транспортом электронов. По этой причине соединения, обеспечивающие протонную проводимость (например, 2,4-ди-нитрофенол), являются разобщителями.
В норме скорость митохондриального транспорта электронов регулируется содержанием АДФ. Выполнение клеткой функций с затратой АТФ приводит к накоплению АДФ, который в свою очередь активирует тканевое дыхание. Таким образом, клетки реагируют на интенсивность клеточного метаболизма и поддерживают запасы АТФ на необходимом уровне, т.е. осуществляют дыхательный контроль.
За сутки человек потребляет около 550 л (24,75 моля) кислорода. Если считать, что в тканевом дыхании за этот период восстанавливается 40 г атомов кислорода (20 молей), а величину Р/О принять за 2,5, то в митохондриях должно синтезироваться 100 молей, или около 50 кг АТФ! При этом часть энергии окисления субстратов расходуется на совершение полезной работы, не превращаясь в АТФ.
В дыхательной цепи электроны не всегда достигают места назначения – нередко они выпа-дают из цепи, образуя активные формы кислорода (АФК), концентрация которых в матриксе в 5-10 раз превышает содержание оных в цитоплазме. Что же собой представляют АФК?
Антиоксиданты и механизм образования активных форм кислорода в клетке.
Механизм образования активных форм кислорода
Потребляемый организмом кислород практически полностью (95-98%) расходуется на выработку энергии и окислительный катаболизм субстратов, и лишь малая его часть переходит в активные формы кислорода (уровень АФК в тканях равен примерно 10-8 М).
Конфигурация внешней электронной оболочки атома кислорода 2S2 2P4 . Молекула кислорода двухатомна. В основном состоянии (триплетное 3 ∑- g ) два валентных электрона молекулы О2 , находящиеся на разрыхляющих орбиталях πх и πу , не спарены (рис. 25) и, таким образом, молекула кислорода является бирадикалом. Помимо основного, существуют еще два долгоживущих возбужденных состояния О2 - синглетное 1 Δg (энергия возбуждения 94,1 кДж/моль, время жизни 45 мин) и синглетное 1 ∑+ g (энергия возбуждения 156,8 кДж/моль).
Рисунок 25: Схема распределения электроном по атомным орбиталям молекулы кислорода.
Существует также аллотропная модификация кислорода - азон О3 .Озон образует озониды, в которых ионная форма кислорода - О- 3 . Молекула кислорода образует три различные ионные формы, каждая из которых дает начало классу соединений: О- 2 - супероксидам, О2 2- - пeроксидам, О+ 2 - диоксигенильным соeдинениям.
Молекула кислорода, присоединяя дополнительный электрон, образует высоко реакцион-носпособный супероксид-радикал (•О2 - ). Супероксид может порождать вторичные АФК:
- присоединяя еще один электрон, образует короткоживущий пероксид-анион (•О2 2- ), который легко связывает протоны и вследствие этого переходит в Н2 О2
- присоединяя NO, образует пероксинитрит (образуется при избытке О2 - )
- переводит трехвалентное железо Fe3+ в двухвалентное Fe2+ , которое при взаимо-действии с Н2 О2 , НClО и липоперекисями образует гидроксильный радикал ОН* или липоксильный радикал LO* (образуется при избытке О2 - )
- присоединяя 2 протона и электрон, образует перекись кислорода Н2 О2 (основной продукт).
Присоединение электрона к Н2 О2 ведет к расщеплению молекулы на ионы О2- и О- . В то время как О2 - путем присоединения двух протоны образует воду, протонирование О- приводит к особо опасному гидроксил-радикалу (ОН- ). Присоединение еще одного электрона и заключительное протонирование ОН- заканчивается образованием воды (рис. 26).
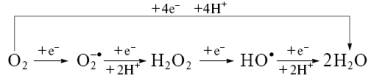
Донорами электронов могут быть Fe2+ , Cu+ (из активных центров) или семихиноны, а для второй и третей реакций – также и О2 - :
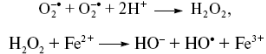
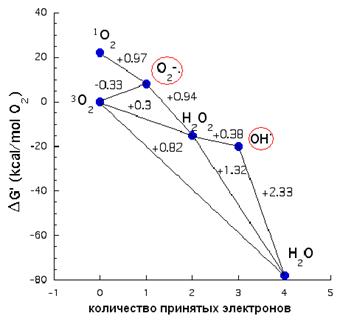
Рисунок 26: АФК.
В клетке активные формы кислорода возникают в результате различных окислитель-восстановительных реакций, протекающих в ней. К АФК относятся супероксид анион-радикал O2 .- , перекись водорода H2 O2 , гидроксильный радикал (ОН- ), синглетный O2 , озон O3 , гипохлорид НClО, окись азота NO и ряд других кислородсодержащих веществ, обладающих высокой окислительной активностью и способных повреждать редокс-чувствительные компоненты клетки, прежде всего белки, липиды и нуклеиновые кислоты.
Раньше полагали, что АФК являются исключительно токсичными для клетки метаболитами и поэтому в клетке существует множество систем для борьбы с ними. Но по мере изучения АФК стало ясно, что они не всегда пагубно влияют на клетку.
К настоящему времени накопилось немало сведений о сигнальной роли АФК, хотя конкретных метаболических путей, в которых могут участвовать АФК, в большинстве случаев еще не выявили. Так, например, есть данные, что АФК участвуют в качестве сигнальных молекул при активации транскрипционных факторов AP-1 и NF-κB и индукции экспрессии генов при иммунном ответе. АФК могут выступать и в качестве индукторов клеточной гибели или наоборот, ингибировать цитотоксическое действие терапевтических препаратов на опухолевые клетки [44]. Возможно, что АФК могут выступать в роли митотических стимуляторов.
Существуют также данные об участии АФК в регуляции редокс-статуса и окислительных модификаций белков.
Регуляция редокс-сигнализации может осуществляться как через общий уровень глутатиона (GSH) в клетке, так и через соотношение GSH/GSSH (рис.29). Глутатион (трипептид Glu-Cys-Gly) находитсяся почти во всех клетках в высокой концентрации и содержит нетипичную γ-связь между Glu и Cys. Восстановителем здесь является тиольная группа цистеинового остатка. Две молекулы восстановленной формы (GSH) при окислении образуют дисульфид (GSSG) (рис. 27). Окислительные модификации затрагивают, как правило, остатки цистеина в функциональных доменах различных белков, приводя к инактивации ферментов, изменению способности связывания транскрипционных факторов с ДНК и другим функциональным нарушениям. При понижении уровня восстановленного глутатиона нарушается проведение сигнала от ряда рецепторов факторов роста и связывание транскрипционных факторов с ДНК, подавляется рост и размножение многих клеточных типов.
Рисунок 27: Глутатион.
Источником АФК в клетке является множество различных ферментативных и неферментативных систем. Одним из главных генераторов АФК в клетке являются пероксисомы, в которых локализован целый ряд образующих перекись водорода ферментов. Эта перекись используется клеткой в основном для детоксикации ксенобиотиков, и практически вся утилизируется внутри этих органелл. В гладком эндоплазматическом ретикулуме локализован ряд цитохром-зависимых оксигеназ, продуцирующих супероксид O2 . – . Очень много образуется АФК в эритроцитах. В плазмалемме макрофагов и эндотелиоцитов существует НАД(Ф)Н-оксидазная система, продуцирующая супероксид анион в ходе иммунного и воспалительного ответа. Остеокласты (специализированные макрофаги) применяют АФК для разрушения кости – обязательное условие ее обновления. При этом клетки-защитники быстро поглощают большое количество O2 (дыхательный взрыв), образуя внешней стороны мембраны супероксид O2 .– за счет окисления цитозольного НАД(Ф)Н.
![]()
В клетках образование АФК происходит еще и потому, что в дыхательной цепи митохондрий происходит утечка электронов с комплексов I и III и за счет этого в среднем около 2% поступающего кислорода переходит в активную форму, при этом часть АФК идет на оксидативную модификацию макромолекул. Продукция O2 .– в митохондриях осуществляется несколькими различными путями и значительно зависит от активности дыхания (состояние 3 или 4) и изменений парциального давления кислорода (гипоксия или реоксигенация). Митохондрии более всех других органелл подвержены атаке АФК и, как следствию, повреждению мембранных липидов, углеводов, белков и ДНК, причем для гибели митохондриям не требуется никаких дополнительных белков, кроме тех, которые присутствуют в них самих. Окислительный стресс является причиной множества дегенеративных заболеваний, старения и гибели клетки.
Основным местом утечки электронов из дыхательной цепи и, следовательно, образования O2 .– является убихинол цитохром с оксидоредуктаза, где генерация происходит за счет одноэлектронного восстановления молекулярного кислорода от убисемихинона [43]. В НАДН-убихинон-редуктазе источником O2 .– служит семихиноновая форма флавина. При изменении интенсивности потока электронов и степени восстановленности компонентов дыхательной цепи митохондрий йзменяется и количество выпадающих электронов. Так, например, в присутствии цианида и ротенона продукция супероксида понижается, а при добавлении ингибитора комплекса III антимицин А (приводит к увеличению пула семихинонов), образование АФК в следствии окисления субстрата I или II комплексами увеличивается, в то время как (рис.28).
В условиях высокого Δψ в дыхательной цепи усиливается обратный транспорт элект-ронов, и тогда главным продуцентом супероксида становиться комплекс I. При повыше-нии митохондриального трансмембранного потенциала (Δψ) становится дыхательная цепь становиться более восстановленной, что увеличивает образование АФК в Q-цикле.
Рисунок 28: Электрон-транспортная цепь и сайты генерации АФК. Антиоксидантные системы клетки[15]
Как уже было сказано выше, АФК очень реакционноспособные и легко переходят из одной формы в другую (рис. 29), окисляя при этом различные молекулы. Так, в результате утечки электронов из дыхательной цепи и в реакциях НАД(Ф)Н-оксидазы и ксантин-оксидазы первым образуется супероксид анион радикал, который очень быстро дисмутирует до перекиси водорода.
Из всевозможных восстановленных форм кислорода перекись водорода является самым стабильным соединением и обладает меньшей реакционной способностью, нежели другие формы. Молекула H2 O2 способна перемещаться в клетке на значительные расстояния и довольно долго сохраняться в ней. Скорее всего, перекись не достаточно активна, чтобы как-то сильно повредить клеточным структурам, а играет роль сигнальной молекулы. При этом в присутствии активаторов, как-то: ионов меди и ионов железа (образуются при окислении железо - серных центров ряда ферментов кислородными радикалами), - из перекиси и супероксида образуется гидроксильный радикал. Гидроксильный радикал является самым опасным и обладает наивысшей реакционной способностью среди всех АФК. Он мог бы разрушить практически все клеточные структуры, но имеет очень маленькое время жизни (около нескольких наносекунд) и не способен диффундировать на значительные расстояния от места образования.
Также супероксид способен реагировать с оксидом азота (II) (обладает сосудо-расширяющим действием) с образованием активного оксиданта пероксинитрита.
При избытке супероксида, он может переводить трехвалентное железо Fe3+ в двухвалентное Fe2+ , которое при взаимодействии с Н2 О2 , НClО и липоперекисями образует гидроксильный радикал ОН* или липоксильный радикал LO* .
+H+
![]()
![]() Fe2+ + H2O2 [(FeIV=O)2+ + H2O] Fe3+ + H2O + HO.
Fe2+ + H2O2 [(FeIV=O)2+ + H2O] Fe3+ + H2O + HO.
![]()
![]() Cu+ + H2O2+ H+ [(CuIII-OH)2+ + H2O] Cu2+ + H2O + HO.
Cu+ + H2O2+ H+ [(CuIII-OH)2+ + H2O] Cu2+ + H2O + HO.
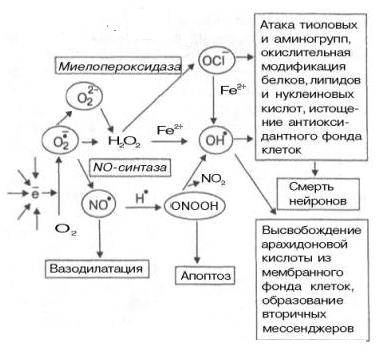
Рисунок 29: Переход из одних форм АФК в другие и воздействие на клетку.
Когда митохондрии перестают справляться с проблемой детоксикации образуемых ими АФК, усиливается дисбаланс между их (АФК) генерацией и нейтрализацией, что приводит к так называемому окислительному стрессу. В результате избыточного образования кислородных радикалов, последние начинают выполнять в основном деструктивные функции, нежели служат в качестве сигнальных молекул. Происходят специфические изменения множества клеточных компонентов: повреждаются мембранные структуры из-за перекисного окисления липидов, происходит окисление белков по остаткам тирозина, цистеина и серина, повреждение ДНК, смещение редокс-потенциала клетки из-за окисления глутатиона и НАД(Ф)Н.
Так, примером действие АФК в условиях, способствующих их избыточному образованию, может служить избыток O2 , особенно при гипербарической оксигенации (лечение кислородом под повышенным давление), сильного спазма (характерен для инфаркта миокарда или инсульта головного мозга) и реперфузии миокарда после периода ишемии (возобновление кровотока после его нарушения из-за тромбоза, т.е. закупорки сосуда), сопровождающаяся развитием повреждений, сопоставимых по степени с возникшими в результате самой ишемии. Механизм образования АФК при реперфузии, вероятно, обусловлен созданием условий, благоприятствующих образованию вторичных радикалов. Во время ишемии парциальное давление кислорода в кардиомиоцитах резко снижается, и это сопровождается переходом окисленных атомов железа Fe3+ в восстановленные Fe2+ , а также повышением активности ксантиноксидазы. Оба эти компонента при появлении в цитоплазме больших количеств кислорода в начале реперфузии резко активируют образование ОН* , и возникающее под действием этого радикала повреждение клеточных структур может приобретать необратимый характер, что вызывает развитие апоптоза
Самым распространенным патологическим состоянием, приводящим к значительной вспышке продукции АФК, является гипоксия и последующая реоксигенация. В ходе продолжительной гипоксии происходит множество изменений в активности ряда клеточных ферментов, истощение и повреждение антиоксидантных защитных систем и быстрое восстановление компонентов дыхательной цепи за счет обращения АТФ-синтазной реакции, используемой для создания протонного градиента в условиях недостатка кислорода. В результате всех этих изменений при последующей реоксигенации утечка электронов с комплексов дыхательной цепи и генерация супероксида значительно увеличивается.
В условиях нормоксии повышенная генерация активных форм кислорода, приводящая к окислительному стрессу, наблюдается обычно только в очагах воспаления. В данном случае кислородный взрыв обусловлен деятельностью НАДФН-оксидазных систем макрофагов и является жестко регулируемым, оказывая деструктивное влияние только на клетки, на которые направлена иммунная реакция.
Поскольку образование АФК в клетках любых аэробных организмов происходит непрерывно, то клетках должны быть и защитная система против их пагубного влияния.
Защита клетки от избытка кислородных радикалов и снижение вызванных ими окислительных повреждений осуществляется двумя принципиально разными механизмами:
1. снижение образования первичных АФК (супероксида) путем уменьшения кислорода в клетке или его более быстрого использования дыхательной цепью ввиду снятия ее контроля ∆μН+
2. функционированием антиоксидантной системы, которая включает антиоксидантные ферменты, низкомолекулярные соединения, образующие редокс-буфер, витамины, альбумины, свободные жирные кислоты и комплексоны ионов металлов (рис. 30).
К нейтрализующим АФК ферментам относятся супероксиддисмутазы (СОД), каталаза и пероксидазы. СОД катализирует дисмутацию двух молекул супероксида с образованием перекиси водорода и O2. Изоформы этого фермента присутствуют во всех клеточных компартментах, где возможно образование супероксида, нейтрализуя O2.-. Образующаяся при дисмутации супероксида перекись нейтрализуется каталазой или глутатион- и тиоредоксин- пероксидазами в пероксисомах.
Внутриклеточный редокс-статус обеспечивается системой тиолов, в первую оче-редь глутатиона (GSH) и тиоредоксина (TRX), которые создают буферную систему для поддержания более восстановленных по сравнению с внеклеточной средой условий.
Глутатион (GSH) и тиоредоксин (TRX) являются важнейшими антиоксидантами в клетке. Глутатион участвует в поддержании редокс-статуса за счет нейтрализации перекиси глутатион-пероксидазой.
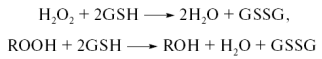
Образовавшейся НАДФН+Н+ поставляет Н+ для регенерации восстановленного глутатиона (GSH) из глутатион-дисульфида (GSSG) с помощью глутатион-редуктазы.
![]()
В условиях окислительного стресса соотношение GSН/GSSG быстро падает из-за окисления глутатиона, но быстро восстанавливается до исходного уровня. При этом в организме в случае исчерпания GSH в какой-либо ткани, обеспечение может происходить за счет выброса его в кровь из депо (печень) [49]. Тиоредоксин действует как восстановитель дисульфидных связей в белках и донор электронов для TRX-пероксидазы, при это не оказывая влияния на продукцию АФК или количество восстановленного глутатиона. Восстанавливается тиоредоксин с помощью тиоредоксин-редуктазы и НАДФН [50].
Когда митохондрии перестают справляться с проблемой детоксикации АФК, происходит разрушение митохондриальных структур от мембраны до мтДНК. Из АФК только ОН- вызывает повреждения ДНК (окисление оснований, их модификации, повреждение хромосом). Подобные мутации могут привести к патологии и гибели клеток или их злокачественному перерождению (раки, лейкозы).
АФК может повреждать мембраны митохондрий. Так, на первый взгляд не очень опасная молекула пероксида водорода может генерировать гидроксил-радикал в присутствии двухвалентного железа или превращаться в гипохлорит-анион ОСl– ферментом миелопероксидазой. Как гипохлорит-анион, так и гидроксил-радикал являются сильными окислителями. Они способны модифицировать белки, нуклеиновые кислоты, индуцировать перекисное окисление липидов (от которого наиболее сильно «страдают» полиненасыщенные жирными кислотами, входящими в состав мембранных липидов). Так, при перекисном окисление липидов кислородный радикал, чаще всего это бывает гидроксил-радикал, который хорошо проникает в мембраны, будучи незаряженным, отнимает атом водорода от молекулы жирной кислоты с образованием перекисного радикала жирной кислоты. Этот радикал запускает цепную реакцию, взаимодействуя с другой жирной кислотой, в ходе которой образуются перекись кислоты и новый радикал:
LH + HO . → L . + H2 O
L . + O2 → LOO .
LOO . + L′ H → LOOH + L′ . , и так далее.
Таким образом, затрагивается значительное количество клеточных липидов, и повреждаются мембраны. Кроме того, может происходить и амплификация окислительного повреждения за счет распада гидроперекисей на два новых радикала, каждый из которых запускает свою цепь.
Процессы, протекающие до момента образования гипохлорит-аниона или гидроксил-радикала, локализованы в цитоплазме и контролируются цитоплазматическими ферментами или природными водорастворимыми антиоксидантами. Например, таурин способен связывать гипохлорит-анион в форме хлораминового комплекса, дипептид карнозин и его производные нейтрализуют гидроксил-радикал, а такие соединения, как белое ферритин, связывают железо. Большое значение для предотвращения перекисного окисления липидов, инициируемое в гидрофобном пространстве клеточных мембран, и уничтожения радикалов жирных кислот имеет гидрофобный локализованный в мембранах α-токоферол (витамин Е). Его высокая концентрация в биологических мембранах препятствует их повреждению свободными радикалами. Витамин Е обрывает цепные реакции образования липидных пероксилов, превращаясь в радикал, который регенерирует как с помощью активных водорастворимых восстановителей типа аскорбата и глутатиона, так и с помощью гидрофобного убихинола (см. ниже).
АФК бывают трех типов (Ю.А. Владимиров):
- Первичные (индуцирующие) - образуются при окислении некоторых молекул; к ним относятся оксид азота NO и супероксид О2 -; обладают регуляторным или умеренным антимикробным действием.
- Вторичные - образуются вследствие атаки супероксида других молекул ;к ним относятся гидроксильный радикал ОН*, липоксильный радикал LO* и пероксинитрит; обладают сильным токсическим действием вследствие своей способности необратимо повреждать мембранные липиды, а также молекулы ДНК, углеводов и белков
- Третичные - образуются вследствие соединения вторичных радикалов с молекулами антиоксидантов и других легко окисляющихся соединений; их роль может быть различной
В рамках общей концепции окислительного стресса большое значение имеет феномен АФК-индуцированного образования АФК [52]. При этом небольшие количества индуцирующих АФК приводят к падению трансмембранного потенциала и активная генерация вторичных АФК, что приводит к развитию «окислительного взрыва». Предположительно в ходе АФК-индуцированного образования АФК происходит окисление неких белков и регуляторных тиолов, которые изменяют редокс-статус клетки, инициируя неспецифическую проницаемость мембран. Хоть неспецифическую проницаемость и носит обратимый характер, но все же приводит к нарушению функционирования электрон-транспортной цепи, изменению свойств мембран и, в конечном счете, к “окислительному взрыву”.
При повреждении комплекса I дыхательной цепи происходит прямое окисление белков, разрушение железосерных кластеров, нитрозилирование и глутатионилирование, вследствие чего сильно снижается его активность, что происходит, например, при ишемической болезни сердца (и, как следствия, реперфузии).
При повреждении белков наиболее уязвимыми являются следующие аминокислоты: цистеин, метионин, тирозин, триптофан, фенилаланин, валин, лейцин, гистидин, глутамил, пролин, треонон, аргинин, лизин (табл. 3).
Таблица 3: Модификации аминокислот.
| аминокислота |
Модифицированный продукт |
| Цистеин |
Cys-Cys, HNE-Cys |
| Метионин |
Метионин сульфоксид |
| Тирозин |
дитирозин, нитротирозин, хлоротирозин, dopa |
| Триптофан |
Гидрокси- и нитро-триптофан, кинуренин |
| Фенилаланин |
гидроксифенилаланин |
| Валин, лейцин |
Гидро(перо)ксиды |
| Гистидин |
2-оксогистидин, аспарагин, аспартат, HNE-His |
| Глутамил |
щавеливая кислота, пировиноградная кислота |
| Пролин |
гидроксипролин, пирролидон, глутаминовый семиальдегид |
| Треонин |
2-Amino-3-ketobutyric acid |
| Аргинин |
глутаминовый семиальдегид, хлорамин |
| Лизин |
α-Aminoadipic семиальдегид, хлорамины, MDA-Lys, HNE-Lys, акролеин-Lys, карбоксиметиллизин, pHA-Lys |
АФК разрушают белки, разделяя их на меньшии пептиды (рис.30). Это происходит следующим образом.
Гидроксил радикал отнимает притон от -CH(R)- группы белка, образую воду (реакции a и b). Образовавшийся алкил радикал может либо связаться со вторым алкил радикалом (реакция р), либо прореагировать с кислородом, образовав алкил пероксид радикал (реакция с). Далее алкил пероксид радикал, присоединяя протон, образует алкил пероксид. Протон он получает реагируя либо с Fe2+ (реакция g), либо с пероксильным радикалом (НО2 *) (реакция f). Алкил пероксид белка может реагировать с таким же пероксидом (дисмутация), высвобождая кислоров и образуя алкокси белок (реакция о). Алкокси белок может также образовываться путем восстановления алкил пероксида либо Fe2+ (реакция g), либо пероксильным радикалом (НО2 *) (реакция f).
Рисунок 30: Окисление белков по α-амидному и диамидному путям.
Дальнейшее преобразование алкокси белока может пойти двумя альтернативными путями:
- α-амидный путь: алкокси белок может преобразовываться в гиброксильную производную (реакция i, j), пептидня связь которой подвергается в дальнейшем расщеплению (реакция k, l),
- диамидный путь (реакция m).
В итоге исходный белок разделяется на более мелкие пептиды, что приводит к его дисфункции.
АФК значительно влияют на концентрации ионов кальция в матриксе и цитоплазме, провоцируя закачку Са2+ в цитоплазму из внеклеточного пространства и внутриклеточных депо, а в матрикс из цитоплазмы, путем активации кальциевых транспортеров [51].
Еще одно уязвимое место дыхательной цепи - Q-цикл. В двух Q-связывающих сайтах комплекса III происходит генерация убисемихинон анион радикала. Убисемихинон, образовавшийся в Qp сайте, способен реагировать с молекулярным кислородом с образованием убихинона и супероксида:
UQ.– + O2 → UQ + O2 .– .
В сайте QN активное взаимодействие радикала с кислородом не наблюдается из-за хорошей стабилизации радикала и его глубокого относительно толщи мембраны расположения, так, что кислороду трудновато до него добраться.
При связывании антимицина А с сайтом QN окисление убисемихинона в сайте Qp предотвращается, увеличивается его время существования, что повышает вероятность формирования O2 .– . Супероксид инициирует цепной процесс автоокисления коэнзима, легко окисляя его с образованием новых молекул убисемихинона. Таким образом, одним из главных источников активных форм кислорода в митохондриях является Q-цикл.
Замечательное свойство убисемихинон состоит в том, что образующийся молекулы убисемихинон легко включается в Q-цикл, при этом легко и быстро регенерируя убихинол в ходе постоянно идущего естественного процесса транспорта электронов в дыхательной цепи. Убихинол, свою очередь, проявляет ярко выраженные свойства антиоксиданта, предотвращая перекисное окисление мембранных липидов (см. выше) [35]. Убихинол достаточно эффективно обрывает цепной процесс образования перекос-ных радикалов, превращаясь в убисемихинон, который затем может реагировать с новы-ми липидными радикалами, а также диспропорционировать с образованием UQ и UQH2 :
UQH2 + L . / LOO . → UQH . + LH / LOOH
UQH . + L . / LOO . → UQ + LH / LOOH
UQH . + UQH . → UQ + UQH2
В любом случае, образующиеся формы CoQ способны включаться в Q-цикл, и тем самым антиоксидант убихинол постоянно регенерируется.
Кроме явного проявления антиоксидантных свойств путем непосредственного взаимодействия с АФК, убихинол принимает еще и опосредованное, неявное участие в борьбе с клеточными вредителями. Убихинол восстанавливает другой важнейший жирорастворимый антиоксидант – витамина Е: убихинол взаимодействует с α-токофероксил радикалом с образованием убисемихинон радикала, который регенерируется за счет взаимодействия с другими радикалами или включения в Q-цикл дыхательной цепи (рис. 31).
Замечательно то, что антиоксидант убихинол, принимая на себя удар, может регенерироваться, вступая своей окисленной формой в Q-цикл, быстро восстанавливаясь в ходе постоянно идущего естественного процесса транспорта электронов в дыхательной цепи.
В ряде работ также показано участие UQH2 в предотвращении окисления мембранных белков и ДНК [37]. Митохондриальная ДНК является еще одной мишенью для АФК. Высокая концентрация активных форм кислорода в митохондриях и слабая система репарации увеличивают частоту мутаций мтДНК по сравнению с ядерной на порядок. Радикалы кислорода служат причиной специфических замен Ц®Т (дезаминирование цитозина) и Г®Т (окислительное повреждение гуанина), вследствие чего, возможно, мтДНК богаты АТ-парами. Повреждение мтДНК особенно опасно в связи с постепенным накоплением мутаций, длительным эффектом АФК. В митохондриальном геноме закодирован ряд важнейших уникальных митохондриальных белков и повреждение ответственных за них генов приводит к нарушениям в их экспрессии и последующем функционировании. Прослеживается четкая корреляция между возрастом и накоплением мутаций в мтДНК, падением эффективности дыхания и увеличением продукции АФК, что легло в основу митохондриальной теории старения [53].
Рисунок 31: Про-оксидативные и антиоксидантные свойства кофермента Q [37].
Аналоги убихинона.
Таким образом, коэнзим Q является антиоксидантом клетки. Многие заболевания и общее старение организма связано с тем, что митохондрии не справляются с детоксикацией АФК. Поэтому изучение и возможное терапевтическое применение антиоксидантов (в частности, CoQ и его аналогов) представляет очень большой интерес. Можно попытаться распознать функцию CoQ, изменяя содержание CoQ внутри митохондрий, но для повышения концентрации CoQ в митохондрии необходимо адресовано ввести кофермент в изолированные митохондрии, клетки или же организмы. Вследствие гидрофобности и соответственно низкой растворимости в водной среде возникает проблема доставки CoQ и, следовательно, и его изучения in vitro.
Для повышения концентрации аналогов хинонов, животным в течение нескольких недель дают пищу обогащенную хинонами, так что во всех тканях устанавливается стабильная необходимая для исследований концентрация. Эти соединения могут с помощью кровотока равномерно распределяться в тканях; так их активные формы были обнаружены в наиболее подверженных окислительному стрессу тканях, то есть в мозге, печени, сердце и мышцах животных. При этом концентрация аналогов хинонов в митохондриях в несколько сот раз выше, чем в кровотоке. Аналоги хинонов при необходимости легко выводятся из тканей, возвращаясь опять в кровь и достаточно быстро экскрегируются из организма при отмене диеты.
Гидрофобность коэнзима определяется в первую очередь его боковой изопреноидной цепью. Менее гидрофобные, но по-прежнему активные производные CoQ могут быть получены путем замены длинной боковой цепи на более водорастворимые «хвосты». Такие производные CoQ широко используются в качестве электронных доноров и акцепторов при изучении ферментов и для повышения содержания коэнзима в митохондриях и клетках. Биологическая активность подобных искусственно синтезированных аналогов CoQ должна в значительной степени сохраняться, так как в передаче электронов участвует бензохиноновое кольцо, а боковая цепь выполняет только функцию заякоривания молекулы в мембране.
Как правило, такие производные (рис. 32) имеют либо очень короткую боковую цепь из одной - двух изопреноидных звеньев в позиции 6 (коэнзимы Q1, Q2), либо более простую алифатическую боковую цепь без разветвлений (децилубихинон) или модифицированную гидроксилом или другой гидрофильной группой (например 10-гидроксидецил в идебеноне) [75]. В любом случае, даже подобные аналоги CoQ все еще достаточно гидрофобны, и, при попытке их введения в биологические системы, неспецифично включаются во все фосфолипидные бислои, и только маленькая часть попадает в митохондриальные мембраны.
Для адресной доставки коэнзима Q в митохондрии перспективно использование конъюгатов с так называемыми липофильными катионами, в том числе с трифенилфосфонием.
Так, аналоги кофемента Q, ковалентно связанные с катионами трифенилфосфония, образуют ряд молекул (рис.34):
- MitoQ (mitochondria-targeted ubiquinone)-производное хинона, ковалентно связанное с катионом алкилТРР; MitoQ10 -хинол, у которого в качестве боковой цепи алкильная цепь из 10 углеродов с ТРР+ на конце.
- Mito Vit Q (mitochondria-targeted derivative of α-tocoferol),
- spin traps (Mito PBN, mitochondria-targeted derivative of the spin trap phenylbutylnitrone),
- TBTP, IBTP (тиоловые зонды),
- MitoDC81 (DNA alkylating reagent).
Еще в 1969 году Скулачевым и коллегами было показано потенциал-зависимое накопление дибензиламмония в митохондриальном матриксе, что дало толчок к изучению накопления липофильных катионов энергизованными митохондриями [72]. Накопление дибензиламмония было весьма слабым и требовало наличия противоиона, в качестве которого использовался липофильный анион тетрафенилборат. В дальнейших исследованиях использовался другой катион– метилтрифенилфосфоний, который не нуждается в противоионе. Таким образом, катионы трифенилфосфония (ТРР) стали применяться в качестве зондов при изучении функций митохондрий.
Рисунок 32: производные коэнзима Q
Липофильные катионы, несмотря на положительный заряд, имеют высокую растворимость в липидах, легко проходят через мембраны бислоя без участия ионофоров и аккумулируются в митохондриях в клетки, движимые высоким потенциалом митохондриальной мембраны. Подобное свойство обусловлено гораздо меньшей по сравнению с гидрофильными катионами типа Na+ энергией активации перехода иона из водной среды в липидное окружение. Эта энергия определяется электростатической и гидрофобной составляющими.
Основной вклад в электростатическую компоненту вносит энергия Бора, которая представляет собой вклад энтальпии, необходимый для удаления гидратирующих катион молекул воды при переносе в липидную фазу из водного раствора. Энергия Бора обратно пропорциональна ионному радиусу катиона, что обусловлено пониженной гидратацией катиона при распределении заряда по большей площади поверхности, которая в этом случае имеет меньшую напряженность электрического поля, поляризующего молекулы воды. Липофильные катионы представляет собой фосфоний, окруженный тремя гидрофобными фенильными группами, за счет чего имеют большойим ионныйм радиус около 4 Ǻ. Таким образом, включение в мембранный бислой липофильных катионов типа тетрафенилфосфония с большим ионным радиусом в 4, 2 Ǻ гораздо менее энергетически невыгодно, чем поглощение маленьких катионов типа Na+ с радиусом ~1 Ǻ.
Помимо энергии Бора существует еще две электростатических составляющих, но которые вносят значительно меньший вклад. Первая обусловлена электростатическими свойствами на границе раздела фаз с различной диэлектрической проницаемостью, а вторая связана с локальным электрическим потенциалом, возникающим во внутренней части мембраны благодаря ориентации диполей карбонильных групп жирных кислот в фосфолипидах. Существование этой дипольной силы объясняет факт о значительно более быстром проникновении анионов сквозь бислой по сравнению с катионами.
В целом электростатические силы препятствует переносу катиона из водной в липидную фазу. Однако существует не менее важная компонента энергии перемещения, обусловленная гидрофобностью катиона. Она способствует включению его в бислой за счет положительного гидрофобного эффекта, который заключается в повышении энтропии, связанном с нарушением структуры воды. Гидрофобный эффект оценивается примерно в 92 Дж/моль на Ǻ2 доступной растворителю поверхности, и, к примеру, для тетрафенилфосфония выигрыш в энергии составит порядка 29 кДж/моль. Помимо этого, гидрофобный эффект возникает сразу после поглощения катиона мембраной, тогда как увеличение отталкивающих электростатических сил возникает постепенно при прохождении через мембрану. Вследствие этого в энергетическом профиле перемещения катиона сквозь бислой помимо центрального энергетического барьера имеются потенциальные «ямы» рядом с поверхностью мембран. Катионы связываются с мембраной, попадают в потенциальную «яму» у поверхности и быстро проходят сквозь гидрофобный центр к противоположной потенциальной «яме», после чего десорбируются в раствор по другую сторону барьера. Таким образом, катионы находяться в динамическом равновесии между формами, связанными с поверхностью внутренней мембраны и свободными формами в растворе, при этом в связанном состоянии находиться примерно 60% ТРМР и 85% тетрафенилфосфония (ТРР). Т.е. в перемещении липофильных катионов через фосфолипидный бислой можно выделить три стадии: адсорбцию, транслокацию и десорбцию (рис.33).
Рисунок 33: Накопление MitoQ10 в митохондрии в ответ на мембранный потенциал Δψ.
Связывание производных трифенилфосфония происходит в большей степени по мере роста гидрофобности боковой цепи из-за увеличения движущей силы энтропийной природы. К примеру, константа ассоциации с бислоем увеличивается в 10 раз при пере-ходе от ТРМР к амилТРР и в 6 раз при переходе к тетраТРР. При этом для всех производных группа ТРР ассоциируется с мембраной в одном и том же положении на гидрофобной стороне раздела липид/вода при одновременном проникании боковой цепи в мембрану, поэтому даже самые гидрофобные производные ТРР быстро проходят сквозь бислой, не задерживаясь в нем из-за липофильности алкильной цепи. Это подтверждается коэффициентами распределения производных ТРР в системе октанол/фосфатный буфер, имитирующей внешний мембранный слой, которые относительно велики: 0,35 у ТРМР и 160 у MitoQ10 . При этом коэффициент распределения в имитирующей середину бислоя с низкой диэлектрической постоянной системе циклогексан/вода для MitoQ10 незначителен.
Таким образом, в отсутствии мембранного потенциала в условиях деэнергизованных митохондрий катионы связываются с наружной стороной мембраны, затем преодолевают гидрофобный энергетический барьер липидного бислоя, сявзываются с внутренней стороной мембраны и, наконец, десорбируются в митохондриальный матрикс.
При наличии Δψ перемещение катионов через мембрану приводит к их накоплению в митохондриальном матриксе в соответствии с уравнением Нернста. При Δψ около 60 мВ концентрация катионов в матриксе увеличивается в 10 раз, а при митохондриальном Δψ в 140-180 мВ – в сотни раз (рис. 36).Мера накопления катионов в ответ на мембранный потенциал Δψ описывается уравнением Нернста, где z - это заряд на катион.
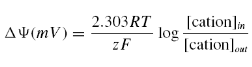
При этом уравнение Нернста оперирует концентрациями несвязанных катионов. Значительная часть проникших в митохондрии катионов ТРР связана с внутренней мембраной, что обусловлено большим объемом внутренней мембраны по сравнению с объемом матрикса. Повышение гидрофобности производного приводит к увеличению адсорбции.
Так, при 37°С до логарифмирования фактор равен 61мВ (для монокатионов), в то время как in vivo – приблизительно 120-180 мВ, а концентрация липофильных монокатионов увеличивается в 100-1000 раз внутри митохондрии (используется для измерения Δψ и обнаружения митохондрий в клетке) [76].
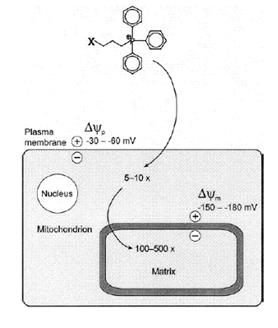
Рисунок 34: Адресная доставка в митохондрии с помощью катионов ТРР+ (by Murphy, 2004, [19]).
В свете описанных свойств катионов ТРР+, ковалентное присоединение незаряженных биологически активных соединений к катионам ТРР+ должно приводить к их адресной доставке внутрь митохондрий под действием высокого мембранного потенциала, что позволит исследовать различные вещества и использовать их в терапевтических целях. Рассмотрим некоторые производные хининов поподробнее.
Так аналоги кофемента Q, ковалентно связанные с катионами алкилтрифенилфосфо-ния, образуют молекулы MitoQ (рис.32), которые имеют различную длину боковой цепи.
Так, например, MitoQ10 – это хинол, у которого в качестве боковой цепи алкильная цепь из 10 углеродов с ТРР+ на конце (рис.32). Эксперименты в данном направлении на изолированных митохондриях и клетках показали, что MitoQ10 эффективно накапливается в митохондриях, включаясь во внутреннюю митохондриальную мембрану со стороны матрикса. Изопреноидный хвост CoQ располагается в центре бислоя параллельно поверхности, заякоривая молекулу внутри мембраны; бензохиноновое кольцо CoQ также погружено в мембрану, но способно менять свою пространственную ориентацию, тем самым, обеспечивая перенос электронов. Молекула же MitoQ ориентирована иначе: бензохиноновое кольцо локализуется в толще бислоя, изопреноидный хвост перпендикулярен поверхности мембраны, а объемный катион ТРР находится на поверхности мембраны, обращенной в матрикс (рис. 35). Для гомологов CoQ c достаточно длинной боковой цепью молекулярная динамика и минимизация энергии показали свернутую структуру молекулы: последняя изопреноидная единица находится в тесном контакте с бензохиноновым кольцом.
Рисунок 35: Ориентация CoQ и MitoQ оносительно мембранного бислоя.
Тем не менее, MitoQ10 может окисляться и восстанавливаться митохондриальной дыхательной цепью и это в основном происходит в активных центрах дыхательных комплексов, а не за счет эндогенного пула убихинонов [74]. Было показано, что MitoQ10 может принимать электроны вблизи комплексов I и II и передавать их на комплекс III, возможно, конкурируя при этом с CoQ, а также эффективно блокирует окислительные повреждения [75].
Таким образом возможно осуществлять и направленный транспорт CoQ в составе MitoQ10 , который способен выполнять функции антиоксиданта, а также блокировать многие из предполагаемых путей митохондриальной редокс-сигнализации и регуляции метаболизма, в том числе повреждение теломер, активацию UCP и пути, включающие в себя р53 [73].
Mito Vit Q – это аналог кофемента Q, являющийся производным α-токоферола (рис.32). Поскольку и CoQ и витамин Е проявляют антиоксидоньные свойства и предотвращают перекисное окисление липидов, то был синтезирован аналог убихинона Mito Vit Q. in vitro показано, что Mito Vit Q быстро и избирательно аккумулируются в изолированных митохондриях и в митохондриях изолированных клеток.
Помимо окислительных повреждений, АФК могут выполнять еще и сигнальную функцию, механизм которой пока еще малоизучен. Адресованные антиоксиданты могут так же использоваться для выслеживания сигнальных путей. Так с помощью Mito PBN (spin trap) (рис. 32) показали, что супероксид индуцирует активацию разъединения белков через образование из карбонильных радикалов фосфолипидов [73]. Mito PBN также модулирует роль продукции АФК в предполагаемых сигнальных путях внутри клетки.
Таким образом, катионы ТРР (трифенилфосфония), связанные с антиоксидантами и другими зондами, избирательно направляют их (связанные с ТРР молекулы) в митохондрии внутри клеток и in vivo. Это использует для изучения окислительного повреждения и, возможно, лечения вызываемых АФК заболеваний.
Ученые стремились улучшить количество и селективность доставки антиоксидантов в митохондрии iv vivo, заменив липофильный монокатион на дикатион (рис.30), который теоретически должен был быть значительно более эффективным. Подобное предположение возникло исходя из уравнения Нернста: на каждое повышение мембранного потенциала на 60мВ дикатионы накапливаются 100-кратном размере внутри митохондрии, (по сравнению с деситекратным увеличение для монокатионов), давая 100-1000 кратное увеличение по сравнению с монокатионами. Подобное увеличение было бы весьма значительным в усовершенствовании разрабатываемой терапии.
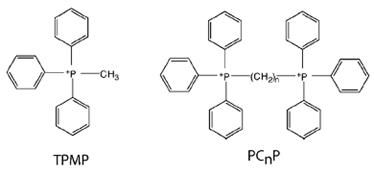
Рисунок 36: Моно- и дикатионы трифенилфосфония
Мало что известно про взаимодействие липофильных дикатионов с митохондриальной мембраной и про пределы накопления дикатионов в митохондриях. Было проведено всего несколько экспериментов по взаимодействию дикатионов с митохондриями и ни один из них не показал, что дикатионы накапливаются в соответствии с уравнение Нернста [76]. Липофильные катионы проходять сквозь мембраны за счет гидрофобности катиона и низкой энергии Бора. Энергия Бора для дикатионов в четыре раза выше чем для монокатионов, а значит дикатионы должны быть более гидрофобными, чтоб переноситься через мембраны наравне с монокатионами.
После проведения ряда экспериментов стало ясно, что дикатионы накапливаются в митохондриях при повышении мембранного потенциала примерно на 90-100мВ. Потому нецелесообразно применять дикатионы в роли векторов для доставки антиоксидантов в митохондрии. При низком мембранном потенциале (in vitro) дикотионов значительно больше нежели монокатионов, поэтому дикотионы могут использоваться для измерения мембранного потенциала.
Представляет очень большой интерес изучение как функций и механизмов действия естественных антиоксидантов клетки, так и их аналогов и дальнейшее возможное их терапевтическое применение. Окислительный стресс с накоплением в тканях и биологических жидкостях АФК и вторичных продуктов оксидативно модифицированных молекул обнаружены при многих (более 60) болезнях и патологических синдромах, нередко называемых свободно-радикальной патологией: старении тканей и всего организма, различных злокачественных процессах, хроническом воспалении (ревматоидный артрит, гастрит и язва, колиты, цистит и другие), СПИДе, сахарном диабете, атеросклерозе, последствиях инфаркта и инсульта, катаракте, нейродегенеративных заболеваниях (паркинсонизм, болезнь Альцгеймера и другие) и многих других. Вот только первично ли возникновение АФК или же накопление их является следствием патогенеза пока не совсем ясно. Несомненно, что избыточность АФК повреждает клетки и тем самым способствует развитию заболеваний, поэтому-то и необходимо изучение и создание новых неприродных антиоксидантов, которые совместно с клеточными антиоксидантами могли бы поддерживать АФК на допустимом для нормального фнкционирования клетки уровне.
[1] Chen, L.B., Summerhayes, I.C., Johnson, L.V., Walsh, M.L., Bernal, S.D., and Lampidis, T.J. (1982) Cold Spring Harbor Symp. Quant. Biol. 46, 141–155
[2] Heggeness, M.H., Simon, M., and Singer, S.J. (1978) Proc. Natl. Acad. Sci. U.S.A. 75, 3863–3866
[3]Ball, E.H. and Singer, S.J. (1982) Proc. Natl. Acad. Sci. U.S.A. 79, 123–126
[4] Johnson, L.V., Walsh, M.L., and Chen, L.B. (1980) Proc. Natl. Acad. Sci. U.S.A. 77,990–994
[5] Тихонов А. Н.// СОЖ, 1999,№ 6, с.17 - 24.
[6]Kunau W.-H., Buhue S., De La Garza M. et al. // Biochem. Soc. Trans. 1988, 16, p. 418-420.
[7] Hackenbrock, C.R., Chazotte, B., and Gupte, S.S. (1986) J. Bioenerg. and Biomembr. 18, 331–368
[8] Chazotte, B. and Hackenbrock, C.R. (1991) J. Biol. Chem. 266, 5973–5979
[9] Ferreira G. C., Pratt R. D., Pedersen R. L // J. Biol. Chem. 1989, 264, P. 15628-15633.
[10] Perkins, G., Renken, C., Martone, M.E., Young, S.J., Ellisman, M., and Frey, T. (1997) J. Struct. Biol. 119, 260–272
[11] Fawcett, D.W. (1981) in The Cell (pp. 410–485), W.B.Saunders, Philadelphia
[12] Schatz G., Dobberstein В. // Science. 1996. V. 271, Р. 1519-1526
[13] Neupert W. // Annu, Rev. Biochem. 1997. V. 66. P. 863-917
[14] Pfanner N., Craig Е.A., Malinger A. // Annu. Rev. Cell. Dev. Biol. 1997. V. 13. P. 25-51
[15] Gray, M.W. and Doolittle, W.F. (1982) Microbiol. Rev. 46, 1–42
[16] Gray, M.W. (1992) Int. Rev. Cytol. 141, 233–357
[17] Nass, S. and Nass, M.M.K. Ultramitochondrial fibers with DNA characteristics. J. Cell. Biol. 19, 593–629. 1963.
[18] Palmer, J.D. (1997) Nature 387, 454–455
[19] Lang, B.F., Burger, G., O’Kelly, C.J., Cedergren, R., Golding, G.B., Lemieux, C., Sankoff, D., Turmel, M., and Gray, M.W. (1997) Nature 387, 493–497
[20] Linnane, A.W., Lamb, A.J., Christodoulou, C., and Lukins, H.B. (1968) Proc. Natl. Acad. Sci. U.S.A. 59, 1288–1293
[21] Lamb, A.J., Clark-Walker, G.D., and Linnane, A.W. (1968) Biochim. Biophys. Acta 161, 415–427
[22] Towers, N.R., Dixon, H., Kellerman, G.M., and Linnane, A.W. (1972) Arch. Biochem. Biophys. 151, 361–369
[27] Hatefi Y. // Ann. Rev. Biochem. 1985, 55, p. 1015-1069
[28] Anderson S., De Bruijn H. L, Colison R. A. et al. // J. Mol. Biol. 1982, 156, p. 683-717
[29]Виноградов А. Д., "Биохимия", 1986, т. 51, в. 12, с. 1944-73.
[30] Festenstein G. N., Heaton F. W., Lowe J. S., Morton R. A.,// A constituent of the unsaponifable portion of animal tissue lipids. (λmax 272 mμ.), Biochem. J. 59 (1955) 558-566.
[31] Crane F. L., Hatefi Y., Lester R. L., Widmer C.,// Isolation of a quinone from beef heart mitochondria, Biochem. Biophys. Acta 25 (1957) 220-221.
[32] Wolf D. E., Hoffman C. H., Trenner N. R., Arison B. H., Shunk C. H., Linn B. O., McPherson J. F., Folkers K., //Coenzyme Q. Structure studies on the coenzyme Q group, J. Am. Chem. Soc. 80 (1958) 4750-4752
[33] Ernster L., Lee I.Y., Norling B., Persson B.,// Studies with ubiquinone-depleted submitochondrial particles. Essentiality of ubiquinone for the interaction of succinate dehydrogenase, NADH dehydrogenase, and cytochrome b, Eur. J. Biochem.9 (1969) 299-310.
[34] Mitchell P.,// Protonmotive redox mechanisms of cytochrome b-c1 complex in the respiratory chain: protonmotive ubiquinone cycle, FEBS Lett. 56 (1975) 1-6.
[35] James A. M., Smith R. A. J., Murphy M. P.,// Antioxidant and prooxidant properties of mitochondrial Coenzyme Q, Arch Biochem Biophys. 423(1) (2004 Mar 1) 47-56.
[36] Gibson F,// Chemical and genetic studies on the biosynthesis of ubiquinone by Escherichia coli, Biochem. Soc. Trans. 1 (1973) 317-326.
[37] Turunen M., Olsson J., Dallner G.,// Metabolism and function of coenzyme Q, Biochem. Biophys. Acta 1660(1-2) (2004) 171-99.
[38] Klingenberg M., Huang S. G.,// Structure and function of the uncoupling protein from brown adipose tissue, Biochem. Biophys. Acta 1415 (1999) 271-296.
[39] Fontaine E., Bernardi P.,// Progress on the mitochondrial permeability transition pore: Regulation by complex I and ubiquinone analogs, J. Bioenerg. Biomembranes 31 (1999) 335-345 [40] E. Fontaine, P. Bernardi, Progress on the mitochondrial permeability transition pore: Regulation by complex I and ubiquinone analogs, J. Bioenerg. Biomembranes 31 (1999) 335-345.
[41] D. R. Green, J. C. Reed, Mitichondria and apoptosis, Science 281 (1998) 1309-1312.
[42] L. Walter, V. Nogueira, X. Leverve, M. P. Heitz, P. Bernardi, E. Fontaine, Three classes of ubiquinone analogs regulate the mitochondrial permeability transition pore through a common site, J. Biol. Chem. 275 (2000) 29521-29527.
[43] Q. Chen, E. J. Vazquez, S. Moghaddas, C. L. Hoppel, E. J. Lesnefsky, Production of reactive oxygen species by mitochondria, J Biol Chem. 278(38) (2003 Sep 19) 36027-31.
[44] C. Fluery, B. Mignotte, J. L. Vayssiere, Mitochondrial reactive oxygen species in cell death signaling, Biochimie 84(2-3) (2002) 131-141.
[45] Литошенко А. Я.,// Эволюция митохондрий,Цитология и генетика, том 36, № 5, (2002), 49-57
[46] Минченко А.Г.,// Дударева Н.А. Митохондриальный геном, Новосибирск, (1990).
[47] Дымшиц Г.М.,// Сюрпризы митохондриального генома, Природа, №6 (2002), С.10—18
[48] Гвоздев В.А.,// Сорос. образоват. Журн, №10, (1999), С.11—17.
[49] Urso M. L., Clarkson P. M.,// Oxidative stress, exercise, and antioxidant supplementation, Toxicology 189 (2003) 41-54.
[50] Li C., Jakson R. M.,// Reactive species mechanisms of cellular hypoxia-reoxygenation injury, Am. J. Physiol. Cell Physiol. 282 (2002) C227-C241
[51] Ghosh A., Greenberg M. E.,// Calcium signaling in neurons, molecular mechanisms and cellular consequences, Science 268(5208) (1995) 239-247.
[52] Zorov D. B.,. Filburn C. R, Klotz L. O.,. Zweier J. L,. Sollot S. J,// Reactive oxygen species (ROS)-induced ROS release, a new phenomenon accompanying induction of the mitochondrial permeability transition in cardiac myocites, J. Exp. Med. 192 (2000) 1001-1014.
[53] Papa S., Skulachev V. P.,// Reactive oxygen species, mitochondria, apoptosis and aging, Molecular and Cellular Biochemistry, 174 (1997) 305-319.
[54] Виноградов А.Д., Преобразование энергии в митохондриях, // Соросовский образовательный журнал, 1999, №9, с. 11-19.
[55] Кольман Я., Рем К.Г., Рем К.-Г.,// Наглядная биохимия, Издательство:Мир, (2004).
[56] A. Bremer, U. Aebi, The structure of the F-actin filament and the actin molecule, Curr. Opin. Cell Biol. 4 (1992) 20.
[57] H. Chen, S.A. Detmer, A.J. Ewald, E.E. Griffin, S.E. Fraser, D.C. Chan, Mitofusins Mfn1 and Mfn2 coordinately regulate mitochondrial fusion and are essential for embryonic development, J. Cell Biol. 160 (2003) 189
[58] S. Cipolat, O.M. de Brito, B. Dal Zilio, L. Scorrano, OPA1 requires mitofusin 1 to promote mitochondrial fusion, Proc. Natl. Acad. Sci. U. S. A. 101 (2004) 15927.
[59] D.W. Cleveland, Microtubule MAPping, Cell 60 (1990) 701.
[60] D.W. Cleveland, K.F. Sullivan, Molecular biology and genetics of tubulin, Annu. Rev. Biochem. 54 (1985) 331.
[61] M.L. Garcia, D.W. Cleveland, Going new places using an old MAP: tau, microtubules and human neurodegenerative disease, Curr. Opin. Cell Biol. 13 (2001) 41.
[62] H. Herrmann, U. Aebi, Intermediate filaments: molecular structure, assembly mechanism, and integration into functionally distinct intracellular Scaffolds, Annu. Rev. Biochem. 73 (2004) 749.
[63] A. Kodama, T. Lechler, E. Fuchs, Coordinating cytoskeletal tracks to polarize cellular movements, J. Cell Biol. 167 (2004) 203.
[64] M.A. McNiven, Dynamin: a molecular motor with pinchase action, Cell 94 (1998) 151.
[65] M. Moritz, D.A. Agard, Gamma-tubulin complexes and microtubule nucleation, Curr. Opin. Struct. Biol. 11 (2001) 174.
[66] M. Schliwa, G. Woehlke, Molecular motors, Nature 422 (2003) 759.
[67]D.I. James, P.A. Parone, Y. Mattenberger, J.C. Martinou, hFis1, a novel component of the mammalian mitochondrial fission machinery, J. Biol. Chem. 278 (2003) 36373.
[68] L. Scorrano, Proteins that fuse and fragment mitochondria in apoptosis: con-fissing a deadly con-fusion? J. Bioenerg. Biomembr. 37 (2005) 165.
[69] J.M. Shaw, J. Nunnari, Mitochondrial dynamics and division in budding yeast, Trends Cell Biol. 12 (2002) 178.
[70] E. Smirnova, L. Griparic, D.L. Shurland, A.M. van der Bliek, Dynaminrelated protein Drp1 is required for mitochondrial division in mammalian cells, Mol. Biol. Cell 12 (2001) 2245.
[71] M.A. Welte, Bidirectional transport along microtubules, Curr. Biol. 14 (2004) R525–R537.
[72] E. A. Liberman, V. P. Topali, L. M. Tsofina, A. A. Jasaitis, V. P. Skulachev, Nature, 222 (1969) 1076-1078.
[73] M. P. Murphy, Investigating mitochondrial radical production using targeted probes, Biochem Soc Trans.32(6) (2004) 1011-4.
[74]Kelso G. F., Porteous C. M., Coulter C. V., Hughes G., Porteous W. K. , Ledgerwood E. C. , Smith R. A. , Murphy M. P., Selective targeting of a redox-active ubiquinone to mitochondria within cells: antioxidant and antiapoptotic properties, J Biol Chem. 276(7) (2001) 4588-96.
[75] R. A. Smith, G. F. Kelso, A. M. James, M. P. Murphy, Targeting coenzyme Q derivatives to mitochondria, Methods Enzymol. 382 (2004) 45-67.
[76] Meredith F. ROSS, Tatiana DA ROS†1, Frances H. BLAIKIE, Tracy A. PRIME, Carolyn M. PORTEOUS, Inna I. SEVERINA, Vladimir P. SKULACHEV, Henrik G. KJAERGAARD, Robin A. J. SMITH and Michael P. MURPHY//, Accumulation of lipophilic dications by mitochondria and cells, Biochem. J. (2006) 400, 199–208 (Printed in Great Britain)