| Скачать .docx |
Курсовая работа: Вискозиметрическое исследование комплексообразования ЭЭАКК/АК с ионом стронция
Министерство образования и науки Республики Казахстан
СЕМИПАЛАТИНСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
имени ШАКАРИМА
АГРОЭКОЛОГИЧЕСКИЙ ИНСТИТУТ
КАФЕДРА ХИМИИ И ЭКСПЕРТИЗЫ
КУРСОВАЯ РАБОТА
ВИСКОЗИМЕТРИЧЕСКОЕ ИССЛЕДОВАНИЕ КОМПЛЕКСООБРАЗОВАНИЯ ЭЭАКК/АК С ИОНОМ СТРОНЦИЯ
СТУДЕНТ С.Е. САЛЬМЕНБАЕВ
Группа 510730 Е-412
РУКОВОДИТЕЛЬ Б.А. КАЛИАСКАРОВА
Семипалатинск 2004
СОДЕРЖАНИЕ
Введение
1.Теоретическая часть
1.1 Комплексы водорастворимых полимеров с различными классами соединений
1.2 Интерполимерные комплексы водорастворимых полимеров
1.3. Комплексы полимеров с низкомолекулярными соединениями
1.3.1 Комплексы полимер – ион металла
1.3.2 Ассоциаты водорастворимых полимеров с поверхностно-активными веществами
1.3.3 Молекулярные комплексы полимеров
1.4 Свойства растворов катионных полимеров
1.5 Амфотерные полиэлектролиты
1.5.1 Гидродинамические свойства и молекулярные характеристики полиамфолитов в растворах
1.5.2 Особенности взаимодействия линейных полиамфолитов с ионами переходных металлов
2.Практическая часть
2.1 Характеристика исходных веществ
2.2 Методика исследования
3.Результаты и обсуждение
Заключение
Список использованных источников
Приложения
Введение
Комплексные соединения ионов металлов с макромолекулярными лигандами в последнее время стали объектами интенсивных исследований. Полимер-металлические комплексы, образующиеся в результате реакции между функциональными группами макромолекул и ионами металлов, можно охарактеризовать в качестве новых полимерных веществ, обладающих рядом ценных физико-химических свойств.
Повышенный интерес к таким комплексам связан с их широким применением в области гидрометаллургии, для извлечения и концентрирования ионов редких и благородных металлов, в процессе ионного обмена в почве, для создания высокоэффективных полимерных катализаторов, полупроницаемых мембран, биомедицинских препаратов и др.
Вопросы межмолекулярных взаимодействий и комплексообразования представляют собой одну из важнейших проблем химии и физики полимеров и молекулярной биологии. Кооперативные взаимодействия комплементарных структур широко реализуются в природе, а продукты ассоциации играют важную роль в живых организмах, сравнительно простых полимерных объектах. Они включают и такую важную область полимерной химии, как матричный синтез, дающий широкие возможности для получения полимеров заданной структуры.
Комплексообразование полимеров, содержащих функциональные группы, с различными классами соединений (комплементарными макромолекулами, ионами металлов, ПАВ, красителей, лекарственных веществ и т.д.) приводит к созданию полимерных ассоциирующих систем (полимерных комплексов). Эти системы интересны с точки зрения моделирования процессов, протекающих в сложных биологических системах (репликация ДНК, денатурация белков, взаимодействия протеин-липид, антиген-антитело и т.д.), проблемы совместимости полимеров, исследования структуры и свойств макромолекулярных ансамблей, самоорганизующихся полимерных систем и т.д.
В связи с развитием исследований надмолекулярных структур появились и развиваются новые области науки – супрамолекулярная химия, химия наночастиц. Особый интерес вызывают так называемые «умные полимерные системы», реагирующие на внешние раздражители (рН, температура, электрическое или магнитное поле и т.д.)
В последнее время большое внимание уделяется получению сведений о структуре и константе устойчивости комплексных соединений; о влиянии конформации и микроструктуры полилигандов, природы ионов металлов, pH-среды, ионной силы, температуры, и ряда других факторов.
1.Теоретическая часть
1.1 Комплексы водорастворимых полимеров с различными классами соединений
Исследование взаимодействий комплементарных макромолекул и продуктов этих реакций – полимерных комплексов представляет одну из важнейших проблем химии и физики полимеров и молекулярной биологии.
Комплементарными называются разнородные макромолекулы, содержащие функциональные группы, которые способны к специфическим взаимодействиям, а геометрическое строение цепей не создает препятствий для возникновения достаточно большого числа межмолекулярных связей. Это могут быть водородные связи, электростатические, ион-дипольные, ван-дер-ваальсовые и гидрофобные взаимодействия.
Интерес к данной проблеме связан с тем, что взаимодействие комплементарных структур и продукты их ассоциации играют исключительно важную роль в живых организмах (это образование двойных и тройных спиралей комплексов полинуклеотидов, надмолекулярных структур клеток вирусов, комплексов фермент-субстрат, антиген-антитело). Классическим примером кооперативного интерполимерного комплекса является двойная спираль из комплементарных цепей ДНК. Изучение подобных взаимодействий, но с участием синтетических комплементарных макромолекул делает возможным моделирование процессов, протекающих в биологических системах, на сравнительно простых полимерных объектах, т.е. позволяет осуществить подход к биологическим системам и протекающим в них процессам со стороны химии.
С другой стороны, продукты взаимодействия комплементарных макромолекул – полимерные комплексы являются, по существу, новыми полимерными материалами, хотя и получены в большинстве случаев из известных полимеров при простом смешении растворов взаимодействующих компонентов в общем растворителе. Это открывает новые пути рационального использования известных полимеров и сам процесс комлексообразования можно рассматривать как способ модификации традиционных полимеров.
По типу специфических взаимодействий, обуславливающих комплексообразование, различают комплексы, обусловленные ван-дер-ваальсовыми взаимодействиями (например, комплексы стереоизомеров полиметилметакрилата), электростатическими взаимодействиями (полиэлектролитные комплексы), комплексы с водородными связями (комплексы неионогенных полимеров с поликарбоновыми кислотами), комплексы с координационными связями (например, комплексы полимер-металл).
Существует большой класс так называемых молекулярных комплексов, которые являются продуктами невалентных взаимодействий, в основном, неионогенных полимеров – полиэтиленгликоля (ПЭГ) с резорцином, поливинилпиролидона (ПВПД) с фенолами, высокомолекулярные соединения включения полиэтиленгликоля с мочевиной, тиомочевинной, пергидротрифениленом, солям ртути, поливинилового спирта (ПВС) с йодом и боратами. К молекулярным комплексам относятся комплексы, образующиеся между гетероатомом (O, N, S, P)-содержащими полимерами и ионами щелочных и щелочно-земельных металлов. Эти комплексы стабилизированы ион-дипольными взаимодействиями. Наряду с основным взаимодействием, обуславливающим образование полимерного комплекса, не менее важную роль играют и другие взаимодействия. Например, в стабилизации полиэлектролитных комплексов с водородными связями большую роль играют гидрофобные взаимодействия.
В процессах комплексообразования полимеров могут участвовать различные классы соединений: комплементарные макромолекулы (интерполимерные комплексы), поверхностно-активные вещества (комплексы полимер-ПАВ), ионы металлов (комплексы полимер-металл), красители (комплексы полимер-краситель), лекарственные вещества, органические молекулы и т.д.
Полимерные комплексы могут быть получены несколькими способами. Наиболее распространенный из них – это смешение растворов готовых взаимодействующих компонентов в общем растворителе. В результате образуются так называемые комплексы смешения, свойства которых наиболее детально изучены в растворах.
Полимерные комплексы могут быть получены методом матричной полимеризации. При этом образуются более высокоориентированные полимерные комплексы, поскольку матрица контролирует скорость образования «дочерней цепи», её длину, химическое строение и структуру. Полимерный комплекс образуется лишь при достижении некоторой критической степени полимеризации «дочерней цепи», после чего растущая цепь ассоциируется с матрицей и начинается собственно матричная полимеризация.
В последние годы разработан новый способ получения полимерных комплексов в дополнение к традиционным (смешением растворов готовых комплементарных молекул или реакцией матричной полимеризации). Способ заключается в осуществлении реакции коплексообразования на границе раздела двух несмешивающихся жидкостей, например, бензол-вода, в которой растворены взаимодействующие компоненты. Эти несмешивающиеся жидкости являются перекрестно-селективными растворителями для исходных компонентов. Полимерные комплексы образуются в виде тонких пленок на границе раздела фаз.
Факт комплексообразования в каждой системе устанавливается совокупностью физических и физико-химических методов. Самые различные методы – потенциометрия, кондуктометрия, турбидиметрия, вискозиметрия, калориметрия, седиментация, двойное лучепреломление, светорассеяние, высокоразрешающая ЯМР-спектроскопия, хроматография, ИК- и УФ-спектроскопия, флуоресценция, электронная микроскопия, рентгеноструктурный анализ и другие могут быть использованы для исследования образования, состава и свойств полимерных комплексов.
Экспериментальные результаты могут быть представлены в виде кривых титрования или диаграмм свойство-состав. Экстремумы или точки перегиба на кривых титрования указывают на образование комплексов и их состав. Диаграммы свойство-состав бинарной смеси не подчиняются правилу аддитивности, имеют экстремальный характер и обнаруживают особые точки, что согласно основам физико-химического анализа, свидетельствует об образовании индивидуального соединения (полимерного комплекса), имеющего определенный состав. На седиментограммах поликомплексов наблюдается один пик, однозначно подтверждающий, что полимерный комплекс является индивидуальным соединением, а не смесью исходных взаимодействующих компонентов. В том случае, когда комплексообразования в системе не происходит и комплексы не образуются, кривые титрования не имеют особых точек, а зависимости свойство-состав не подчиняются правилу аддитивности.
Полимерные компоненты, участвующие в реакциях комплексообразования, могут быть гомополимерами и сополимерами (регулярными, статистичными, блочными). Они могут нести положительный заряд (поликатионы), отрицательный заряд (полианионы), оба типа зарядов (полиамфолиты), или быть неионогенными.
1.2 Интерполимерные комплексы водорастворимых полимеров
Интерполимерные (полимер-полимерные) комплексы образуются при взаимодействии химически и структурно комплементарных макромолекул. Интерполимерные комплексы (ИПК) могут быть стабилизированы системой ионных связей. Это полиионные или полдиэлектролитные комплексы (ПЭК). Комплексы поликарбоновых кислот с неионогенными водорастворимыми полимерами (полиэтиленгликоль (ПЭГ), поли-N-винилпирролидон (ПВПД), поливиниловый спирт (ПВС), полиакриламид (ПААм) и др.) стабилизированы системой водородных связей.
Анализ огромного количества данных по исследованию интерполимерных комплексов гомо- и сополимеров, стабилизированных Н-связями, позволяет сделать следующие выводы:
1. Образование ИПК обусловлено именно полимерной природой взаимодействующих компонентов. При использовании в качестве одного из компонентов низкомолекулярного аналога (например, если вместо ПМАК или ПАК использовать уксусную кислоту) или в случае, когда длина цепи меньше критической, необходимой для кооперативного связывания, образования поликомплексов не происходит.
2. Взаимодействие комлементарных макромолекул носит кооперативный характер, т.е. образование и разрушение полимерных комплексов происходит в узком интервале изменения молекулярной массы олигомера, состава сополимера, состава растворителя, рН.
3. Образование интерполимерных комплексов, как правило, отмечается в воде. Вязкость комплексов в воде порядка 0,05-0,10 дл/г, что близко к вязкости глобулярных белков. Водные растворы комплексов обнаруживают ряд присущих им особенностей: низкие значения характеристической вязкости, не зависящие от молекулярной массы матрицы; отсутствие концентрационной зависимости приведенной вязкости, коэффициентов диффузии и седиментации; отсутствие полиэлектролитной аномалии;
4. Образование интерполимерных комплексов наблюдается не только в воде, но и в ряде полярных органических растворителей (метанол, этанол, ДМФА), причем растворы поликомплексов в этих растворителях обнаруживают все свойства, присущие водным растворам поликомплексов. Растворители по их комплексообразующей способности дифференцируют на сильнокомплексующие (вода), слабокомплексующие (спирты, ДМФА) и некомплексующие (ДМСО). Компактная структура комплексов в комплексообразующих органических растворителях дополнительно стабилизирована лиофобными взаимодействиями «нерастворимых» частей реагирующих макромолекул. Стабильность комплексов, образующихся в органических растворителях, к действию различных факторов, разрушающих компактную структуру поликомплексов (второго органического растворителя – ДМСО, температуры, ионизации) меньше стабильности соответствующих комплексов, но образующихся в воде, что связано с ослаблением гидрофобных взаимодействий в этих средах.
5. Кооперативный характер образования (разрушения) интерполимерных комплексов, стабилизированных ионными или водородными связями, предопределяет наличие критических явлений в реакциях комплексообразования. Критические явления наблюдаются как в отношении свойств полимеров, участвующих в реакциях комплексообразования (состава сополимера, длины цепи, степени нейтрализации или отношения ионизированных и неионизированных групп в цепи, микроструктуры полимерной цепи), так и в отношении свойств среды (термодинамическогокачества растворителя, температуры, ионной силы, рН). Критические явления в реакциях комплексобразования обеспечивают одновременное возникновение (разрушение) достаточно большого связей между комплементарными макромолекулами.
6. Для полимерных комплексов характерны реакции макромолекулярного замещения, отбора, вытеснения, распознавания.
1.3 Комплексы полимеров с низкомолекулярными соединениями
1.3.1 Комплексы полимер – ион металла
Полимер-металлические комплексы образуются в результате взаимодействия между функциональными группами макромолекул и ионами переходным металлов (Cu2+ , Cd2+ , Zn2+ , Ni2+ , Co2+ , Mg2+ , Fe2+ и др.). Обычно связь между ионом металла и полимерным лигандом осуществляется посредством донорно-акцепторного взаимодействия с образованием координационной связи (хелатные комплексы) или замещением протона лиганда ионом металла с образованием ионной связи. Ионы металлов являются акцепторами; атомы O-, -N, -S, -F, -Cl полимерной цепи, предоставляющие пару электронов для образования связи, являются донорами. В низкомолекулярных комплексных соединениях обычно координационное число металла равно 4 или 6. В случае макромолекулярных лигандов могут образовываться координационные центры состава 1:1, 1:2, 1:3 или 1:4. Свободные вакансии координационной сферы ионов переходных металлов занимают молекулы растворителя или других низкомолекулярных веществ. Изменение конформации полимерного лиганда в процессе комплексообразования может значительно влиять на результаты расчетов координационного числа иона металла и константы устойчивости комплексов. Так, до сих пор остается открытым вопрос: имеет место ступенчатое образование комплекса полимер – металл или сразу образуется полимер-металлический комплекс с максимальным координационным числом?
Характерной особенностью комплексов полимер – металл в отличие от комплексов низкомолекулярный лиганд – металл является близость всех последовательных констант комплексообразования. Это связано с высокой локальной плотностью активных центров взаимодействия в полимерных цепях, т.е. «полимерный эффект» может играть значительную роль в образовании комплексов полимер – ион металла.
Комплексы полимер – ион металла в воде имеют компактную структуру, стабилизированную внутри- и межцепными координационными «сшивками», которые существенно изменяют размер клубка полилиганда. При добавлении к раствору поли-4-винилпиридина (П4ВП) в метаноле вязкость уменьшается, т.е. происходит сворачивание цепей П4ВП вследствие внутрицепного хелатирования. Сжатие макромолекул различно для разных ионов металла, т.е. структура полимер-металлического комплекса зависит от типа иона металла.
На устойчивость комплексов полимер – ион металла в растворе сильное влияние оказывают такие факторы как конформация и микроструктура полимерных лигандов, природа металлов, степень ионизации, природа противоионов (анионов) металлов, рН среды, ионная сила раствора, природа растворителя, температура, т.е. все те факторы, которые определяют конформационное состояние макромолекул в растворе и их гидродинамические характеристики. Многочисленные исследования систем полимер – металл посвящены установлению влияния этих факторов на свойства и структуру образующихся полимер-металлических комплексов.
Исследована радикальная полимеризация 1-винилазолов (1-винил-имидазол, 1-винилбенз-имидазол, 1-винилбензтриазол) в присутствии солей переходных металлов MgCl2 , NiCl2 , ZnCl2 . Обнаружена спонтанная полимеризация в присутствии ионов Mg2+ , и Zn2+ , в то время как координация макрорадикалов с ионами Ni2+ тормозит реакцию полимеризации.
Исследовано взаимодействие полиакриловой кислоты и сополимера акриловая кислота – малеиновая кислота состава 3:2 соответственно, с различными солями (NaCl, MgCl2 , CaCl2 , SrCl2 , ZnCl2 , Al(NO3 )3 , Fe(NO3 )3 ). Обнаружено, что сополимер, как и полимер, взаимодействует со всеми солями. ИК-спектроскопически подтверждена стабилизация заряда полианиона противоионами в результате образования пендатных связей.
Обнаружено, что некоторые типы синтетических полиамфолитов способны связывать ионы металлов при определенных значениях рН и высвобождать их в изоэлектрической точке (ИЭТ). Такое поведение полиамфолитов, возможно связано с тем, что в ИЭТ электростатическое притяжение между противоположно заряженными зарядами звеньев полиамфолита является более сильным, чем взаимодействие полимер – металл, что ведет к высвобождению связанных ионов металлов из макромолекулярного клубка.
Возможно образование тройных полимер-металлических комплексов, например, полиэтилен-имин-Cu2+ -полиакриловая кислота или поли-4-винилпиридин-Ni2+ (Co2+ )-полиакриловая кислота. Координационные и ионные связи могут участвовать в стабилизации таких комплексов. ЭПР-спектроскопически показано возможность существования нескольких типов структур тройных полимер-металлических комплексов с различным количеством функциональных групп поликислот и полиоснования в координационной сфере иона металла. Это зависит как от их относительной способности к связыванию с ионами металла, так и от координационных способностей полимер-металлических систем.
Путем стехиометрических превращений в звеньях полимерной цепи возможна настройка «первичной» структуры макромолекулы на взаимодействие с определенным ионом металла. Так, комплекс линейный полимер – ион металла сшивается сшивающим агентом, и затем металл удаляется действием минеральной кислоты. Полученный сорбент обладает высокой специфичностью и селективностью. (2)
Повышенный интерес к полимерметаллическим комплексам, с одной стороны, обусловлен тем, что некоторые ионы металлов (железо, медь кобальт, и др.) играют особо важную роль в живых организмах – участвуют в ферментативных реакциях (металлоэнзимы), мышечных сокращениях, явлениях переноса (например, гемоглобин), мембранных процессах (натрий-каливый насос) и т.д. Другая необходимость изучения комплексов полимер-металл связана с практическими задачами – извлечением редких и благородных металлов из промышленных сточных вод, созданием высокоэффективных гомогенных и гетерогенных полимерных катализаторов, термо- и механостойких полимерных материалов, полупроводников, мембран и т.д. Возрастает роль комплексных соединений полимеров в медицине. Всестороннее исследование процессов комплексообразования с целью определения состава, структуры и констант устойчивости комплексов, кинетики и механизма их формирования, анализ влияния микроструктуры, конформационного состояния макромолекул и хелатного эффекта, в конечном счете, может привести к установлению основных закономерностей комплексообразования и физико-химического поведения координационных соединений в растворах. (1)
Помимо органических полимеров должны быть рассмотрены и неорганические макромолекулы, которые обеспечивают лучшую теоретическую и химическую стойкость образующихся полимер-металлических комплексов. Должны быть также рассмотрены надмолекулярные структуры полимер-металлических комплексов, обеспечивающие некоторые свойства материалов на их основе. Взаимодействия макромолекула – ион металла (комплекс, хелат) контролируют не только высокоорганизованную структуру полимер-металлических комплексов, но и их свойства. Полагают возможным обнаружение полимер-металличесими комплексами следующих свойств и соответствующее их применение:
· Извлечение и концентрирование ионов металлов посредством образования комплексов полимер-металл
· Терапевтические эффекты – лекарства, протолекарства
· Селективность – газовый транспорт / разделение, сенсоры
· Ионная проводимость – электрон-улавливающие устройства, батареи
· Системы переменой валентности – мультиэлектронный переход, катализ, фотокатализ
· Электронные взаимодействия в твердом состоянии – проводимость, электрокатализ, электрохимия
· Фотовзаимодействия в твердом состоянии – фотопроводимость, фотогальваника, лазерография, люминесценция, оптическое хранение / переключение
· Нелинейная оптика – модуляторы, интегрированная оптика
· Керамика – квантовые устройства
Наиболее широко взаимодействия полимер – ион металла используются для извлечения и концентрирования ионов металлов. (3)
1.3.2 Ассоциаты водорастворимых полимеров с поверхностно-активными веществами
Механизм и природа взаимодействий между функциональными группами водорастворимого полимера и низкомолекулярного соединения (ПАВ, краситель, лекарственное вещество и т.д.) могут быть различными в зависимости от природы взаимодействующих компонентов: ван-дер-ваальсовые, электростатические, ион-дипольные, гидрофобные взаимодействия, водородные связи. Так, при взаимодействии полимерных кислот и оснований с катионными, анионными или неиоными ПАВ образуются компактные структуры, стабилизированные электростатическими и гидрофобными взаимодействиями, водородными связями.
Взаимодействие между полиэлектролитами и противоположно заряженными ПАВ в основном электростатическое. Это сильное взаимодействие вызывает ассоциацию при очень низких концентрациях ПАВ, известных как критическая концентрация агрегации (ККА), которая обычно ниже критической концентрации мицелообразования (ККМ) свободного ПАВ. Дальнейшее добавление ПАВ приводит к фазовому разделению. Максимальный выход осадка имеет место при отношении заряда ПЭ и ПАВ около 1:1. В зависимости от природы электролита дальнейшее добавление избытка ПАВ может вызвать растворение осадка. Следовательно структура и условия существования комплексов полимер-ПАВ, будут определятся соотношением полимер-ПАВ, что связано с образованием стехиометрического и нестехиометрического комплекса. Структура полимерного комплекса зависит от такой важной характеристики ПАВ как критическая концентрация мицелообразования (ККМ).
Осаждение систем полиэлектролит-ПАВ при очень низких концентрациях затрудняет изучение комплексообразования.
В разбавленных растворах при добавлении к полиэлектролиту противоположно заряженного ПАВ (до точки минимума вязкости) получается система, напоминающая полимерное мыло. Часть зарядов полииона нейтрализована заряженными группами ионов ПАВ, тогда как длиноцепные гидрофобные радикалы ПАВ, стремясь избежать контакта с водой, образуют неполярные ядра. Эти ядра поддерживаются в воде свободными зарядами полиэлектролита – образуется мономолекулярная мицелла. Добавление органического растворителя приводит к разрушению гидрофобного ядра мицеллы, что сопровождается разворачиванием компактных клубков поликомплекса и увеличением их размеров.
Гидрофобизация комплексов полиэлектролит-ПАВ обуславливает их компактизацию и выделение в отдельную фазу. Так, добавление ПАВ к полиэлектролиту приводит к сильному снижению приведенной вязкости системы, что свидетельствует об уменьшении размера комплексных частиц. Однако, дальнейшее увеличение содержания ПАВ может привести к гомогенизации системы и возрастанию вязкости. Это зависит от баланса между энергиями электростатического и гидрофобного взаимодействий.
На глубину комплексообразования и стабильность ассоциатов полимер-ПАВ влияют такие факторы как длина цепи полимера, гибкость, конформация, микроструктура полимерных молекул, свойства среды (концентрации компонентов, степень их ионизации, температура, рН и ионная сила среды, состав растворителя).
1.3.3 Молекулярные комплексы полимеров
Молекулярные комплексы полимеров являются продуктами нековалентных взаимодействий, в основном, между неиоными полимерами и различными низкомолекулярными соединениями. Это комплексы полиэтиленгликоля (ПЭГ) с резорцином, поли-N-винилпиролролидона (ПВПД) с фенолами; соединения включения полиэтиленгликоля с мочевиной, тиомочевинной, пергидротрифениленом, солями ртути; поливиниловый спирт (ПВПС) – йод и бораты; комплексы гетероатом (O, S, N, P)-содержащих полимеров с ионами щелочных и щелочноземельных металлов.
Интересный и практически важный тип комплексов – это соединения, образующиеся при взаимодействии полиэтиленгликоля с тиоцианатами, иодидами щелочных металлов. Эти комплексы изучены различными методами: ИКС, ЯМР, кондуктометрии и др. Структура этих комплексов представляется в виде цилиндров (спирали, включающие ионы металла), скрепляемых анионами. Однако роли анионов уделяется недостаточное внимание.
Значительный интерес представляют молекулярные комплексы образующиеся между гетероатомом (O-, N-, S-, P-) содержащими полимерами и ионами щелочных и щелочноземельных металлов. Эти системы весьма перспективны из-за возможности их использования в качестве твердых электролитов для аккумуляторов и батарей и в регистрирующих системах.
Методами электропроводности, вискозиметрии, ЯМР-, ИК- и КР-спектроскопии, рентгеновской дифрактометрии изучено комплексообразование полимерных эфиров и поливинилпиридинов с солями щелочных и щелочно-земельных металлов. Показано большое влияние на процесс комплексообразования как природы макромолекул и их длины, так и строения катиона, аниона, природы среды, предыстории приготовления образца. Установлен, что процесс комплексообразования может идти двумя путями: 1) ион-дипольным взаимодействием неподеленной пары электронов гетероатома полимерной цепи с катионами металлов; 2) образованием водородной связи между концевыми гидроксильными группами полиэфира и анионами соли. В зависимости от условий преобладает тот или иной механизм взаимодействия. (2)
1.4 Свойства растворов катионных полимеров
В последние годы вопросам синтеза и исследования физико-химических свойств катионных полиэлектролитов уделяется большое внимание. Благодаря высокому содержанию ионогенных групп поликатионы широко применяются в различных отраслях народного хозяйства, технике и медицине. Возможные области применения катионных полиэлектролитов: флокулянты, коагулянты, структурообразователи почв, анионообменики, лекарственные препараты, электропроводящие материалы, стабилизаторы эмульсий, пен, фотоматериалы, ингибиторы коррозии, полупроницаемые мембраны, адгезивы, производство бумаги, шампуни, мыла и другие косметические средства, антистатики, комплексообразователи, гомогенные и гетерогенные катализаторы.
В зависимости от расположения атомов азота вдоль полимерной цепи катионные полимеры можно разделить на два больших класса: полиоснования с атомом азота в основной цепи (интегральные) и полиоснования с атомом азота в боковой цепи (пендантные). К первому классу полимеров относятся ионены, полиэтиленимин и полиамидоамины, а второй более обширный класс поликатионов – составляют поливиниламин, поливинилпиридины, полиаминоалкилметакрилаты и другие типы катионных полимеров.
Наличие в основной или боковой цепи реакционных первичных, вторичных и третичных аминогрупп путем модификации позволяет получать сильные полиэлектролиты, полиамфолиты бетаинового типа, полимыла и др.
Поведение растворов катионных полиэлектролитов в значительной степени зависит от ионного окружения, рН среды, температуры, состава смешанного растворителя и т.д. На конформацию полиэлектролитов влияют также гидрофобные взаимодействия, которые в определенных условиях становятся преобладающим фактором, контролирующим состояние макромолекул в растворе.
1.5 Амфотерные полиэлектролиты
Высокомолекулярные соединения, содержащие в цепи функциональные группы кислотного и основного характера, называются полиамфолитами. К ним относится большинство полимеров биологического происхождения – белки и нуклеиновые кислоты. Однако в отличие от синтетических аналогов биополимеры обладают специфическим строением, функциями и свойствами, которые в полной мере проявляются лишь в живом организме. Тем не менее, ряд свойств природных полимеров удается моделировать при помощи синтетических амфотерных макромолекул.
Широко и разнообразно применение практическое применение амфотерных полиэлектролитов в различных областях народного хозяйства. Амфотерные ионообменники обладают высокой сорбционной емкостью по отношению к ионам металлов и позволяют проводить селективное разделение. Благодаря высокому содержанию функциональных групп они служат эффективными флокулянтами и коагулянтами. Полимерные амфолиты могут выступать в роли катализаторов, моделирующих функцию биокатализаторов – ферментов, носителей лекарственных препаратов – полимерных депо, микрокапсул, латексов и т.д.
1.5.1 Гидродинамические свойства и молекулярные характеристики полиамфолитов в растворах
В зависимости от изменения рН среды полиамфолиты проявляют свойства как поликислот, так и полиоснований. Значение рН, при котором средний заряд макромолекул равен нулю, соответствует изоэлектрической точке полиамфолита (ИЭТ). Классическим методом установления ИЭТ является электрофорез при разных рН с экстраполяцией к нулевому заряду.
Можно ожидать, что в области рН, значительно удаленной от ИЭТ, в макромолекуле будет появляться избыток зарядов одного знака. Это, в свою очередь, разворачивает цепные молекулы и увеличивает их размеры. При приближении к ИЭТ взаимное притяжение противоположно заряженных групп должно приводить к относительно плотному сворачиванию полиионов. Характерная особенность большинства полиамфолитов – ухудшение растворимости в воде вблизи ИЭТ.
По поведению вблизи ИЭТ полиамфолиты можно разделить на два типа: полиамфолиты, водорастворимые при любых значениях рН, и полиамфолиты, которые вблизи ИЭТ коагулируют и дают область нерастворимости. Наличие или отсутствие растворимости определяется концентрацией биполярных ионов (цвиттерионов) в ИЭТ. Если в пределе полимерная молекула представляет собой строение цвиттериона, то данный полиамфолит водорастворим во всем интервале изменения рН. Если же макромолекула в ИЭТ не заряжена (т.е. концентрация биполярных ионов очень низкая), то для таких полиамфолитов обнаруживается область нерастворимости. В свою очередь концентрация цвиттерионов зависит от константы диссоциации кислотных и основных составляющих сополимера.
Равновесие ионов водорода в растворах синтетических полиамфолитов детально не анализировалось. Причина этого заключается в том, что вблизи ИЭТ макромолекула в целом электронейтральна и имеет очень компактную конформацию. При приближении к ИЭТ труднее титровать ту или иную группу, несмотря на изменение рН среды на две единицы. Однако по мере преобладания положительного или отрицательного зарядов происходит разворачивание цепи, и дальнейшее титрование кислотных и основных групп значительно облегчается.
Для амфотерных полиэлектролитов вблизи ИЭТ возможно увеличение размеров клубка в присутствии низкомолекулярных электролитов. В кислой и щелочной областях молекулы полиамфолита веду себя как поликатионы и полианионы соответственно – вязкость полиамфолита () падает с ростом ионной силы раствора (), тогда как в ИЭТ наблюдается противоположный эффект – вязкость полиамфолита возрастает с увеличением . Такой характер изменения () с ростом ионной силы обусловлен тем, что низкомолекулярный электролит, экранируя противоположные заряды на макромолекулах, ослабляет их взаимодействие и приводит к разворачиванию клубка.
Не менее интересно влияние добавок органического растворителя на поведение водорастворимых полиамфолитов вблизи ИЭТ. Заметный рост при увеличении доли органического растворителя в бинарной смеси, вероятно связан с уменьшением диэлектрической проницаемости и улучшением качества растворителя по отношению к гидрофобной части макромолекулы.
1.5.2 Особенности взаимодействия линейных полиамфолитов с ионами переходных металлов
Среди синтетических полиэлектролитов к наиболее близким по своей структуре и поведению, биологическим полимерам следует отнести амфотерные полиэлектролиты. Однако процесс комплексообразования с участием полиамфолитов и ионов металлов изучен недостаточно. Причиной этого является, по-видимому, сложность структуры и конформационная лабильность такого класса полиэлектролитов. В отличие от гомополиэлектролитов полиамфолиты в своем составе содержат, по крайней мере, две потенциально комплексообразующие группы. Причем доля их участия в образовании комплексов будет определяться структурой и составом сополимеров, степенью ионизации составляющих звеньев, а также конформационным состоянием амфотерных макромолекул, зависящим от рН среды, ионной силы раствора, температуры и т.д. (1)
2.Практическая часть
2.1 Характеристика исходных веществ
Полимер этиловый эфир аминокротоновой кислоты / акриловая кислота (ЭЭАКК/АК)
CH3
(-C-CH-)n -(CH2 -CH-)n
NH2 COOC2 H5 COOH
Нитрат стронция – Sr(NO3 )2 марки ч.д.а., использовался без дополнительной очистки.
Хлорид калия – KCl марки ч.д.а., использовался без дополнительной очистки.
Оборудование: весы технохимические, весы аналитические, шкаф сушильный, вискозиметр, термостат, секундомер.
2.2 Методика исследования
Вязкость водных и водно-солевых растворов измеряем в капиллярных вискозиметрах Убеллоде, в термостатируемой камере при температуре 25![]() 0,1 о
С и вычисляем по формуле:
0,1 о
С и вычисляем по формуле:
h пр = h уд /С
где h = (t - t 0 )/t 0
t 0 - время истечения чистого растворителя, t - времяистечения раствора, – концентрация полимера (г/дл);
5мл раствора наливают в ячейку вискозиметра и помещают в термостат, где поддерживается постоянная температура. Вискозиметр представляет собой капиллярную трубу, соединенную с измерительным шариком.
Вискозиметр погружен в термостат. Раствор засасывается грушей из резервуара вискозиметра в шарике, выше верхней метки над измерительным шариком. Измеряется время истечения жидкости между метками.
3.Результаты и обсуждение
Цель работы:
1. Исследование комплексообразования ЭЭАКК/АК с ионом стронция вискозиметрическим методом анализа.
2. Изучение влияния различных факторов (температуры, ионной силы, pH) на поведение сополимера ЭЭАКК/АК и комплекса ЭЭАКК/АК-Sr2+ .
Метод вискозиметрии является одним из специфических методов исследования полимеров и комплексов полимер – металл. Он позволяет изучить гидродинамические и термодинамические свойства самого полимера и в присутствии ионов металла. Увеличение вязкости говорит о раскручивании, а напротив уменьшение – о скручивании полимерного клубка.
С целью изучения возможности комплексообразования в системе ЭЭАКК/АК-Sr2+ было исследовано поведение свободной макромолекулы, а также в присутствии ионов стронция. На рис.1 представлена кривая зависимости приведенной вязкости водного раствора сополимера ЭЭАКК/АК в отсутствии ионов металла, от разбавления. Как видно из рисунка с разбавлением наблюдается рост приведенной вязкости. Увеличение приведенной вязкости раствора с разбавлением обусловлено усилением электростатического взаимодействия между разноименно заряженными звеньями макромолекулы, известного под названием полиэлектролитного эффекта.
На рис.2 представлена кривая приведенной вязкости сополимера ЭЭАКК/АК в присутствии ионов стронция. Из рисунка видно, что начальные значения вязкости чистого полимера имеют высокие значения. При добавлении незначительных количеств (0,5мл) соли стронция происходит резкое падение вязкости. Понижение приведенной вязкости вызывается связыванием ионов металла с полиэлектролитом, что в свою очередь уменьшает размеры цепи. Падение вязкости объясняется образованием компактных структур стабилизированных внутрицепными, межцепными «сшивками» существенно изменяющими гидродинамические размеры макромолекулы, где роль сшивающего агента играют ионы металла.
На рис.3 представлено влияние ионной силы на вязкость сополимера ЭЭАКК/АК и комплекса ЭЭАКК/АК-Sr2+ . Ионная сила создавалась использованием растворов KCl различной нормальности. При создании ионной силы при всех значениях 0,1; 0,3; 0,5; 0,7; 0,9; полиэлектролитный эффект подавляется поэтому мы имеем значения характерной вязкости (кривая 1). При (1н. раствор KCl) полимер перестает растворяться, выпадая из раствора в осадок в виде белых хлопьев. Кривая (2) отображает поведение полимер-металлического комплекса от ионной силы. При малых значениях вязкость раствора значительно снижена по сравнению с вязкостью сополимера при таком же значении . При дальнейшем увеличении ионной силы вязкость комплекса падает незначительно и не превышает вязкости самого сополимера. Вероятно, ионная сила способствует стабилизации комплекса.
На рис. 4 приведена температурная зависимость вязкости сополимера ЭЭАКК/АК и комплекса ЭЭАКК/АК-Sr2+ . Как видно из рисунка при повышении температуры вязкость раствора ЭЭАКК/АК возрастает, что обусловлено ослаблением гидрофобного взаимодействия. (Кривая 1) Следствием этого является разворачивание молекулы сополимера. Кривая (2) показывает влияние температуры на вязкость комплекса ЭЭАКК/АК-Sr2+ . С ростом температуры наблюдается незначительное увеличение вязкости. При 80 0 С вязкость исследовать не удалось вследствие выпадения комплекса в осадок. По сравнению с вязкостью сополимера вязкость комплекса имеет низкие значения, что свидетельствует об устойчивости полимер-металлического комплекса к воздействию температуры.
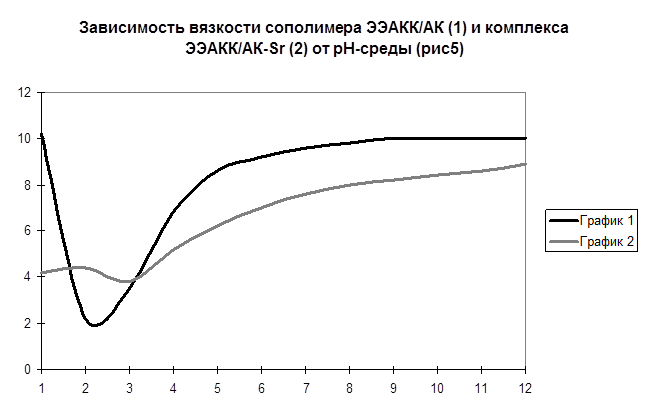
На рис. 5 показано влияние pH-среды на вязкость сополимера ЭЭАКК/АК и комплекса ЭЭАКК/АК-Sr2+ . Так как ЭЭАКК/АК является полиамфолитом, то в зависимости от pH-среды он может вести себя как поликатион или полианион. Значение pH раствора полиамфолита, при котором средний суммарный заряд на цепи равен нулю, называется изоэлектрической точкой (ИЭТ). Как известно вязкость полиамфолита в ИЭТ минимальна. Так как вязкость сополимера минимальна в области, pH 2-2,5 то предположительно ИЭТ находится в этой области (рис. 1). Кривая (2) показывает, что в присутствии ионов стронция область ИЭТ выражена незначительно и смещена в сторону pH 3,0. Вязкость комплекса в этой области превышает вязкость самого сополимера. При дальнейшем увеличении pH вязкость комплекса падает, что вероятно связано со связыванием ионов металла полиамфолитом при определенных значениях pH и частичным высвобождением их в области ИЭТ из-за сильного электростатического притяжения между противоположно заряженными участками цепи.
Заключение
1. Методом вискозиметрии исследовано комплексообразование в системе ЭЭАКК/АК-Sr2+ .
2. Исследована стабильность комплекса ЭЭАКК/АК-Sr2+ к действию различных факторов (температуры, pH-среды, ионной силы).
Список использованных источников
1) Е.А. Бектуров, С. Кудайбергенов, Р.Э. Хамзамулина «Катионные полимеры». Издательство «Наука» Алматы, 1986 – 160 с.
2) Бектуров Е.А., Бимендина Л.А., Мамытбеков Г.К. «Комплексы водорастворимых полимеров и гидрогелей». НИЦ «Ғылым» Алматы, 2002 – 202 с.
3) Бимендина Л.А., Яшкарова М.Г., Кудайбергенов С.Е., Бектуров Е.А. «Полимерные комплексы» (получение, свойства, применение): монография/под редакцией Жубанова Б.А. – Семипалатинский государственный университет имени Шакарима. – Семипалатинск, 2003. – 285с.
4) Гавриленко А.Г., Турсунова К.С., Тарасенко С.В. «Оформление курсовых и дипломных работ естественно-научных специальностей 0100: Методическое пособие для студентов факультета естественных наук» - Семипалатинск, Государственный университет им. Шакарима. 2000-50 с.
Приложение А (обязательное)


Приложение Б (обязательное)


Приложение В (обязательное)