| Скачать .docx |
Реферат: Классификации катализаторов
Классификации катализаторов
Существуют различные типы классификации катализаторов, в основе которых лежит определенная совокупность свойств или характеристик. Наиболее широко используется классификация по типу веществ, которые являются катализаторами. Она включает следующие группы катализаторов:
1. Металлы (массивные, чистые, сплавы, скелетные, нанесенные) – гетерогенные катализаторы.
Так, например, металлы VIII группы (Fe, Ni, Co, Pt, Pd) используются в качестве катализаторов гидрирования ненасыщенных соединений (главным образом алкенов и алкинов). Серебро является катализатором окисления и окислительного дегидрирования (напр., синтез формальдегида из метанола).
Металлические катализаторы могут быть компактными, скелетными, нанесенными.
Pt-сетка (компактный металл в виде переплетенных нитей) – Кт окисления диоксида серы в триоксид (получение серной кислоты). Или известный катализатор гидрирования – Никель Ренея (это скелетный катализатор, который получается при выщелачивании сплава никель-алюминий).
Нанесенные катализаторы – палладий на угле (Pd/C), палладий на оксиде алюминия (Pd/Al2 O3 ) и т.д.
2. Твердые бинарные соединения металлов Мm Эn , где Э – О, S, Se, Te, As, P, C, N, Si, B, гетерогенные катализаторы. Из этой группы чаще всего используются оксиды или халькогениды металлов полупроводникового типа. Примерами служат оксиды MgO, ZnO, Fe2 O3 , Cr2 O3 , WO3 , MoO3 , V2 O5 и др.
Так, в синтезе серной кислоты в настоящее время используется V 2 O 5 .
Катализаторы этого типа широко применяются в процессах гидрирования. Например в синтезе метанола из СО и водорода по реакции:
CO + H 2 → CH 3 OH
катализатором служит смесь оксидов:
Cr2 O3 +ZnO (IKt, суммарное давление газов 250-300 атм, температура 300-4000 С ), Cr2 O3 +ZnO+CuO (IIKt, условия более мягкие: суммарное давление 50-100 атм., температура 220-2700 С, однако, в отличие от предыдущего, катализатор чрезвычайно чувствителен к наличию серосодержащих примесей в исходных газах).
Смесь оксидов молибдена, висмута и фосфора состава MoO3 ∙Bi2 O3 ∙P2 O5 – катализатор окислительного аммонолиза пропилена в акрилонитрил:
CH2 =CH-CH3 + NH3 + 1.5 O2 → CH2 =CH-CN + 3H2 O
Сульфиды молибдена и вольфрама состава Mox Sy +Wx Sy являются хорошими катализаторами в процессах гидроочистки (обессеривания) нефтяных фракций –– в присутствии этих катализаторов происходит восстановление серосодержащих органических соединений до элементарной серы или сероводорода.
3. Кислоты и основания (гомогенные и гетерогенные катализаторы) – протонные кислоты Бренстеда (НА) в водных и неводных средах, апротонные кислоты Льюиса – Усановича (BF3 , RI), протонные и апротонные центры твердых оксидов (оксиды алюминия, алюмосиликаты), любые типы оснований (в том числе твердые – МgO, CaCO3 , ионообменные смолы).
На таких катализаторах протекают реакции кислотно-основного катализа, а именно крекинг нефтяных фракций (на алюмосиликатах и цеолитах), дегидратация и гидратация, синтез аминов из спиртов (на Al2 O3 ), этерификация спиртов и кислот, конденсация альдегидов и кетонов.
3. Комплексы металлов, включая соли (гомогенные и гетерогенные катализаторы). Следует отметить, что соли переходных металлов – это, как правило, комплексные соединения.
Рассмотрим, например, Вакер-процесс (окисление этилена в ацетальдегид), который протекает в присутствии катализатора PdCl2 /CuCl2 . На самом деле PdCl2 является линейным полимером, в котором атомы металла связаны хлоридными мостиками:
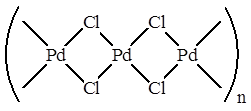
В растворе к присутствии хлорид-ионов, он деполимеризуется с образованием плоско-квадратных анионных комплексов палладия

и именно эти анионные комплексы являются составной частью катализатора и участвуют в каталитическом цикле.
В гидрировании алкинов и алкенов катализатором служат фосфиновые комплексы родия состава RhCl(PPh3 )3.
В процессе карбонилирования метанола в уксусную кислоту (процесс фирмы Монсанто) в качестве предшественника катализатора используют смесь карбонильных комплексов Rh(I) и иодистого метила (MeI).
Катализаторы реакции Реппе (карбонилирование алкинов в присутствии воды (гидрокарбоксилирование), спиртов или аминов) является тетракарбонил никеля состава Ni(CO)4 – довольно лабильный комплекс, имеющий тетраэдрическое строение.
4. Ферменты (гомогенные и гетерогенные).
Ферменты (энзимы) – биологические катализаторы обладают уникальными свойствами: высокой производительностью в расчете на один реакционный центр и селективностью, связанной со специфичностью действия. Работают ферменты в очень мягких условиях, при атмосферном давлении и температуре до 40о . В биологических системах отсутствуют неводные растворители и сильные кислоты и основания ( рН ≈ 7 ). Например фермент уреаза гидролизует только молекулы мочевины, не обращая внимания на другие амиды, и делает это гораздо эффективнее обычных кислотных катализаторов (табл. ).
Таблица
| Реакция и субстрат | Катализатор | Константа ско-рости второго по-рядка, моль-1 ∙с-1 | Температура, о С |
Гидролиз сложных эфиров Этилбензоат Этиловый эфир N-бензоил-L-тирозина |
Н3 О+ Химотрипсин |
9,0∙10-5 1,9∙104 |
54 25 |
| Гидролиз аденозин-трифосфата (АТФ ) | Н3 О+ Миозин |
4,7∙10-6 8,2∙106 |
40 25 |
Гидролиз амидов Бензамид Амид N-бензоил- L-тирозина Мочевина |
Н3 О+ Химотрипсин Н3 О+ Уреаза |
2,4∙10-6 14,9 7,4∙10-6 5,0∙106 |
52 25 62 21 |
II . Классификация катализаторов по степени дискретности и коллективности действия
Взаимодействие катализатора с реагентами в газовой и жидкой фазе носит в основном дискретный характер (взаимодействие с одним реакционным центром катализатора) (гомогенный катализ). Взаимодействие реагентов с активными центрами на поверхности гетерогенного катализатора подвергается влиянию специфических эффектов твердого тела (большое количество ядер и электронов). Здесь главную роль играют коллективные эффекты. Поэтому катализаторы можно классифицировать по степени дискретности.
Коллективные эффекты выражены сильно в: а) массивных металлах, б) твердых растворах (сплавах).
Коллективные эффекты выражены слабее в: а) полупроводниковых оксидах, б) солях металлов в кристаллическом состоянии (HgCl2 , MoS2 , PdCl2 , CuCl).
Дискретные свойства выражены сильно в: а) кислотных катализаторах в растворах, б) комплексах металлов в растворах, в) комплексах металлов, химически связанных с поверхностью носителя.
Фактически в ряду металлы → оксиды металлов → кислотные катализаторы и комплексные соединения происходит уменьшение влияния коллективных эффектов и увеличение влияния дискретных свойств. Такое деление не полностью совпадает с делением на гомогенные и гетерогенные катализаторы.
III . Классификация по специфике электронного строения
1. d–Катализаторы – катализаторы на основе переходных металлов, имеющие d–электроны и энергетически выгодные d–орбитали.
2. s,p-Катализаторы – катализаторы, в активном центре которых находится элемент, имеющий валентные S и P – орбитали(электроны). Это протонные и апротонные кислоты (НХ, RX, R+ , BF3 , оксиды алюминия, алюмосиликаты), а также основания Бренстеда (O, N, S, P, Hal – содержащие ионы и молекулы.
Металлы побочных подгрупп I и II групп Периодической системы относятся к промежуточному типу.
Группа d–катализаторов обладает несомненно более широким спектром каталитического действия из-за большего числа энергетически доступных орбиталей:
(n-1) d, ns, np и электронов, участвующих в элементарных стадиях каталитических процессов.
Из группы d-катализаторов особенно широким спектром каталитических свойств обладают металлокомплексные катализаторы (как в растворах, так и на поверхности). Именно исследование металлокомплексных катализаторов позволило установить механизм многих каталитических процессов на “молекулярном уровне”.
Особенно следует отметить, что появление металлокластерных катализаторов позволило "перебросить мостик" между металлокомплексными катализаторами в растворе и гетерогенными катализаторами на носителе.
Фактически кластерные катализаторы сочетают в себе
- с одной стороны – свойства дискретной молекулы, дополненные взаимодействием между металлами на молекулярном уровне,
- с другой стороны – свойства ансамбля из атомов металла, ограниченные рамками одной молекулы.
Представления о том, как происходит превращение субстрата (или нескольких субстратов) на поверхности катализатора и является главным подходом к пониманию механизма каталитических процессов.
Но, фактически, такие превращения – это превращения, протекающие в координационной сфере атома металла и они подчиняются всем закономерностям, которые наблюдаются в координационной химии.
Поэтому, прежде чем обсуждать механизмы активации молекул катализатором (что, собственно говоря, и является “интимным” механизмом катализа), необходимо вспомнить основные понятия координационной химии