| Скачать .docx |
Реферат: Діоксини та біфеніли
КИЇВСЬКИЙ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ ІМЕНІ Т. Г.ШЕВЧЕНКА
Діоксини та біфеніли
Робота
студентки IVкурсу
кафедри аналітичної хімії
Пилипюк Наталії
КИЇВ 2007
Зм іст
1. Загальні відомості
1.1 Структура
1.2 Фізичні властивості
2. Вплив на організм
3. Поведінка у навколишньому середовищі
4. Джерела надходження
5. Токсичність
6. Методи визначення
6.1 Сучасні методи пробопідготовки
6.2. Методи аналізу
7. Методи детоксикації
8. Висновок
1. Загальні відомості
1.1 Структура
Діоксином в органічній хімії називають шестичленний цикл, в якому два атоми Карбону зв’язані двома етиленовими містками. В токсикології під терміном "діоксин" розуміють 2,3,7,8-тетрахлордибензо-п -діоксин (2,3,7,8-ТХДД), який є найбільш токсичним представником групи надзвичайно небезпечних ксенобіотиків із числа поліхлорованих поліциклічних сполук, до яких відносяться дибензо-п -діоксини (ПХДД), дибензофурани (ПХДФ) и біфенили (ПХБ).
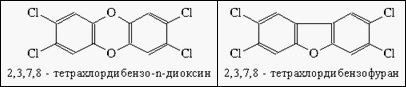
Рис. 1. Структурні формули найбільш токсичних діоксиноподібних речовин.
Дибензо-n-діоксини відносяться до гетероциклічних полі хлорованих сполук, в структурі яких присутні два ароматичних кільця, зв’язаних між собою двома кисневими містками
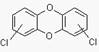
Дибензофурани містять один атом кисню
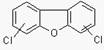
Всього відомо 210 таких сполук, з яких 75 відноситься до полі хлорованим діоксинам, а 135 – до фуранів.
1.2 Фізичні властивості
Це безбарвні кристалічні речовини, температура плавлення яких залежить від числа атомів Хлору в структурі. Вони добре розчинні в органічних розчинниках і практично не розчинні у воді (10-2 – 10-6 мг/ л), причому зі збільшенням числа атомів Хлору розчинність зменшується. Ці сполуки характеризуються високою хімічною стійкістю, навіть при високій температурі. В присутності домішок кислот під впливом сонячного випромінювання, вони порівняно легко втрачають атоми хлору і при цьому стають нетоксичними.
Крім високої ліофільності (здатності розчинятися в органічних розчинниках та утримуватись в жироподібних матрицях), діоксини характеризуються високою адгезією до частинок грунту, золи, донних відкладень, що сприяє їх накопиченню та міграції у вигляді зависей та комплексів з органічними речовинами в поверхневих водах.
2. Вплив на організм
Діоксин – надзвичайно сильна отрута (за рівнем токсичності перевищує кураре і синильну кислоту), оскільки навіть при малих концентраціях вражає практично всі форми живої матерії – від бактерій до теплокровних. Для людини мінімальна токсична доза складає 0,5-1 мкг/кг.
Табл.1. Гранично допустимі концентрації чи рівні деяких токсичних речовин в різноманітних об’єктах.
| Речовина | Вода, мг/л | Повітря, мг/м3 | Грунт, мг/кг | |
| рухома форма | загальний вміст | |||
| Діоксини (ДЕ)* | 5∙10-8 | 5∙10-10 | - | 110-8 |
| Бенз(а)пірен | 5∙10-6 | 1∙10-6 | - | 0,02 |
| Трихлорбифенили | 0,001 | - | - | 0,03 |
| Пентахлорбифенили | 0,001 | - | - | 0,1 |
| ДДТ | 0,1 | 5∙10-4 | - | 0,1 |
| Гексахлорциклогексан | 0,02 | 0,03 | - | 0,1 |
| N-нітрозодиметиламін | - | 5∙10-5 | - | - |
| 1-Нафтиламін | - | 0,003 | - | - |
| Ртуть | 5∙10-4 | 3∙10-4 | - | 2,1 |
| Кадмій | 0,001 | 3∙10-4 | 3,0 | - |
| Свинець | 0,03 | 3∙10-4 | 6,0 | 32 |
*ДЕ – діоксиновий еквівалент.
Токсичність діоксину для найпростіших організмів, очевидно, зумовлена порушенням функцій металоферментів, з якими він утворює міцні комплекси.
В організмі теплокровних діоксин спочатку потрапляє в жирові тканини, а потім перерозподіляється, накопичуючись переважно у печінці. Його розклад всередині організму незначний: діоксин виводиться в основному незмінним, у вигляді комплексів до цих пір не встановленої природи. Період напіввиведення коливається від кількох десятків днів (миші) до року і більше (примати) і за звичай зростає при повільному потраплянні до організму.
При гострому отруєнні спостерігаються ознаки загальнотоксичної дії діоксину:
- втрата апетиту;
- фізична і статева слабкість;
- хронічна втомлюваність;
- депресія;
- різка втрата ваги.
У цьому випаду летальний кінець настає за кілька днів, в залежності від дози отрути і швидкості її потрапляння до організму.
У випадку несмертельних доз діоксин викликає важкі специфічні захворювання.
У високочутливих осіб спочатку з’являється ураження шкіри – хлоракне (пошкодження сальних залоз, яке супроводжується дерматитами і утворенням виразок, що довго не загоюються), причому у людей хлоракне може виявлятися знову і знову навіть після багатьох років після одужання. Більш сильне ураження діоксином призводить до порушення обміну порфіринів – важливих складових гемоглобіну і простатичних груп залізовмісних ферментів (цитохромів).
Порфірія – так називається ця хвороба – проявляється в підвищенні фоточутливості шкіри: вона стає крихкою, вкривається численними мікро пухирцями. При хронічному отруєнні розвиваються також різноманітні хвороби, пов’язані з ураженням печінки, імунних систем і центральної нервової системи.
Діоксини потрапляють в організм людини в основному з їжею, водою і повітрям. Причому для цієї отрути не існує так званого "порогу дії": навіть одна молекула здатна спровокувати аномальну клітинну діяльність і викликати ланцюг реакцій, котрі порушують діяльність організму.
Крім того, діоксини поволі вражають на клітини, що відповідають за роботу гормональних систем. Зростає ризик захворювання діабетом, порушується статеве дозрівання; організм втрачає опір інфекціям, зростають алергічні реакції і онкологічні захворювання; виникають ендокринні і гормональні розлади, змінюється вміст статевих гормонів, гормонів щитовидної і підшлункової залози.
3. Поведінка у навколишньому середовищі
В біосфері діоксин швидко поглинається рослинами, сорбується грунтом, де практично не змінюється під впливом фізичних, хімічних і біологічних факторів середовища. Завдяки здатності до утворення комплексів, він міцно зв’язується з органічними речовинами грунту. Період напіврозпаду діоксину в природі перевищує 10 років. Таким чином, різноманітні об’єкти навколишнього середовища є надійними сховищами для цієї отрути.
Подальша поведінка діоксину визначається властивостями об’єктів, з якими він зв’язується. Його вертикальна і горизонтальна міграції у грунтах можливі лише для ряду тропічних районів, де у грунтах переважають нерозчинні у воді органічні речовини. У грунтах інших типів він міцно зв’язується у верхніх шарах (низька розчинність у воді робить неможливим проникнення вглиб) і поступово накопичується у змертвілих рештках організмів. Багаторічний моніторинг на територіях, які піддавалися сильному забрудненню пестицидами 2,4,5-Т і 2,4-Д в США і Канаді, показав, що 2,3,7,8-ТХДД неможливо виявити на глибині більше 5-20 см.
Виводяться діоксини із грунтів переважно механічним шляхом. Комплекси діоксину з органічними речовинами, які мають малу густину, а також рештки організмів видуваються вітром з поверхні грунту, вимиваються дощовими потоками і в результати потрапляють до низин, створюючи нові центри зараження (місця накопичення дощової води, озера, придонні відклади річок, каналів).
4. Джерела надходження
Промисловість
Джерелом надходження діоксинів до оточуючого середавища є підприємства майже всіх галузей, де використовують у виробництві хлор, однак хімічні, нафтохімічні і целюлозно-паперові заводи лідирують у цьому списку. Максимальні викиди діоксинів в екосферу у всьому світі спостерігався у 60-70х роках через збільшення виробництва вибіленого паперу.
Особлива роль належать і сміттєспалювальним заводам, де процеси відбувається при температурі 800-9500 С. Саме тоді утворюється максимальна кількість діоксинів. Спалюючи один кілограм полівінілхлоридів – а це лінолеум, деякі види шпалер, пластикових пляшок – ми отримуємо до 50 мкг діоксинів. Ефективна їх руйнація можлива лише при 1150-12000 С. Більше того, кожне підвищення цін на бензин теж певний час супроводжується посиленням викидів діоксинів у повітря: міські комунальні служби економлять на вивозі сміття, і двірники палять його прямо на місці, а у міському смітті повно, зокрема, пластикових пляшок.
Озброєння армії
Це джерело діоксинів пов’язане із озброєнням ще Радянської армії і прямим використанням бойового гербіциду на основі американської суміші "AgentOrange", яку використовували у В’єтнамській війні. Військовим тоді планували мати два гербіциди, які склали основу суміші (гербіциди 2.4.5-Т і 2.4-Д, відповідно, три- і дихлорфеноксиоцтові кислоти) і які планувалося використовувати для знищення рослинності "потенційного ворога". І вони отримали в середині 1960-х років таку суміш – більше 4000 тон. Причому досліджували ефективність дії цієї суміші безпосередньо на теренах Радянського Союзу.
Очевидно, що потужне джерело діоксинових забруднень – знищення хімічної зброї.
Їжа
Чим жирніші страви на столі, тим більша ймовірність, що діоксини "оселяться" у нашому організмі. Як відомо, діоксини добре розчиняються в жирах і зовсім не люблять воду. В рослинних жирах діоксинів практично немає, так як рослини не здатні засвоювати ліпофільні речовини. Допустима добова норма діоксинів для людини, котра важить 70 кг - 700пкг. З’ївши півкілограма морської риби, в якій 5% жиру, він отримає вдвічі більше.
З-під крану
Хлор, який використовують для знезараження води, сам містить діоксини. Випивши 2-3 літри води, людина вживає 60 пкг діоксинів. Тому в усьому світі розгортаються кампанії щодо заміни метода хлорування озонуванням води.
Таблица 6. Основні джерела утворення ПХДД и ПХДФ в США .
| Джерело емісії | Розмірність | Всього, г/рік | |
| 2005 | 1987 | ||
| Спалювання побутового сміття | нг/кг | 1100 | 7915 |
| Спалювання небезпечних відходів | нг/кг | 5,7 | 5,0 |
| Спалювання медичних відходів | нг/кг | 461 | 2440 |
| Крематорії | мкг/тіло | 9,1 | 5,5 |
| Спалювання стічних вод | нг/кг сухогоосаду | 14,6 | 6,0 |
| Спалювання покришок | нг/кг гуми | 0,11 | 0,11 |
Автотранспорт – етильований бензин |
пг/км пробігу |
1,7 |
31,9 |
| – неетильований бензин | пг/км пробігу | 5,6 | 3,3 |
| – дизельне паливо | пг/км пробігу | 33,5 | 26,3 |
Опалення деревиною – побутове |
нг/кг |
62,8 |
89,6 |
| -- промислове | нг/кг | 26,2 | 25,1 |
| Промислове спалювання масел | нг/л масла | 9,3 | 15,5 |
Виробництво цементу – при спалюванні небезпечних відходів |
нг/кг цементу | 145,3 | 109,6 |
| – без спалювання небезпечних відходів | нг/кг цемента | 16,6 | 12,7 |
| Регенерація катализаторів нефтепереробки | нг/баррельпродукта (159 л) | 2,11 | 2,14 |
| Ре активування вугілля | нг/кг угля | 0,08 | 0,06 |
| Куріння | пг/сигарета | 0,8 | 1,0 |
| Печі для знищення картону | нг/кг отходов | 2,3 | 2,0 |
| Природні пожежі | нг/кг биомассы | 208 | 170 |
| Чорна металургія (агломерат) | нг/кг агломерата | 25,1 | 29,3 |
| Производство дихлорметана и винилхлорида | нг/кг | 12,76 | |
| Отбеливание древесной и бумажной пульпы | 20,9 | 370,1 | |
| Осадки бытовых стоков | 76,6 | 76,6 | |
| Осад побутових стоків | 2,6 | 2,6 | |
Табл.7. Викиди діоксанів в атмосферу (г ДЕ/ рік)
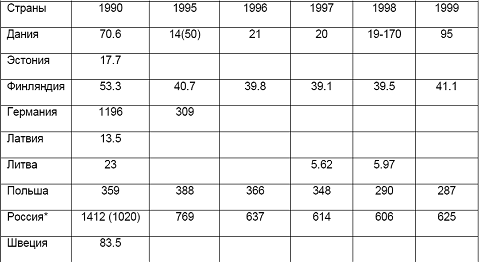
Так, можна прослідкувати основний шлях переміщення діоксинів в природі:
джерело → повітряне середовище → вода → грунт → рослини → молочна худоба → різноманітні продукти → людина → грудне молоко матері → новонароджена дитина.
Саме дитина виявляється основним "споживачем" цих суперекотоксикантів, оскільки на кожному етапі харчового ланцюга відбувається багатократне зростання концентрації отрути.
Отже, в середині 60-х років в продуктах хімічних виробництв були знайдені чужорідні для живих організмів речовини, які нині об’єднують під загальною назвою – діоксини. Це найбільш ефективна отрута, яку поки що знає людство, котра має надзвичайно високу кумулятивну токсичність, що пов’язано із наявністю в нашому організмі особливих біоакцепторів, котрі збільшують час ви ходу діоксину із організму до 10 років. Але найбільш небезпечними є діоксани для молодого організму на стадії формування. Це означає, що виробляючи діоксини ми не лише отруюємо себе, а й вбиваємо майбутнє своєї нації.
Єдиний шлях вирішення цієї проблеми – створення контролю діоксинового фону оточуючого середовища (моніторингу): виявлення джерел генерації діоксинів, організації заходів, направлених на усунення джерел (зміна технологій, очистка зараженої території).
5. Токсичність
Для токсикологічних досліджень не менш важливим є структурна різноманітність як самих визначуваних речовин, так і принципова відмінність у токсичності окремих ізомерів. Небезпеку складають лише 17 похідних поліхлорованих бибензо-п -діоксинів (ПХДД) та поліхлорованих дибензофуранів (ПХДФ), які мають заміщений галоїд в положеннях 2, 3, 7, 8. Інші, з врахуванням тих кількостей, які можуть зустрічатися в об’єктах оточуючого середовища, не являють серйозної небезпеки. Для цих 17 сполук введена система коефіцієнтів токсичності, яка дозволяє зводити до єдиного токсичного еквіваленту (діоксиновий еквівалент – ДЕ) токсичні характеристики любої реальної суміші. Тобто, токсичність любої суміші ПХДД і ПХДФ може бути виражена через токсичність 2,3,7,8-ТХДД, взятого в еквівентній за токсичністю кількості. Система коефіцієнтів токсичності для ПХДД, ПХДФ і диоксиноподібних ПХБ приведена в табл.2 і 3.
Табл.2. Коефіцієнти токсичності для ПХДД і ПХДФ відносно 2,3,7,8-ТХДД.
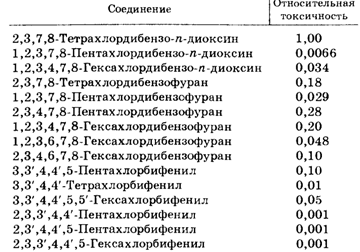
Табл.3. Коефіцієнти токсичності для діоксиноподобних ПХБ відносно 2,3,7,8-ТХДД.
| Ізомер, номер IUPAC | WHO, 1994 | WHO, 1998 для: | ||
| ссавців | риб | птахів | ||
| Не ортозаміщені ПХБ | ||||
| 3,3',4,4'-TХБ (77) | 0,0005 | 0,0001 | 0,0005 | 0,0001 |
| 3,4,4',5-TХБ (81) | 0 | 0,0001 | 0,0001 | 0,0001 |
| 3,3',4,4',5-ПеХБ (126) | 0,1 | 0,1 | 0,005 | 0,00001 |
| 3,3',4,4',5,5'-ГеХБ (169) | 0,01 | 0,01 | 0,00005 | 0,00001 |
| Моно-ортозаміщені ПХБ | ||||
| 2,3,3',4,4'-ПеХБ (105) | 0,0001 | 0,0001 | <0,000005 | 0,0001 |
| 2,3,4,4',5-ПеХБ (114) | 0,0005 | 0,0005 | <0,000005 | 0,0001 |
| 2,3',4,4',5-ПеХБ (118) | 0,0001 | 0,001 | <0,000005 | 0,00001 |
| 2',3,4,4',5-ПеХБ (123) | 0,0001 | 0,0001 | <0,000005 | 0,00001 |
| 2,3,3',4,4',5-ГеХБ (156) | 0,0005 | 0,0005 | <0,000005 | 0,0001 |
| 2,3,3',4,4',5'-ГеХБ (157) | 0,0005 | 0,0005 | <0,000005 | 0,0001 |
| 2,3',4,4',5,5'-ГеХБ (167) | 0,00001 | 0,00001 | <0,000005 | 0,00001 |
| 2,3,3',4,4',5,5'-ГпХБ (167) | 0,0001 | 0,0001 | <0,000005 | 0,00001 |
| 2,2',3,4,4',5,5'-ГпХБ (170) | 0,0001 | 0 | ||
| 2,3,3',4,4',5,5'-ГпХБ (180) | 0,00001 | 0 | ||
Т- тетра-, Пе- пента-, Гк- гекса-, Гп- гепта-, О- окта-.
6. Методи визначення
Визначення діоксинів у навколишньому середовищі і в біологічних об’єктах є однією із найважчих задач. В першу чергу це пов’язано з високою токсичністю цих сполук, що вимагає, аби межі виявлення їх в різноманітних матрицях були суттєво нижчі від характерних для багатьох задач органічного аналізу.
Вирішення цієї задачі вимагало розробки і введення до аналітичної практики методів розділення і детектування, які забезпечують визначення пікограмових кількостей діоксинів на фоні речовин, які присутні в матриці в значно більш високих концентраціях. Такі методи включають багатостадійну пробопідготовку, яка дозволяє видалити основну кількість заважаючи речовин, з наступним розділенням методом капілярної газо-рідинної хроматографії і детектуванням за допомогою мас-спектрометрів високої роздільної здатності. Незважаючи на значні досягнення в області ультраслідового аналізу, визначення діоксанів є однією із самих дорогих аналітичних задач, які виконуються серійно – вартість аналізу однієї проби перевищує 1000 доларів.
6.1 Сучасні методи пробопідготовки
Стандартні методики для визначення діоксинів, розраховані на високу відтворюваність є надто трудоємними і на практиці рідко використовуються в повному обсязі. Для того, аби задовільнити потребу на проведення екологічних досліджень, існуючі методики вдосконалюються і створюються нові методи аналізу.
Одним із таких вдосконалень стало створення автоматичної системи пробоочистки (Power-Prep, FluidManagementSystems, Inc.). ця система значно понижує вплив людського фактору на якісь результатів, а використання фабричних одноразових колонок із сорбентами практично повінстю нівелює артефакти і підвищує відтворюваність. На жаль, система на п’ять проб має вартість близько $70000, що поряд з її низькою надійністю практично повність виключає її використання на теренах СНД.
Найбільш значним вдосконаленням процедури пробопідготовки при аналізі ПХДД/ПХДФ в СНД стало використання у лабораторній практиці вугільних мікро колонок ФАС-МД російського виробництва. Це дозволило вирішити проблему відділення планарних речовин від жиру та інших компонентів матриці і позбавитися стадії упарювання толуолу.
Іншим великим досягненням аналітичної хімії стало створення метода екстракції в субкритичних умовах, тобто в інтервалі температур між температурою кипіння розчинника і критичною температурою при тиску не менше тиску рівноважної пари розчинника.
Відомо, що збільшенню ефективності рідинної екстракції з твердих матриць сприяє підвищення температури і високий градієнт концентрації, для чого на практиці використовують кип’ятіння з оберненим холодильником, екстракція кількома порціями розчинника чи екстракція в апараті Сокслета. Метод екстракції в субкритичних умовах дозволив скоротити тривалість екстракції від кількох діб до кількох хвилин.
В загальному випадку, установка для субкритичної екстракції є ВЕРХ системою, в якій колонка з нерухомою фазою замінена картриджем зі зразком, вміщеннм в термостат газового хроматографа. Тиск в системі регулюється вихідним краном, для охолодження перегрітого розчинника достатньо використовувати сталевий капіляр довжиною 50 см, вміщений у холодну воду. Постійна подача чистого розчинника створює високий градієнт концентрацій речовин, які відокремлюємо. Відносна простота обладнання (для роботи можна використовувати частини морально застарілих приладів) і висока перспективність стали причиною швидкого розвитку цього методу.
6.2 Методи аналізу
На сьогодні основними методами визначення діоксини залишаються газо-різинна хроматографія і хромато-мас-спектрометрія.

Рис.5. Загальна схема аналізу проби ПХДД/Ф
7. Методи детоксикації
Як було зазначено вище специфіка токсичності діоксинів полягає в тому, що серйозну небезпеку являють лише заміщені галогеном в положенні 2,3,7,8 похідні ПХДД/ПХДФ. Всі інші, з врахуванням концентрацій, в яких вони можуть знаходитись в оточуючому середовищі, не являють серйозної небезпеки, тобто для детоксикації достатньо видалити один із чотирьох латеральних атомів галогену.
Звичним методом знищення особливо шкідливих речовин є їх руйнація під дією високих температур (спалювання чи піроліз). Але у випадку хлорованих органічних речовин високотемпературні процеси є основними джерелами забруднення оточуючого середовища діоксинами.
Сьогодні запропоновано ряд низькотемпературних матодів деструкції. Всі вони відомі достатньо давно, але, з різних причин, поки що жоден з них не знайшов практичного використання, тому нижче наведені лише короткі описи.
Табл. 9. Нетермічні методи детоксикації ПХДД/ПХДФ
| Процес | Ступіньрозкладу, % | Вплив на оточуюче середовище |
| Фотоліз | >99,8 | Не впливає |
| Радиоліз | 97 | Радіація, утвореннямалохлорованих діоксинів |
| Гідродехлорування | >99 | Утворення токсичнихпобічних продуктів |
| Дехлорування | >99 | Не впливає |
| Каталітичне окиснення | >99 | Потребує високих температур ітиску |
| Озонування | 97 | Залишки продуктів реакції |
| Розкладйодидом хлора | 92 | Утворення хлорорганічних залишків |
Найбільш ефективним і безпечним із цих методів можна вважати фотоліз , який є основним шляхом деградації ПХДД і ПХДФ в оточуючому середовищі. Діоксини поглинають електромагнітні хвилі довжиною більше 290 нм і можуть піддаватися фотолізу. Найшвидше (кілька хвилин) фотоліз діоксинів відбувається в органічних розчинниках. В чистій воді фотоліз значно понижується. Період напіврозпаду під дією сонячного світла складає 6-8 годин. Фотолізу у водному середовищі сприяють добавки апротонних розчинників. Також фотоліз можливий у газовій фазі, на поверхні твердих часток і у воді.
Механізм фотолізу та його продукти до кінця не вивчені. Вказують на вплив матриці та агрегатного стану, що не дає можливості повного використання лабораторних результатів для опису процесів у навколишньому середовищі. Процес фотодехлорування в розчинах, в тому числі і водних, описується кінетичним рівнянням першого порядку і приводить переважно до відщеплення атома хлору з латерального положення.
Лужне дегідрування субстратів, забруднених ПХДД/ПХДФ, вважається найбільш перспективним серед хімічних методів як для рідких, так і для твердих матеріалів. Де галогенування можна здійснювати за допомогою сумішей водних розчинів солей лужних металів і поліспиртів. Реакційну суміш витримують при температурі 140-2200 С, ступінь деструкції діоксину сягає 99,95%. Висока ефективність дегазації ПХДД/ПХДФ помічена при використанні поліетиленгліколяту калію, який дозволяє провести дехлорування до утворення KCl та інших відносно нетоксичних продуктів. В залежності від температурного режиму і часу реакцій ефективність деструкції ПХДД і ПХДФ може сягати 99,9%.
Радіоліз – метод базується на розкладанні діоксинів під дією -випромінювання. Радіоліз призводить до часткового видалення атомів галогену з молекули ПХДД/ПХДФ, не руйнуючи основну "діоксинову" структуру.
Озоноліз – полягає в пропусканні озону через суспензію, яка містить ПХДД/ПХДФ. Розклад відбувається лише в лужних умовах (рН=10). Через 48 годин при кімнатній температурі відбувається руйнація 93% 2,3,7,8-ТХДД, а при 50 °С за 30 хв – 94%.
Метод хлорйодидного розкладу передбачає використання солей четвертинних амонієвих основ. Такі хлор йодиди призводять до розриву кисневих зв’язків в молекулі діоксину за м’яких умов при 200 С з утворенням хлорфенолів, фенолів і 2-феноксифенілу. Для дегазації використовують рочзин, що містить 5-10 г/л хлор йодидів четвертинних амонієвих солей. Ефективність методу – 70% за 24 години.
Гідразиновий метод заснований на взаємодії діоксинів з водними розчином гідразину, який має в структурі молекули етильну групу чи утворює її в процесі реакції. Обробка матеріалів. Забруднених діоксанами, здійснюється при 20-200°С під тиском 15 атмосфер протягом 15-480 хвилин. В якості каталізаторів використовують метали VIII групи чи випромінювання УФ. Одноразова обробка дає 90-98% ефект.
Біотичний та абіотичний розклад. Цей напрямок є порівняно новим, але напрочуд перспективним. В основному роботи проводили з 2,3,7,8-ТХДД. Залишається суперечливим питання щодо вкладу мікроорганізмів в біорозклад і видалення ТХДД з оточуючого середовища. Вважають, що відбувається або кометаболізм цієї сполуки, або його використовують в якості джерела вуглецю. Доведений мікробіологічний розклад 2,3,7,8-ТХДД чистими бактеріальними культурами з періодом напіврозкладу 1 рік. Останнім часом в серії експериментів з культурою псевдо монад Alcaligenesdenitrificansбув встановлений швидкий розклад 2-МХДФ, повільний – 2,8-ДХДФ і відсутність розкладу 1,3,7,8-ТХДФ.
Зрозуміло, що найкращим засобом боротьби з діоксиновими забрудненнями є зниження ймовірності утворення діоксанів у відповідних технологічних стадіях і видалити діоксани з продукції. Так, колективом професора Іпполітова Є.Г. при РАН були розроблені нові без хлорні дезинфікуючі суміші широкого спекру дії на основі пер оцтової кислоти та перексоду водню, нові технології безхлорного пероксидного відбілювання текстильних виробів тощо.
Висновок
Як бачимо, діоксини відносяться до когорти стійких органічних забруднювачів, а це значить, що вони дуже повільно детоксикуються у природі, тим самим збільшуючи ризик потрапляння їх до організму людини. Тому, з метою попередження, слід розробити низку заходів направлених на постійний моніторинг середовища на вміст цих сполук.
Література
1. Диоксин. Медико-экологически аспекты. Под редакцией проф.П.Е. Шкодича, Москва, 1997 г.2. Румак В.С., Поздняков С.П., Умнова Н.В. и др.Диоксины-супертоксиканты XXI века.М.:19983. Гибс Л.М. Правда о диоксинах. Иркутск, 1998 г.4. Веб-сайт екологічного проекта "Экологическая геохимия", http://ecology.icm.ac.ru/.5.Клюев Н.А. Контроль суперэкотоксикантов в окружающей среде и источники их появления // ЖАХ. - 1996. - Т.51, №2. - C.163-172.
6.Experiments on the mobility of 2,3,7,8-tetrachlorodibenzo-p -dioxin at Times Beach, Missouri / R.A. Freeman, F.D. Hileman, R.W. Noble, J.M. Schroy In: J.H. Exner ed. // Solving Hazardous Waste Problems, ACS Symposium Series Num. 338. - 1987.
7. Федоров Л.А., Мясоедов Б.Ф. Диоксины как экологическая опасность: ретроспектива и перспективы // Успехи химии. - 1990. - т.59, №11. - С. 1818-1823.діоксин пробопідготовка хроматографія детоксикація
8. Федоров Л.А. Диоксины как экологическая опасность: ретроспектива и перспектива. - М.: Наука, 1993. - 265 с.
9. Майстренко В.Н., Хамитов Р.З., Будников Г.К. Эколого-аналитический мониторинг супертоксикантов. - М.: Химия, 1996. - 319 с.
10.Антонюк В.В., Позняков С.П., Ермаков С.П. Современные подходы к интегральной оценке изменений состояния здоровья населения под воздействием неблагоприятных факторов внешней среды. М., 1998. – 324 с.
11. Медицинская экотоксикология и экологическая химия диоксинсодержащихэко-токсикантов. Книга 2, часть III / Под. ред. В.С. Румака и Н.А. Клюева. - Б.м., 1997. - 372 с.