| Скачать .docx | Скачать .pdf |
Реферат: Синтез и физико-химические свойства магний - алюминиевого сорбента со структурой гидроталькита
Синтез и физико-химические свойства магний - алюминиевого сорбента со структурой гидроталькита
Новоселецкая Оксана Вячеславовна
Автореферат диссертации на соискание учёной степени кандидата химических наук
Краснодар-2007
Работа выполнена на кафедре неорганической химии Кубанского государственного технологического университета
Общая характеристика работы
Актуальность работы:
Решение проблемы предотвращения загрязнений окружающей среды зависит от успешного решения задачи очистки промышленных сточных вод от ионов тяжелых металлов. Нередко возникает необходимость удаления из промышленных сточных вод гальванических производств гексацианоферрат- и хромат- анионов. В производстве средств молекулярной электроники, антикоррозионных добавок в химические источники тока существуют отдельные участки, связанные с переработкой ртути и ее соединений, что требует решения задачи, связанной с обезвреживанием ртутьсодержащих сбросов. Очистка производственных стоков ртути до уровня ПДК(0,005 мг) возможна только с использованием сорбционной технологии.
В связи с этим создание на основе гидроксидов металлов ионообменных материалов, позволяющих за счет высоких емкостных и кинетических характеристик осуществить глубокую очистку технологических стоков от токсичных анионов и катионов, является чрезвычайно важной задачей. Следует отметить, что целый ряд эффектов, используемых для разделения ионов с помощью неорганических сорбентов, в принципе не может быть эффективно использован с применением ионообменных материалов на основе органических полимеров.
Исследования, проводимые в конце прошлого века Львовичем Б.И., Сальниковой В.А., Науменко Л.В., Вольхиным В.В.,Сухаревым Ю.И., Воловичем А.М., Барковским И.П., Павловичем Ю.А., Бичиным Н.А., Сметанкиным В.И., Окопной Н.Т., Ропотом В.М., Оратовским В.А., Комиссаровой Л.Н., Шацким В.М., Моисеевым В.Е., позволили разработать широкий спектр неорганических материалов, однако они не всегда отвечали требованиям, позволяющим широко использовать их на практике. Поэтому проблема создания работоспособных неорганических ионообменных материалов, обладающих достаточной механической прочностью, осмотической устойчивостью, приемлемой кинетикой массообменных процессов до сих пор является достаточно актуальной. Анализ литературных данных показал, что наиболее перспективными являются сорбенты на основе двойных гидроксидов металлов со структурой гидроталькита.
Диссертационная работа выполнена в соответствии с темой НИР Кубанского государственного технологического университета «Научные исследования высшей школы в области химии и химических продуктов. Разработка новых путей синтеза и исследование физико-химических свойств систем на основе оксидов и гидроксидов» (№ государственной регистрации 01200511295).
Целью работы является синтез неорганического сорбента со структурой гидроталькита на основе совместно осажденного гидроксида магния и алюминия с использованием золь-гель процесса, исследование механизма взаимодействия между анионами и сорбентом. Определение кинетических характеристик процессов сорбции и десорбции.
В ходе выполнения исследования решались следующие задачи:
*Синтез совместно осажденного гидроксида магния и алюминия с использованием золь-гель процесса.
*Определение адсорбционно-структурных характеристик сорбента.
*Установление механизма взаимодействия анионов Cr(VI), Hg(II), [Fe(CN)6]3-, [Fe(CN)6] 4- с совместно осажденным гидроксидом магния и алюминия.
*Изучение динамики сорбции.
*Определение кинетических характеристик процессов сорбции указанных анионов совместно осажденным гидроксидом магния и алюминия.
*Разработка рекомендации по эффективному использованию полученных сорбентов для очистки сточных вод гальванических производств.
Научная новизна работы:
Предложен новый способ получения магний-алюминиевого сорбента со структурой гидроталькита с использованием золь-гель процесса, исследована его сорбционная способность по отношению к ионам CrO42-, [Fe(CN)6]3,[Fe(CN)6] 4-, [Hg I4] 2-.
Установлены механизмы взаимодействия указанных анионов с совместно осажденным гидроксидом магния и алюминия со структурой гидроталькита.
С использованием программы FAVORIT получен атлас решений системы дифференциальных уравнений для моделирования процесса сорбции в динамических условиях.
Определены сорбционно-кинетические показатели, характеризующие процесс ионного обмена на синтезированном сорбенте.
Показана принципиальная возможность применения разработанного сорбента для сорбции CrO42-, [Fe(CN)6]3-, [Fe(CN)6] 4-,[Hg I4] 2-.
Практическая значимость работы: Синтезирован сорбент на основе гидроксидов магния и алюминия, который может применяться для извлечения анионов CrO42-, [Fe(CN)6]3-, из сточных вод гальванических производств. Проведено полупромышленное испытание полученного сорбента на ОАОТ «Краснодарский ЗИП». Предлагаемая технология сорбции позволит очистить стоки гальванического цеха от хрома(VI), [Fe(CN)6]3- до норм ПДК. Полученные результаты могут быть использованы при проведении лекций, а также практических занятий по курсу «Экология» в КубГТУ и других технических университетах.
На защиту выносятся:
1. Рекомендации по выбору методов синтеза и гранулирования неорганических ионитов для обеспечения наиболее благоприятного кинетического режима.
2. Данные исследований физико-химических свойств совместно осажденного гидроксида со слоистым типом структуры на основе гидроксидов магния и алюминия.
3. Результаты экспериментальных исследований динамики сорбции, ее теоретическое описание на основе полученных кинетических уравнений.
4. Результаты экспериментальных исследований кинетики ионного обмена на СОГ со слоистым типом структуры на основе гидроксидов магния и алюминия с применением математических моделей.
Апробация работы: Материалы диссертации докладывались и обсуждались на Всероссийской научно-практической конференции «Защитные покрытия в машиностроении и приборостроении», Пенза, 2005 г, VII Всероссийской научно-технической конференции «Новые химические технологии: производство и применение», Пенза, август 2005 г, II Международный симпозиум «Разделение и концентрирование в аналитической химии и радиохимии », Краснодар, сентябрь 2005 г, VIII Международной научно-практической конференции «Экология и жизнь», Пенза, 24-25 ноября 2005 г, III Международной научно-практической конференции «Теоретическая и экспериментальная химия»», Караганда, 21-22сентября 2006г., III Международной научно-практической конференции «Проблемы экологии: наука, промышленность, образование», Белгород, 25–27октября2006г
Публикации: Основное содержание диссертационной работы опубликовано в 7статьях и 7 тезисах докладов.
Структура и объем работы: Диссертационная работа, изложена на 120 страницах машинописного текста, из них 23 рисунков ,19 таблиц, 1 приложения, состоит из введения, четырех глав, общих выводов, списка литературы из 110 наименований работ российских и зарубежных авторов.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Во введении обоснована актуальность выбранной темы, сформулированы цель и задачи исследования, отражена научная новизна и практическая значимость работы, а также основные положения диссертации, выносимые на защиту.
В первой главе представлен анализ состояния исследований по составу, структуре и свойствам, методам получения, возможным областям применения сорбентов на основе оксидов и гидроксидов металлов. Рассмотрены технические решения, применяемые для получения этих материалов в гранулированном виде. Приведены данные об устойчивости и формах состояния исследуемых анионов в водных растворах. Обсуждены современные представления о взаимодействии ионов с соответствующими гидроксидами и имеющиеся методы прогнозирования его результатов. Показано, что сведения о механизме сорбции и десорбции для данного класса сорбентов весьма ограничены, что затрудняет синтез новых видов неорганических сорбентов с заданной структурой.
Во второй главе представлены методики синтеза, гранулирования и исследования физико-химических свойств сорбентов. В работе применены методы рентгенофазового, ИК - спектроскопического, химического, атомно-адсорбционного анализа, потенциометрического титрования. Величину удельной поверхности образца определяли по низкотемпературной адсорбции азота хроматографическим методом с последующей обработкой полученных результатов по методу БЭТ. Для определения пористости использована ртутная порометрия.
В третьей главе описана методика синтеза совместно осажденных гидроксидов и приведены основные результаты исследования физико-химических свойств, а так же данные по изучению сорбции ионов CrO42, [Fe(CN)6]3-, [Fe(CN)6] 4-, [Hg I4]2 на синтезированном сорбенте.
Для синтеза совместно осажденных гидроксидов магния и алюминия использовали 1,0 н растворы хлоридов магния и алюминия, смешанных в соотношении 4:1, по литературным данным признанным оптимальными. Полученную смесь при интенсивном перемешивании добавляли к 1н раствору гидроксида натрия. Значение рН поддерживали в интервале 9,6-10. Осадок выдерживали в маточном растворе в течение 24 часов, затем отмывали дистиллированной водой методом декантации до отрицательной реакции на ионы С1- как в растворе, так и в самом осадке, после чего осадок отжимали и подвергали гранулированию, помещая пастообразный материал в формы и высушивая при температуре 1200С. Известно, что при замачивании высушенного материала в воде происходит частичное растрескивание исходных гранул. Причиной разрушения является возникновение напряжения, вызванного его усадкой при высушивании. В сухом материале эти напряжения компенсируются силами сцепления отдельных твердых фрагментов, при замачивании возникает дополнительная нагрузка, обусловленная образованием двойного электрического слоя на стенках пор или давлением, возникающим при заполнении капиллярной системы раствором. Эти процессы могут происходить в ходе эксплуатации сорбента. Поэтому для увеличения осмотической устойчивости применяли золь-гель процесс. Смесь солей хлоридов магния и алюминия, взятых в соотношении 4:1 капельно диспергировали в большую емкость с раствором NaOH, где происходит образование частиц твердой фазы. После отверждения гель-сферы промывали водой, а затем высушивали.
При использовании золь-гель процесса, продуктом реакции является не аморфный осадок, а сферические частицы геля размером 5-8 мм. Согласно литературным данным малые размеры частиц геля приводят к относительно небольшим линейным усадкам в ходе высушивания гидрогеля, что в свою очередь, препятствует возникновению и развитию трещин в высушиваемом материале. Данный метод получения позволяет получать сорбенты прочность гранул, которых значительно превосходит этот показатель для материалов, изготовленных путем осаждения в свободном объеме. Выбирая методику получения совместно осажденных гидроксидов с использованием золь-гель процесса, исходили из того, что она обеспечивает получение достаточно прочных гранул доступных для массообменных процессов. Следует отметить, что в данном случае не следует добавлять связующее вещество, так как гидроксид магния способен к поликонденсации с образованием механически прочных структур.
Для характеристики структуры СОГ проведен рентгенофазовый анализ, метод ИК-спектроскопии Полученные данные подтвердили образование структуры типа гидроталькита с примесью фазы брусита (Mg(OH)2).
![]() На ИК-спектрах образцов СОГ магния и алюминия (рис. 1) проявляется узкая полоса поглощения ν (ОН) в области 3660 -3620 см-1, которая отвечает валентным колебаниям связи ОН не возмущенным водородными связями и свидетельствующая о присутствии фазы Mg(OH)2. Полоса при 1595см-1 принадлежит деформационным колебаниям воды, полосы при 1020, 860 и 735 см-1вызваны деформационными колебаниями групп ОН ˉ гидроксидов, связь Ме – О дает слабые полосы поглощения в области 510 – 470 см-1.
На ИК-спектрах образцов СОГ магния и алюминия (рис. 1) проявляется узкая полоса поглощения ν (ОН) в области 3660 -3620 см-1, которая отвечает валентным колебаниям связи ОН не возмущенным водородными связями и свидетельствующая о присутствии фазы Mg(OH)2. Полоса при 1595см-1 принадлежит деформационным колебаниям воды, полосы при 1020, 860 и 735 см-1вызваны деформационными колебаниями групп ОН ˉ гидроксидов, связь Ме – О дает слабые полосы поглощения в области 510 – 470 см-1.
 |
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 4000 3500 3000 2500 2000 1500 1000 500 ν см-1
4000 3500 3000 2500 2000 1500 1000 500 ν см-1
Рис. 1. ИК - спектр СОГ магния и алюминия
Одним из основных свойств неорганических сорбентов является структура порового пространства.
Для характеристики пористой структуры определяли: удельную поверхность; объем пор, отнесенный к массе сорбента; распределение пор по эквивалентным радиусам.
Размеры микропор (радиус меньше 0.15нм) соизмеримы с размерами адсорбируемых молекул, поэтому систему микропористый адсорбент-адсорбат рассматривают как однофазную, именно в микропорах размещаются сорбируемые ионы.
Мезопоры (радиусы от 0.15 до 200нм) обеспечивают транспорт ионов в пределах гранул. При этом адсорбция электролитов на поверхности данных пор приводит к образованию двойного электрического слоя и возникновению расклинивающего давления.
Макропоры (от 200 до 2000нм) рассматриваются как система магистральных трещин, развитие которых под действием нагрузок, возникающих в мезопорах, приводит к разрушению гранулы.
Адсорбционно-структурные характеристики образца совместно осажденного гидроксида высушенного при температуре 120 0С приведены в таблице 1.
Таблица 1.
Адсорбционно-структурные характеристики образца СОГ
| Удельная поверхность, м2/г | Общий объем пор, см3/г | Распределение пористости по эквивалентным радиусам, нм |
||||
| 3-10 | 10 -102 | 102 – 103 | 103-104 | 104 -3 104 | ||
| 135 | 0,34 | 0,135 | 0,147 | 0,012 | 0,028 | 0,008 |
Полученные результаты показывают возможность применения полученного СОГ в качестве сорбента.
Известно, что в зависимости от рН раствора Сr(VI) может существовать в виде как протонированных, так и депротонированных форм, кроме того состояние Сr(VI) в растворе также зависит от его собственной концентрации. Катионы ртути (II) в водных растворах в зависимости от рН и концентрации галогенид ионов могут существовать в следующих формах: HgНаI2, [HgНаI3], [HgНаI4] 2-, HgОНСI, Hg(ОН)2. На рис. 2 представлены зависимости изменения содержания комплексов ртути (II) в растворах солей NaHaI.
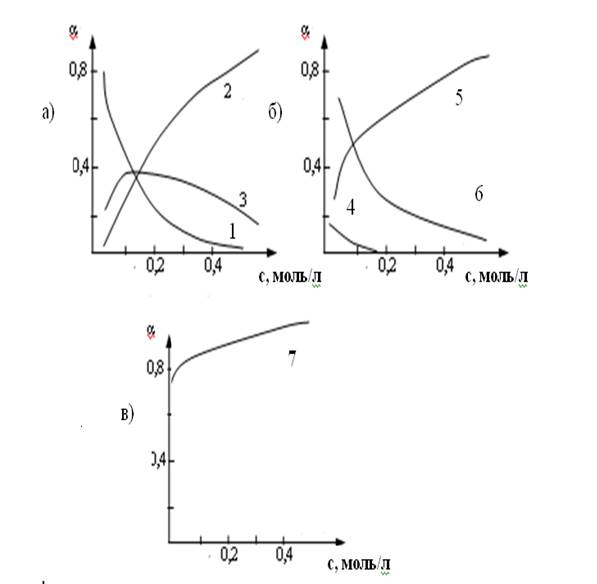
Рис.2. Графики зависимости процентного содержания комплексов ртути (II) от концентрации NaHaI в растворах.
a) NaCI , б) NaBr в) NaI ;
1-HgСI2 , 2-[HgСI3]-, 3-[HgСI4]2-, 4- HgBr2 , 5- [HgBr3]-, 6-[HgBr4]2-,7-[Hg I4]2-.
Анализ концентрационных диаграмм показывает, что в разбавленных растворах в присутствии NaCI при малом содержании ионов хлора преобладают нейтральные молекулы HgСI2, при увеличении концентрации NaCI до 0,1 моль/ л количество анионных комплексов возрастает до 35-40 %, в присутствии NaBr или NaI в тех же количествах, что и NaCI в первом случае содержание HgBr2 составляет 10- 15 % , при увеличении концентрации NaBr до 0,15 моль/ л в растворе присутствуют только анионные комплексы состава [HgBr3] - и [HgBr4] 2-, для иодидных растворов во всем диапазоне исследуемых концентраций присутствуют только комплексы состава [Hg I4] 2- .
Изучение сорбционной активности сорбентов на основе СОГ проводили в статических условиях по стандартным методикам, при этом использовали гранулы в виде шариков диаметром 2,5-3 мм. В качестве адсорбатов использовали Сr(VI), [Fe(CN)6]4- , [Fe(CN)6] 3- , [Hg На14] 2-. Результаты лабораторных исследований сорбции Cr (VI) представлены в таблице 2.
Таблица 2
Результаты сорбции и десорбции оксоанионов Cr (VI) на СОГ
| Значения Е, ммоль CrO42-/ г СОГ | |||||
| 1 | 2 | 3 | |||
| Сорбция | Десорбция | Сорбция | Десорбция | Сорбция | Десорбция |
| 1, 23 | 0,846 | 1,05 | 0,73 | 0,72 | 0, 57 |
Результаты эксперимента показывают, что ионы CrO42-обмениваются с ионами ОН-, входящими в состав совместно осажденных гидроксидов. При этом рН раствора увеличивается до с 7,3 до 8,4.
Эффект понижения сорбционной емкости в циклах сорбция-десорбция можно объяснить переходом части ионов CrO4 2- в необменное состояние за счет обмена с ОН - группами слоев структуры
≡Ме-OH+CrO42-<=>≡Ме-OСrO3- + OH-
Поглощенные таким образом хромат-ионы участвуют в компенсации положительного заряда слоев структуры и тем самым уменьшают содержание межслоевых ионов, способных участвовать в анионном обмене. Образование связи Ме - ОCrO3 подтверждают данные ИК-спектроскопии: в спектре продукта сорбции по сравнению с исходным образцом, появляется дополнительная полоса при 860-910 см-1, которая относится к колебанию связи -О-CrO3-
Судя по результатам рентгенофазового анализа насыщение образца ионами CrO42- приводит к образованию новой фазы с меньшим межслоевым расстоянием по сравнению с исходной фазой. По литературным данным, такой результат возможен при образовании прямых связей Mе-O-CrO3.
Анализ полученных результатов позволяет сделать вывод, что в процессе сорбции анионы обмениваются как с гидроксильными группами на поверхности сорбента, так и с гидроксильными группами, принадлежащими внутреннему объему фазы СОГ гидроксидов. Причем в данном случае полизарядные анионы могут обмениваться на гидроксо-группы гидроксидных слоев, связанных напрямую с атомами металла и, компенсируя оставшимся зарядом положительный заряд слоев, переходить в неионообменное состояние. Количество ионообменных ионов при этом уменьшается.
Цианидные комплексные анионы железа (II,III) характеризуются высокой устойчивостью, они практически не гидролизуются в водных растворах. Рассмотрим результаты сорбции ионов [Fe(CN)6]4- и [Fe(CN)6]3- на СОГ (табл. 3). Следует отметить, что принципиальных различий в поведении ионов [Fe(CN)6]4- и [Fe(CN)6]3- не обнаружено. Исследование эквивалентности ионного обмена показало, то в обмене могут участвовать не только анионы, но и катионы щелочных металлов, при этом образуются смешанные гексацианоферраты Mg-К.
Таблица 3
Результаты сорбции и десорбции [Fe(CN)6]4- на СОГ
| Значения Е, ммоль [Fe(CN)6]4-/ г СОГ | |||||
| 1 | 2 | 3 | |||
| Сорбция | Десорбция | Сорбция | Десорбция | Сорбция | Десорбция |
| 0,68 | 0,56 | 0,55 | 0,38 | 0,42 | 0, 37 |
Образование новой фазы KMg[Fe(CN)6] подтверждено результатами рентгенофазового анализа. ИК-спектр продукта сорбции ионов [Fe(CN)6]3- СОГ магния и алюминия при рН > 10 включает полосу поглощения при 2100 см-1, которую можно отнести к колебаниям гексацианоферрат (III) ионов. Однако в ИК-спектре продукта сорбции при рН исходного раствора ниже 9 наблюдаются две полосы поглощения при 2170 см-1 и 2100 см-1, что характерно для мостиковых групп -CN- , свойственных смешанному гексацианоферрату. При сорбции [Fe(CN)6]4- образование смешанного гексацианоферрата происходит при рН < 10,5. Расщепление полос в спектре [Fe(CN)6]4- носит более сложный характер, что, вероятно, может быть связано с частичным окислением кислородом воздуха железа (II) в комплексе.
Изучение сорбционных свойств СОГ магния и алюминия по отношению к Hg(II) показало, что наибольшая эффективность сорбции Hg(II), достигнутая в интервале значений концентраций Hal от 10-2 до10-3 моль / л соответствует раствору, в котором Hg(II) присутствует в формах HgСI2 и HgОНСI, при переходе к комплексным формам значение сорбционной емкости уменьшается от 34 до 21 мг Hg(II) / г СОГ. При увеличении концентрации ионов хлора больше чем в 4 раза сорбционная емкость также уменьшается (с 21 до 14 мг Hg(II) / г СОГ), при дальнейшем увеличении концентрации ионов СI значение сорбционной емкости уменьшается незначительно. Исходя из полученных экспериментальных данных можно предположить, что поглощение ионов [HgНаI3]-, [HgНаI4]2- может происходить за счет ионного обмена:
≡+Ме- ОН + [HgHaI3 ]– <=> ≡+МеHal- HgHaI2 + ОН– ,
то есть в отсутствии гидролизованных форм Hg(II) в растворах можно предположить ионообменный механизм сорбции. Повышение Е для гидролизованных форм Hg(II) связано с тем, что в данном случае образуются поверхностные внутрисферные комплексы AIOHgCI и AIOHgOHCI. Следует отметить понижение сорбции Hg(II) из растворов, содержащих ионы Br- и I- (табл.4), что можно объяснить повышением устойчивости комплексов [HgНаI3]- , [HgНаI4]2- (рК [HgBr3]–=19,7; рК [HgBr4]2-=21,0; рК [HgI3]–=27,6; рК[HgI4]2– =29,8).
Таблица 4.
Результаты сорбции Hg(II) из растворов, содержащих ионы НаI –
| Анион в растворе | CI- | Br- | I- |
| Е, мг Hg(II)/г СОГ | 24,6 |
15,4 |
8,3 |
Установлено, что по мере роста ионообменного механизма поглощения Hg (II) увеличивается доля десорбированной ртути (табл.5).
Таблица 5
Экспериментальные данные десорбции анионов раствором Na2 НРO4
| Анион | [HgСI4]2– | [HgBr4]2- | [Hg I4]2- |
Степень десорбции, % |
45 |
68 |
98 |
На основании полученных данных можно сделать вывод, что взаимодействие ионов CrO4 2- и [Hg I4]2- происходит по ионообменному механизму, а в случае остальных анионов могут происходить специфические реакции (образование основных солей и смешанных гексацианоферратов), сопровождающие ионный обмен.
При изучении кинетики сорбции анионов на полученном сорбенте для реализации анионного обмена в чистой форме в качестве модельных анионов использовали галогенид ионы. Ионный обмен проводили из раствора КС1 с концентрацией 0.001 М, при температуре 23°С, рН раствора 9,0. Отсутствие влияния стадии стока ионов в твердую фазу сорбента было подтверждено экспериментально путем последовательного уменьшения размеров гранул и определением скорости поглощения хлорид-ионов для каждой из выделенных фракций. Анализ зависимости скорости ионного обмена от размера гранул подтвердил, что кинетика лимитируется стадией диффузии в поровом пространстве гранул.
Для описания экспериментальных данных кинетики ионного обмена использована математическая модель, предложенная профессором Вольхиным В.В., которая основывается на следующих предположениях:
1. Кинетика обмена хлорид-ионов на СОГ магния и алюминия
лимитируется стадией диффузии ионов в поровом пространстве гранулы.
2. Гранулы СОГ магния и алюминия представляют собой агломераты из кристаллитов. Пространства между ними составляют макропоры,
заполненные раствором, по которым обеспечивается транспорт ионов
внутрь гранулы из внешнего раствора. Снижение коэффициента диффузии
внутри пор, составляющих каналы, объясняется меньшей проницаемостью
гранул, извилистостью каналов, по которым диффундируют ионы, их
взаимодействием со стенками пор, где возможно образование двойного
электрического слоя, повышенной вязкостью раствора в порах.
3. Коэффициент взаимодиффузии ионов в поровом пространстве
гранулы определяется согласно модели Туницкого-Гельфериха, при этом
подвижности ионов в поровом пространстве пропорциональны их
подвижностям во внешнем растворе.
4. Изотерма обмена может быть представлена в ленгмюровском виде.
5. Гранулят предполагается монодисперсным, форма гранул - сферическая.
Кинетическая кривая сорбции хлорид - ионов на СОГ магния и алюминия представлена на рис. 3
Е,ммоль/г
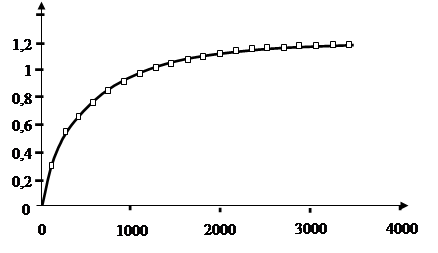
t. сек
Рис. 3 Кинетическая кривая сорбции хлорид - ионов на СОГ магния и алюминияНа кинетической кривой обнаружены два кинетических участка: первый участок отвечает диффузии ионов в макропорах сорбента, на втором участке наблюдается более медленный обмен хлорид-ионов, что, на наш взгляд, вызвано анионным обменом в межслоевых пространствах. Полученные кинетические данные свидетельствуют о высокой скорости химических реакций, приводящих к извлечению анионов из раствора, а также о том, что данные материалы могут быть использованы в процессах очистки сточных вод.
В четвертой главе представлен алгоритм и программа расчета динамики сорбции. Для исследований применен метод, основанный на фильтровании через короткие слои сорбента.
Исследование проводили следующим образом: колонку диаметром 20мм и длиной 400мм загружали исследуемым сорбентом с заданной толщиной слоя и установленным ранее диаметром зерен 2,5-3мм. Фильтрование модельных стоков проводили с заданными концентрациями ионов. Скорость фильтрования поддерживали медицинским дозатором. Пробы фильтрата для анализа отбирали через каждые 20 минут. Концентрацию определяли фотоколориметрическим методом анализа, рН контролировали рН-метром.
На первом этапе исследования толщина слоя сорбента (l) составляла l=400мм. Скорость фильтрования устанавливали υ1=2м/ч, υ 2=3м/ч, υ4=4м/ч. Эффективность очистки стоков во времени оценивалась уровнем проскоковой относительной концентрации (U) ионов в фильтрате, которая определяется соотношением:
U=Сф/С0 ,
где Сф-концентрация ионов в фильтрате;
С0- концентрация ионов в воде, поступающей на фильтрацию.
Процесс фильтрования прекращали, когда уровень проскоковой относительной концентрации стабилизировался. Следующая серия опытов проводилась аналогично, но постоянными оставались концентрация ионов и скорость υ3 =3 м/ч.
В качестве теоретической основы экспериментального определения параметров сорбции использовали математическую модель Петрова, позволяющую описать экспериментально полученные закономерности. При разработке модели использовали методы, позволяющие решить систему дифференциальных уравнений, предложенные Е.В.Венециановым и Е.Г.Петровым.
При проведении опыта известными и постоянными величинами являются: толщина слоя сорбента l, средний диаметр зерен d, скорость фильтрования (υ). Кроме этого постоянными, но неизвестными величинами являются коэффициенты, характеризующие процесс сорбции.
Этими параметрами являются коэффициент внешней диффузии β и кинетические параметры: коэффициент внутренней диффузии D и критерий, учитывающий относительный вклад внешней и внутренней диффузии Н (критерий Био). Массообменным (емкостным) коэффициентом, характеризующим распределение адсорбированного вещества, является коэффициент Генри Г.
Критерий Био равен
![]() (1) ,
(1) ,
безразмерная толщина (Х) слоя сорбента равна
![]() (2).
(2).
Связь между безразмерным (Т) и реальным(t) временем сорбционного процесса определяется по формуле:
![]() (3) ,
(3) ,
откуда следует однозначное соответствие этих времен.
После логарифмирования последнего соотношения получим:
![]() (4)
(4)
Из выражения (4) следует, что в логарифмической системе координат эта связь становится аддитивной, и однозначное соответствие времен может быть установлено продольным смещением временных осей относительно друг друга. Методика сопоставления экспериментальных и теоретических кривых следующая: в результате фильтрования через слой сорбента получают экспериментальные точки зависимости
uэ=f(tэ) (5),
где uэ-экспериментально определенная относительная концентрация ионов в фильтрате; tэ-время, отсчитываемое с начала фильтрования.
Экспериментальные точки этой зависимости наносили на билогарифмическую сетку (рис.4), полностью аналогичную сетке теоретических кривых добиваясь при этом путем перемещения графиков вдоль осей времени наилучшего совпадения экспериментальных точек с одной из теоретических кривых U=F(X,T) при Н=const до соблюдения равенства uэ=U.
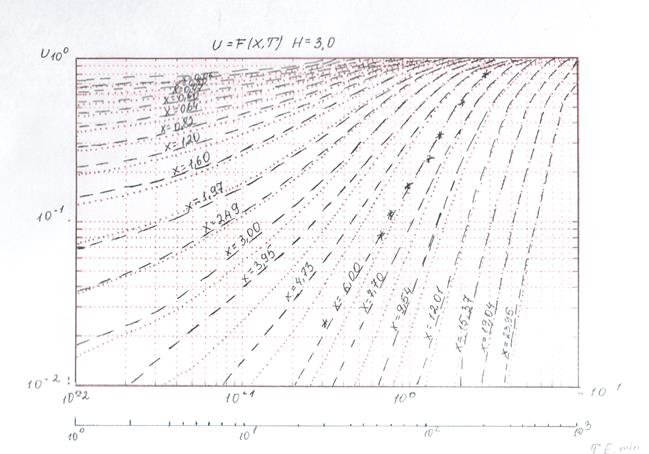
Рис.4 Наложение экспериментальных точек фильтрования на теоретические кривые динамики сорбции из жидких сред для [Fe(CN)6]3-.
Проведенные исследования позволили расчетным путем провести количественную оценку относительной способности ионов адсорбироваться полученным сорбентом, и на основе сопоставления расчетных и экспериментальных данных определить эффективность теоретических прогнозов и выявить те факторы, влияние которых приводит к отдельным отклонениям.
Выводы
1. Разработана новая методика синтеза сорбента на основе гидроксидов магния и алюминия со структурой гидроталькита с использованием золь-гель процесса.
2. Определены адсорбционно-структурные характеристики СОГ (удельная поверхность -135м2/г), общий объем пор - 0.34см3/г, распределение пористости по эквивалентным радиусам), позволяющие предложить синтезированный совместно осажденный гидроксид магния и алюминия в качестве неорганического ионообменника. Величину удельной поверхности образца определяли по низкотемпературной адсорбции азота хроматографическим методом с последующей обработкой полученных результатов по методу БЭТ. Для определения пористости использована ртутная порометрия.
3. Методами ИК-спектроскопии и ренгенофазового анализа установлены механизмы взаимодействия CrO42-, [Fe(CN)6]3-, [Fe(CN)6] 4, HgI4] 2- с совместно осажденным гидроксидом магния и алюминия со структурой гидроталькита.
- Выявлено, что полученный сорбент способен поглощать Cr (VI) за счет обмена, как с поверхностными, так и межслоевыми ОН - группами СОГ. Показана возможность обмена хромат-ионов на гидроксогруппы гидроксидных слоев, связанных напрямую с атомами металла. При этом количество гидроксильных групп способных обмениваться на Cr(VI) уменьшается, так как Cr (VI) переходит в неионообменное состояние.
- Установлено, что в отсутствии гидролизованных форм Hg(II) в растворах имеет место ионообменный механизм сорбции, для гидролизованных форм Hg(II) сорбция сопровождается образованием поверхностных внутрисферных комплексов AIOHgCI и AIOHgOHCI.
- Показано, что сорбция гексацианоферат-ионов зависит от рН и может протекать по двум механизмам: ионообменному, который лимитируется внутренней диффузией (при рН>10), и ионообменному, сопровождающемуся образованием новой фазы смешанного гексацианоферрата KMg [Fe(CN)6] (при рН<9). Скорость данного процесса лимитируется скоростью гетерогенной обменной реакции.
4. Исследована кинетика ионного обмена для всех вышеуказанных анионов. Установлено, что она лимитируется процессом внутренней диффузии ионов в транспортных порах сорбента. Экспериментальные данные сопоставлены с рассчитанными по моделям кинетики и динамики ионного обмена на зернистых сорбентах, что позволило применить полученные расчетные кривые для обработки и прогнозирования применения сорбента в опытно-промышленных условиях.
5. Показана возможность применения сорбентов на основе СОГ магния и алюминия для очистки сточных вод, содержащих Cr (VI), [Fe(CN)6]3- , что подтверждено проведением опытно-промышленных испытаний по извлечению Cr(VI), [Fe(CN)6]3- из сточных вод гальванических цехов ОАОТ «Краснодарский ЗИП». Установлено, что сорбент является высоко селективным к Cr(VI), [Fe(CN)6]3- и устойчив при работе в многоциклическом режиме.
Результаты диссертационной работы изложены в следующих публикациях:
1. Боковикова Т.Н. Синтез неорганических сорбентов на основе гидроксидов металлов и их систем. [Текст] / Т.Н. Боковикова, О.В. Новоселецкая, Н..Н. Полуляхова, Л.А. Марченко // Ж. «Известия высших учебных заведений. Северо-Кавказский регион. Технические науки», -г. Ростов-на Дону.-2005.- Приложение к №1, с.54-63.,
2 Полуляхова Н..Н. Решение проблемы очистки хромсодержащих стоков гальванопроизводств. [Текст] / Н..Н. Полуляхова, О.В.Новоселецкая, Р.И. Екутеч,А.А, Грахова // Сборник материалов 11 Всероссийской научно-практической конференции «Защитные покрытия в машиностроении и приборостроении»,- Пенза, 19-20 мая 2005 г, с. 74-75 .,
3. Процай А.А Расчет динамики сорбции ионов Cr(VI) в смешанно-диффузионной области кинетики. [Текст] / А.А. Процай, О.В. Новоселецкая, Н.М. Привалова, Н.Н. Полуляхова. // Сборник статей VII Всероссийской научно-технической конференции «Новые химические технологии: производство и применение», - Пенза, август 2005 г, с.86-90.,
4. Процай А.А. Ионообменные взаимодействия между гидроксидами двухвалентных и трехвалентных металлов и простых катионов [Текст] / А.А. Процай, О.В. Новоселецкая, Н.М. Привалова, Н.Н. Полуляхова. // Сборник статей VII Всероссийской научно-технической конференции «Новые химические технологии: производство и применение». Пенза, август 2005 г, с.82-86.,
5. Боковикова Т.Н. Сорбционные свойства азотсодержащих сорбентов [Текст] / Т.Н. Боковикова, О.В. Новоселецкая, Л.А. Марченко. // II Международный симпозиум «Разделение и концентрирование в аналитической химии и радиохимии».Краснодар, сентябрь 2005 г, с. 133-134.
6. Марченко Л.А. Технологические особенности получения сорбентов на основе гидроксидов металлов». [Текст] / Л.А.Марченко, О.В. Новоселецкая, В.В. Шерстова, Н.Г.Шкода // Ж. «Современные наукоемкие технологии». - Москва.- 2005г.№5.- С. 43.,
7.Новоселецкая О.В. Сорбенты на основе гидроксидов металлов в решении прикладных задач». [Текст] / О.В. Новоселецкая, А.А. Процай, Н.Н. Полуляхова // Сборник статей VIII Международной научно-практической конференции «Экология и жизнь», Пенза, 24-25 ноября 2005 г, с. 22-23.,
8.Новоселецкая О.В. Гальваношламы как основа для синтеза неорганических сорбентов [Текст] / О.В. Новоселецкая, А.А. Процай, Н.М. Привалова // Сборник статей VIII Международной научно-практической конференции «Экология и жизнь», Пенза, 24-25 ноября 2005 г. с. 24-25.,
9.Боковикова Т.Н. Физико-химические основы сорбции модифицированными неорганическими сорбентами. [Текст] / Т.Н. Боковикова, О.В. Новоселецкая А.А. Процай, Н.Н. Полуляхова // Ж. «Известия высших учебных заведений. Химия и химическая технология». Иваново.2006.- № 6 , с.54-63.,
10. Боковикова Т.Н. Исследование механизма сорбции в физико-химических системах. [Текст] / Т.Н. Боковикова, О.В. Новоселецкая А.А. Процай, Н.Н. Полуляхова // Ж. «Известия высших учебных заведений. Химия и химическая технология». Иваново.2006.- №7. с.54-63.,
11. Новоселецкая О.В Изучение кинетики ионного обмена на неорганических ионитах [Текст] / О.В. Новоселецкая, А.А. Процай, Н.М. Привалова // Сборник статей III Международной научно-практической конференции «Теоретическая и экспериментальная химия»», Караганда, 21-22 сентября 2006 г., с.82-86.,
12. Новоселецкая О.В. Двойные гироксиды в качестве анионообменников: механизм поглощения ионов двойным Mg(OH)2-AlOOH гидроксидом. [Текст] / О.В. Новоселецкая, А.А. Процай, Н.М. Привалова // Сборник статей III Международной научно-практической конференции «Теоретическая и экспериментальная химия»», Караганда, 21-22 сентября 2006 г., с.82-86.,
13. Новоселецкая О.В. Использование неорганических ионитов в очистке сточных вод. [Текст] / О.В. Новоселецкая, Н.Н. Полуляхова, А.А. Процай // Сборник статей III Международной научно-практической конференции «Проблемы экологии: наука, промышленность, образование», Белгород , 25-27 октября 2006 года, с.82-86.,
14. Боковикова Т.Н. Некоторые особенности сорбционного извлечения ртути (II) совместно осажденными гидроксидами магния и алюминия. [Электронный] Т.Н. Боковикова, О.В. Новоселецкая, А.С. Шабанов // Электронный журнал «Физико-химический анализ свойств многокомпонентных систем». Краснодар- Выпуск 3.-2007.