| Скачать .docx | Скачать .pdf |
Реферат: Силикаты и их использование
Содержание
Введение
1. Становление науки о силикатах
2. Кристаллохимическая систематика силикатов
3. Процессы образования силикатов в земной коре
4. Яркие представители группы силикатов
5. Применение и искусственное происхождение силикатов
Заключение
Список используемой литературы
Введение
Силикаты и алюмосиликаты представляют собой обширную группу минералов. Для них характерен сложный химический состав и изоморфные замещения одних элементов и комплексов элементов другими. Главными химическими элементами, входящими в состав силикатов, являются O, Si, Al, Fe2+ , Fe3+ , Mg, Mn, Ca, Na, K, а также Li, B, Be, Zr, Ti, F, H, в виде (OH)1- или H2 O и др.
Общее количество минеральных видов силикатов около 800. По распространённости на их долю приходится более 90% минералов литосферы. Силикаты и алюмосиликаты являются породообразующими минералами. Из них сложена основная масса горных пород: полевые шпаты, кварц, слюды, роговые обманки, пироксены, оливин и др. Самыми распространёнными являются минералы группы полевые шпаты и затем кварц, на долю которого приходится около 12% от всех минералов.
1. Становление науки о силикатах
Хотя история развития человеческого общества тесно переплетена с использованием силикатов как природного, так и искусственного происхождения, научный подход к изучению этих соединений сформировался относительно поздно – в конце XVIII – начале XIX столетия вместе со становлением химической науки. Это объясняется и специфическими особенностями силикатов: сложностью строения, вариациями химического состава, нерастворимостью и химической пассивностью, способностью к переходу в нестабильные состояния и высокой температурой плавления.
Первой научной теорией по систематике силикатов была так называемая поликремневая теория силикатов, которая на протяжении длительного времени (конец первой половины XIX ‑ 20-е годы XX века) играла важную роль в химии силикатов. Согласно этой теории, силикаты рассматривались как соли кремниевых кислот общей формулы nSiO2 " mH2O (n, m – целые числа). Значениям n > 1 соответствовали поликремневые кислоты. Простейшими представителями кремниевых кислот являются метакремневая H2SiO3 (n = 1, m = 1), ортокремневая Н4SiO4 (n = 1, m = 2), двуметакремневая H2Si2O5 (n = 2, m = 1), пирокремневая H6Si2O7 (n = 2, m = 3). Соли этих кислот получили названия мета-, двумета-, орто- и пиросиликатов соответственно. Для простых силикатов такие названия общеприняты и в настоящее время. Невозможность выделения кремниевых кислот в чистом виде из-за их коллоидного характера оставляла открытым вопрос о солеобразной природе силикатов. Более того, многообразие силикатов не укладывалось в рамки этой теории. Например, минералы жадеита NaAlSi2O6 и лейцита KAlSi2O6 относятся, казалось бы, к солям метакремниевой кислоты, но по своим свойствам сильно отличаются друг от друга. В приведенном случае поликремневая теория не смогла дать ответ о связи между химическим составом силикатных соединений и их строением, что является основной задачей любой систематики. Однако при формировании поликремневой теории была высказана гениальная догадка о полимеризации атомов кремния через атомы кислорода.
В своих трудах, посвященных природе силикатов, Д.И. Менделеев указывал на противоречия поликремневой теории. Он высказал идею об изоморфном замещении в силикатах не только оксидов одинакового типа, но и разных, таких, как SiO2 и Al2O3. Это наводило на мысль о сходстве и химических свойств этих оксидов. Далее на основании достаточно широкой вариации соотношения между основными и кислотными оксидами в силикатах Д.И. Менделеев отмечал, что нельзя объяснить все многообразие силикатов только существованием полимерных форм кремниевых кислот. По его мнению, силикаты представляют собой не соли, а «неопределенные соединения», такие, например, как сплавы, но не простых тел, а близких по своим свойствам оксидов. Д.И. Менделеев объяснял особенности силикатных «неопределенных соединений» не существованием различных видов поликремневых кислот, а полимеризацией большинства соединений кремния. Учение Д.И. Менделеева сыграло большую роль в дальнейшем понимании природы силикатов. В конце XIX века химические методы исследования (аналитические и синтетические) исчерпали свои возможности в познании силикатов. Исследователи начали искать новые пути решения проблем силикатов. Наиболее значительные результаты были достигнуты в физико-химическом и геохимическом направлениях.
Метод физико-химического анализа, созданный Н.С. Курнаковым в 20-е годы XX столетия, представляет собой синтез идей химической термодинамики и топологии. В рамках этого метода наиболее информативным оказалось рассмотрение диаграммы температура-состав (диаграмма состояния). Диаграммы состояния позволяют судить о температурно-концентрационных интервалах существования кристаллических и жидких силикатов, их превращениях (плавление, кристаллизация, разложение или соединение). Результаты многочисленных исследований диаграмм состояния (бинарных, тройных и более компонентных систем) обобщаются в соответствующих справочниках, в компьютерных банках данных, монографиях и учебных пособиях. Особенный интерес диаграммы состояния представляют для понимания процессов минералообразования, в материаловедении и технологии силикатов. В настоящее время использование термодинамического метода позволяет корректировать экспериментально полученные диаграммы состояния, предсказывать диаграммы состояния неизученных систем, судить о возможности протекания тех или иных процессов превращений силикатов, рассчитывать энергоемкость этих процессов, сравнивать устойчивость образовавшихся соединений по отношению к распаду на близлежащие по диаграмме состояния. Эти выводы делаются как на базе экспериментальных данных, так и с помощью разнообразных модельных представлений. В этой области автором и его сотрудниками получены интересные результаты, касающиеся устойчивости силикатных соединений, определения областей кристаллизации из расплавов тех или иных силикатов.
Видным представителем геохимического направления является В.И. Вернадский, который интересовался именно строением силикатов. Он создал свою теорию строения алюмосиликатов (1891–1937 годы). В.И. Вернадский так же, как и Д.И. Менделеев, говорил о близости химических функций SiO2 и Al2O3 и отвергал мысль о том, что алюмосиликаты есть соли кремниевых кислот. По его мнению, алюмосиликаты являются производными сложных алюмосиликатных радикалов, «каолиновых ядер». Гипотеза о «каолиновом ядре» как о замкнутой группировке атомов Si, Al и O оказалась актуальной при расшифровке структуры полевых шпатов.
2. Кристаллохимическая систематика силикатов
По хим. природе С. и в особенности С. сложного состава и строения (в т.ч. цементные гидросиликаты, цеолиты, С. с добавочными анионами и комплексными катионами) относятся к типичным гетеродесмич. соединениям, в к-рых реализуются одновременно разл. типы хим. связи-ионная, ковалентная, ионно-ковалентная, координационная, водородная и др. многоцентровые связи.
Структурная классификация С. базируется на рентгено-структурных расшифровках кристаллич. строения важнейших породообразующих силикатных минералов (преим. с мелкими катионами Be, Mg, Al, Zn, Fe, отчасти Na и К), выполненных начиная с кон. 20‑х гг. У. Брэггом, Л. Полин-гом, Нараи Сабо. В основу структурной систематики С. (Брэгг, Ф. Махачки) было положено строение анионных группировок-способ сочленения между собой элементарных звеньев-правильных кремнекислородных тетраэдров ![]() (рис. 1) в анионные радикалы конечных размеров или же в бесконечные одно-, двух- и трехмерные группировки. С 1950 в рентгеноструктурных исследованиях преим. школы Н.В. Белова были расшифрованы мн. кристаллич. структуры С. и их неорг. аналогов с крупными катионами Na, К, Са, Ва, РЗЭ и др. В основе систематики кремнекислородных группировок по Брэггу лежит размерное соответствие ребер тетраэдров SiO4
и октаэдров MgO6
. По Белову для кристаллохимии С. характерно стерич. соответствие ребра октаэдра СаО6
с расстоянием между вершинами диорто-группы
(рис. 1) в анионные радикалы конечных размеров или же в бесконечные одно-, двух- и трехмерные группировки. С 1950 в рентгеноструктурных исследованиях преим. школы Н.В. Белова были расшифрованы мн. кристаллич. структуры С. и их неорг. аналогов с крупными катионами Na, К, Са, Ва, РЗЭ и др. В основе систематики кремнекислородных группировок по Брэггу лежит размерное соответствие ребер тетраэдров SiO4
и октаэдров MgO6
. По Белову для кристаллохимии С. характерно стерич. соответствие ребра октаэдра СаО6
с расстоянием между вершинами диорто-группы![]() . Это наиб. наглядно иллюстрируется сочленением кремнекислородных цепочек с октаэдрич. колонками Са- и Mg‑октаэдров в структурах пироксена энстатита Mg2
(Si, O6
),
(рис. 2, а) и пироксеноида волластонита Са3
(Si3
O9
),
(рис. 2, б).
. Это наиб. наглядно иллюстрируется сочленением кремнекислородных цепочек с октаэдрич. колонками Са- и Mg‑октаэдров в структурах пироксена энстатита Mg2
(Si, O6
),
(рис. 2, а) и пироксеноида волластонита Са3
(Si3
O9
),
(рис. 2, б).

Рис. 1. Элементарный правильный кремне-кислородный тетраэдр SiO4 4-
Для кристаллохимии С. по Белову определяющим критерием конструирования или формирования типа кристаллич. структуры С. и их неорг. аналогов явился принцип «приспособляемости» кремнекислородных анионных группировок к существенно более крупным полиэдрам катионов. При классификации С. выделяют элементарное звено, участвующее в построении кремнекислород-ного![]() анионного каркаса, – орто-, диорто- и триортогруппы.
анионного каркаса, – орто-, диорто- и триортогруппы.

Рис. 2. Элементарные кремнекислородные единицы-ортогруппы![]() в структуре Mg‑пироксена энстатите (а) и диортогруппы
в структуре Mg‑пироксена энстатите (а) и диортогруппы![]() в Са-пироксеноиде волластоните (б).
в Са-пироксеноиде волластоните (б).
В целом С. могут быть подразделены на два класса: соединения с конечными размерами кремнекислородных группировок (островные структуры) и с бесконечными повторениями кремнекислородных тетраэдров при самых разл. способах их сочленения (полимерные, или конденсир., структуры). Причем анионный остов кристаллич. решетки, наряду с кремнекислородными анионами, может включать И дополнит. анионы-О2-
, ОН-
, Cl-
, F-
, ![]() ,
,![]() и нек-рые др.
и нек-рые др.
Островные С. делятся на соед. с одиночными кремнекислородными тетраэдрами – ортосиликаты (рис. 3, а) и со сдвоенными тетраэдрами – диортосиликаты (рис. 3, б). К таким С. относятся оливины (MgFe)2
SiO4
, циркон ZrSiO4
, гранаты ![]() , где МII
= Mg, Ca, Fe(II), Mn(II), МIII
= Al, Fe(III), Сr(III), V(III) и др. Соед. со сдвоенными тетраэдрами-минералы группы тортвейтита Sc2
Si2
O7
, ме-лилита и обширный класс пиросиликатов РЗЭ (рис. 3, б). По сравнению с орто- и диортосиликатами значительно менее распространены С. с открытыми линейными три- и тетраор-тогруппами, напр. киноит Cu2
Ca2
Si3
O10
·2H2
O.
, где МII
= Mg, Ca, Fe(II), Mn(II), МIII
= Al, Fe(III), Сr(III), V(III) и др. Соед. со сдвоенными тетраэдрами-минералы группы тортвейтита Sc2
Si2
O7
, ме-лилита и обширный класс пиросиликатов РЗЭ (рис. 3, б). По сравнению с орто- и диортосиликатами значительно менее распространены С. с открытыми линейными три- и тетраор-тогруппами, напр. киноит Cu2
Ca2
Si3
O10
·2H2
O.
Среди природных и искусственных С. широко распространены соед. с циклич. (замкнутыми) кремнекислородными группировками из трех-, четырех-, шестизвенных (рис. 3, в, г, д) и более сложных (восьми-, девяти-, двенадцатичленных) колец. К данной группе островных метасиликатов относится, напр., псевдоволластонит -Ca3 Si3 O9 (рис. 3, в). В берилле Ве3 Al2 Si6 O18 реализуется шестичленный кольцевой анион (рис. 3, д) с двумя мостиковыми Si‑О–Si связями, приходящимися на каждый тетраэдр, как и в др. циклич. анионах.
Известны кристаллич. структуры островных С. со сдвоенными, конденсированными «двухэтажными» трех-, четырех-и шестизвенными кольцевыми анионами. Напр., в минерале эканите ThK (Ca, Na)2 Si8 O20 реализуется сдвоенный четы-рехзвенный кольцевой анион. Аналогичный кремнекисло-родный анион обнаружен в С. с комплексными катионными группировками, напр. тетраметиламмониевыми в соед. [N(CH3 )4 ]8 Si8 O20 . Сдвоенное «двухэтажное» шестизвенное кольцо обнаружено, в родственном бериллу С. миларите K(Be2 Al) Ca2 Si12 O30 . В «двухэтажных» циклич. кремнекислородных группировках число мостиковых связей на каждый тетраэдр повышается соотв. до трех. Для мн. сложных по составу островных С. характерно сочетание в анионном остове одновременно неск. разл. кремнекислородных группировок, чаще всего орто- и диортогрупп.
Класс полимерных, или конденсированных, С. подразделяют на 4 подкласса. 1) Цепочечные С. с бесконечными цепочками из одиночных кремнекислородных тетраэдров, каждый из к-рых с соседними имеет по две мостиковые связи. Данный структурный тип метасиликатов охватывает большую группу породообразующих минералов и их синте-тич. аналогов, моноклинных и ромбич. пироксенов и пиро-ксеноидов широкого диапазона составов: энстатит (MgFe)2 (Si2 O6 ), диопсид CaMg(Si2 O6 ), сподумен LiAl(Si2 O6 ), волластонит – Са3 (Si3 O9 ), родонит CaMn4 (Si5 Oi5), и мн. др. представители пироксен-пиро-ксеноидных С. (рис. 4) с периодом повторяемости из 2, 3, 5 кремнекислородных тетраэдров и более вдоль оси цепочки.
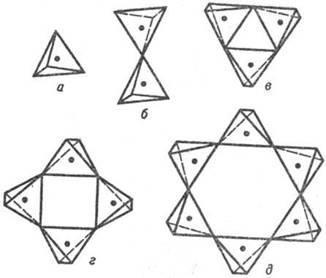
Рис. 3. Простейшие типы островных кремнекислородных анионных группировок: а-SiO4 , б-Si2 O7 , в-Si3 O9 , г-Si4 О12 , д-Si6 O18 .

Рис. 4. Важнейшие типы кремнекислородных цепочечных анионных группировок (по Белову): а-метагерманатная, б – пироксеновая, в-батиситовая, г-вол-ластонитовая, д-власовитовая, е-мелилитовая, ж-родонитовая, з-пирокс-мангитовая, и-метафосфатная, к-фторобериллатная, л – барилитовая.

Рис. 5. Конденсация пироксеновых кремнекислородных анионов в ленточные двухрядные амфиболовые (а), трехрядные амфиболоподобные (б), слоистые тальковые и близкие им анионы (в).

Рис. 6. Структурно-гомологический ряд кремнекислородных анионных группировок ксонотлита (а) и тоберморита (б); волластонит-см. рис. 4, г.
2) С. с ленточными кремнекислородными анионами из двух-, трех- и n‑рядных цепочек, сконденсированных между собой по боковым связям перпендикулярно цепочке (рис. 5). В природе наиб. распространены в данном подклассе в-в амфиболовые и амфиболоподобные асбесты – волокнистые С. с двухрядными ленточными анионами, важнейшие представители – минералы тремолит Ca2 Mg5 (Si8 O22 XOH)2 и роговые обманки (Na, Ca)2 (MgAl)5 (Al, Si)8 O22 (OH)2 . Ленточный анион цементного минерала ксонотлита Ca6 (Si6 O17 ) (OH)2 (рис. 6, а) – продукта конденсации волластонитовых цепочек (рис. 2, б или 4, г) – состоит из восьмичленных колец, в отличие от шестизвенных гексагон. колец амфиболовых лент (рис. 5, а, 6,7).
3) С. с двухмерными слоистыми или листовыми анионами характеризуются широким разнообразием возможных сочленений кремнекислородных тетраэдров в правильные или же в низкосимметричные шести-, четырех- и восьмичленные кольца с тетрагон. и ромбич. симметрией слоя, восьми-, шести- и четырехчленные кольца, воедино связанные в слоистом анионе, и т.д. (рис. 5, в, 6, б).

Рис. 7. Важнейшие типы ленточных кремнекислородных группировок (по Белову): а – силлиманитовая, амфиболовая-см. рис. 5, а, ксонотлитовая-см. рис. 6, а; б-эпидидимитовая; в-ортоклазовая; г-нарсарсукитовая; д-фенаки-товая призматическая; е-эвклазовая инкрустированная.
В прир. – слоистых С. группы слюд (мусковит ![]() , биотит
, биотит![]() тальк, пирофиллит и др.), глинистых
тальк, пирофиллит и др.), глинистых![]() минералов [каолинита Al4
(Si4
O10
) (OH)8
и др.] кремнекислородные сетчатые анионы образованы правильными шестичленными кольцами из тетраэдров SiO4
. Эти сетки являются продуктом конденсации пироксеновых или же амфиболовых лент (рис. 5). Строение слоистых С. предопределяет их отчетливую спайность по базальной плоскости (параллельно слоям), наиб. отчетливо проявляющуюся в слюдах (рис. 8). При конденсации в плоскости волластонитовых цепочек (Si3
О9
),
(рис. 2, б или 4, г) или же ксонотлитовых лент (Si6
O17
),
(рис. 6, а) образуются тетрагон, тоберморитовые сетки Ca5
(Si6
O16
) (OH)2
·4H2
0 (рис. 6, б).
минералов [каолинита Al4
(Si4
O10
) (OH)8
и др.] кремнекислородные сетчатые анионы образованы правильными шестичленными кольцами из тетраэдров SiO4
. Эти сетки являются продуктом конденсации пироксеновых или же амфиболовых лент (рис. 5). Строение слоистых С. предопределяет их отчетливую спайность по базальной плоскости (параллельно слоям), наиб. отчетливо проявляющуюся в слюдах (рис. 8). При конденсации в плоскости волластонитовых цепочек (Si3
О9
),
(рис. 2, б или 4, г) или же ксонотлитовых лент (Si6
O17
),
(рис. 6, а) образуются тетрагон, тоберморитовые сетки Ca5
(Si6
O16
) (OH)2
·4H2
0 (рис. 6, б).
4) К С. каркасного строения относятся многочисл. группы алюмосиликатов (в меньшей степени – боросиликаты), вязаный каркас к-рых образован четырьмя мостиковыми связями и имеет общую ф-лу (Alm Sin _m O2n )m- Избыточный отрицат. заряд анионного остова из (Аl, Si) – теграэдров электростатически компенсируется щелочными и щел.-зсм. катионами, располагающимися в полостях каркасной структуры. Среди каркасных алюмосиликатов более всего в природе распространены щелочные полевошпатовые С.: твердые р-ры альбита NaAlSi3 O8 и ортоклаза KAlSi3 O8 , а также альбита и анортита CaAl2 Si2 O8 , известные под назв. плагиоклазов. Каркасные С. цеолиты характеризуются большими внутр. полостями и входными окнами, в к-рых могут абсорбироваться крупные молекулы диаметром 0,3–0,5 нм и более (рис. 9).

Рис. 8. Фрагмент (элементарный пакет) слоистой кристаллич. структуры мусковита KAl2 (AlSi3 O10 XOH)2 , иллюстрирующий переслаивание алюмокремне-кислородных сеток с полиэдрич. слоями крупных катионов Аl и К.

Рис. 9. Проекция фрагмента пористой кристаллич. структуры цеолита фошазита (фожазита) с широкими входными каналами эллиптич. сечения.
3. Процессы образования силикатов в земной коре
Теперь рассмотрим минеральный состав земной коры с позиций строения кремнекислородных радикалов. За счет внутренней энергии Земли магма – расплав, состоящий из основных пород (ортосиликаты магния и железа и их твердые растворы), поднимаясь по трещинам на поверхность, обогащается кремнеземом, глиноземом, водой. При этом с понижением температуры из него кристаллизуются сначала тугоплавкие минералы, а оставшийся расплав снова взаимодействует с встречающимися на его пути породами, образующиеся кристаллы взаимодействуют с гидротермальными водами. Из образовавшихся растворов выкристаллизовываются минералы, содержащие воду. Безусловно, это очень упрощенная картина сложных геохимических процессов, происходящих в действительности. К основным минералам относятся оливины – ортосиликат магния Mg2SiO4, в котором часть катионов магния может быть замещена на Fe2 +. Поэтому для оливинов принимается общая формула [Mg, Fe] 2 [SiO4], а их структура образована изолированными тетраэдрами [SiO4] 4 -, соединенными между собой катионами. При увеличении содержания SiO2 образуются пироксены – метасиликаты натрия, магния, кальция, железа, содержащие бесконечные метасиликатные цепочки (SiO3)?. В зависимости от природы катиона найдены различные виды изолированных и более сложных цепочек. Минерал жадеит NaAl[Si2O6], о котором шла речь, также относится к группе пироксенов, то есть к минералам с цепочечной структурой. Ионы натрия и алюминия образуют катионную составляющую структуры.
Следующей ступенью полимеризации являются соединения, содержащие ленточные кремнекислородные радикалы. Некоторые виды этих радикалов, зависящие от природы катионов, представлены на рис. 3. Во времена У.Л. Брэгга такие соединения еще не были известны. К ленточным силикатам относятся амфиболы – гидросиликаты Ca, Mg, Fe, содержащие группы [Si4O11] 6 – К амфиболам относится и один из древнейших минералов, используемых человеком, – нефрит – Ca2 (Mg, Fe) [Si4O11] (OH) 2, и асбесты.
Дальнейшая конденсация приводит к образованию слоистых силикатов. К их числу относятся слюды и глины, содержащие в своей структуре группировки [Z4O10], где Z=Si и Al в четверной координации относительно кислорода. В слюдах слои состоят из шестичленных колец, построенных из алюмо- и кремнекислородных тетраэдров. Слоистых силикатов существует множество: слои могут быть построены из пяти- и шестичленных колец (см. рис. 1); состоять из чередующихся в определенном отношении восьми- и пятичленных колец; могут существовать слои, в которых кремнекислородный тетраэдр необязательно имеет три мостиковых атома кислорода, и др.
И наконец, последней ступенью полимеризации являются силикаты с каркасным строением, которых тоже существует великое множество. Примером каркасных силикатов могут служить кремнезем и полевые шпаты. Полевые шпаты делятся на плагиоклазы (непрерывный ряд твердых растворов в системе альбит-анортит (NaAlSi3O8‑CaAl2Si2O8)) и калиевый полевой шпат K[AlSi3O8]. Их структура представляет собой бесконечный объемно-увязанный каркас из тетраэдров SiO4 и AlO4, в пустотах которого расположены ионы Na, Ca, K (рис. 4). Сам же кремнезем – это вязь из кремнекислородных тетраэдров. К разряду каркасных силикатов, но не полевых шпатов относится и упоминаемый ранее минерал лейцит K[AlSi2O6], казалось бы, метасиликат калия и алюминия. В действительности это каркасный алюмосиликат, в котором атомы алюминия выполняют структурную функцию атомов кремния. Каркас состоит из тетраэдров AlO4 и SiO4 (все атомы кислорода мостиковые), в пустотах которого расположены ионы калия. Полевые шпаты, в свою очередь, в результате процессов выветривания превращаются в глины и различные виды кремнезема:
2K[AlSi3O6] + CO2 +2H2O =
= Al2 [Si2O5] (OH) 4 + K2CO3 + SiO2
Каолинит Кварц, опал
Каолинит – минерал со слоистой структурой. Слои состоят из шестичленных кремнекислородных колец. В конечном итоге процессы выветривания полевых шпатов, слюд, талька, нефелина приводят к образованию растворимых солей щелочных и щелочноземельных металлов, плохо растворимых гидратов оксидов железа и алюминия и гидросиликатов, которые переносятся водными растворами и дают начало образованию новых минералов, с которых как бы начинается новый виток образования силикатных минералов.
4. Яркие представители группы силикатов
а) Топаз – полудрагоценный камень, минерал из группы островных силикатов алюминия (Al2 [SiO4 ] (F, OH)2 ). Примеси Fe2+ , Fe3+ , Ti, Cr, V и др. Кристаллизуется в ромбической сингонии, ромбо – дипирамидальный вид симметрии.
Этимология. Название топаз получил по месту первой его находки на острове Топазиос (Топазион) в Красном море, в настоящее время – остров Зеберген, по другой версии – от санскритского слова «топас» – огонь. Синоним – «тяжеловес» (старое название уральских рудокопов, по большому уд. весу)
Свойства. Цветовая гамма топаза разнообразна: от коричнево- и винно-желтого до голубого, розового, золотистого, оранжевого и красновато-оранжевого (редко). Чаще – бесцветный. Встречаются полихромные топазы, когда разные участки или зоны одного кристалла имеют разную окраску (обычно голубой / винно-жёлтый). Твёрдость 8; плотность 3,49–3,6 г/см3 . Спайность совершенная в одном направлении по (001). Излом раковистый. Блеск сильный, стеклянный, на плоскостях спайности – перламутровый. Очень устойчив, в кислотах не растворяется. Разлагается фосфорной солью.
Топаз – один из эталонных минералов для определения относительной твёрдости методом царапанья – шкалы Мооса (минералогической шкалы твердости).
Форма нахождения. Обычен в кристаллах. Кристаллы ромбо-призматические или кроткостолбчатые. Иногда крупные, известны находки кристаллов массой до 60–80 кг и более. Грани призмы обычно немногочисленны, а головки кристаллов бывают весьма разнообразны и богаты гранями. Характерны признаки природного растворения, проявляющиеся в конусовидных и сосковидных формах на головках кристаллов и в углублениях и бороздах в форме отрицательных тетрагональных пирамид на призме. Также параллельно-шестоватые крупнокристаллические сростки, скрытокристаллические «яшмоподобные» образования, лучистые и тонкопластинчатые (пикнит) образования.
Местонахождения.Наибольшее число находок топаза в Ильменском минералогическом заповеднике в России (Урал) приходится на гранитные пегматитовые жилы. В Ильменах обнаружено большое количество пегматитовых жил, в которых встречаются топазы. Знаменитыми во всем мире, особо выдающимися и потому успешно выдерживающими конкуренцию на мировом рынке стали всего пять уральских драгоценных камней и среди них топаз. С открытия топазов началась слава Ильменских гор. В Ильменах топаз встречался не только бесцветный, но и более ценный – голубой. Здесь находили топазы массой до 30 кг. Топазы встречаются на Урале в четырех различных формациях, причем для каждой характерна определенная окраска самоцвета и формы кристаллов. Бесцветные топазы, нередко в виде крупных кристаллов, интенсивно добывались в свое время из друзовых полостей амазонитовых гранитных пегматитов Ильменогорского самоцветного пояса, впервые обнаруженные казаком Прутовым еще в начале XIX века и находящиеся в частной коллекции. Из них добыто несколько тонн прозрачных кристаллов. Наиболее крупные кристаллы топаза имели массу до 10 кг. Обломки кристаллов топаза употреблялись преимущественно как ювелирное сырье. Голубые и желтые топазы характерны для жильных гранитных пегматитов топазо-бериллового типа с друзовыми полостями в Мурзинско-Адуйском самоцветном поясе, ярко-голубые – для сложнопостроенных гранит-пегматитовых тел, и, наконец, малиновые и розовые топазы были встречены только в кварцевых жилках около восточного тектонического шва Кочкарского мегантиклинория на Южном Урале. Суммируя общие перспективы Урала по топазовой минерализации, А.Е. Ферсман в 1925 г. писал: «Россия может гордиться своими топазами, которые по красоте тона, чистоте воды и величине кристаллов занимают исключительное место среди топазов всего света: по качеству русский топаз выделяется среди всех топазов известных месторождений, причем красота нежно-голубого топаза Мурзинки, красновато-фиолетовый тон топазов Санарки и Каменки – всё это составляет гордость русских цветных камней».
Топаз массой в 5 тонн найден в Бразилии. В большом количестве винно-жёлтые и голубые топазы находят на Волынском месторождении (Украина) – в 1965 году в одной из шахт обнаружили винно-желтый кристалл топаза массой 117 кг. В горах Шри-Ланки еще в древности были обнаружены месторождения драгоценных камней топазов.
Отличительные признаки.Спектр окрасок природных (натуральных) топазов необычайно разнообразен – бесцветные, различные оттенки жетовато-коричневого, зеленовато-синего, розового и синего тонов. Характерной особенностью топазов является плеохроизм, заключающийся в изменении окраски кристалла в зависимости от направления света. Это свойство отчетливо проявлено в розовых и винно-желтых топазах, а в голубых – слабо. Обычно кристаллы прозрачны, иногда с облачным эффектом или эффектом «кошачьего глаза».
В ультрафиолетовых лучах длинноволнового диапазона наблюдается свечение (люминесценция) топазов: для голубых кристаллов – зеленоватое или желтоватое; для розовых и коричневых (винных) – оранжево-желтое. В коротковолновом диапазоне люминесценция слабая.
Физические свойства позволяют достаточно легко отличить топаз от многочисленных внешне сходных с ним камней-имитаторов. Так, шпинель и алмаз, не обладающие двулучепреломлением, легко отсортировать с помощью несложного прибора – порярископа. В отличие от топазов под ультрафиолетовой лампой аквамарин вообще не люминесцирует, а гелиодор светится желтым светом только в коротковолновом диапазоне.
Аквамарин, гелиодор и зеленоватый берилл (берилловая группа) и цитрин (кварцевая группа) отличаются от топаза значительно меньшей плотностью, что легко устанавливается путем вычисления массы вставки. В ряде случаев может помочь испытание карандашами твердости. Топаз по твердости значительно превосходит цитрин и циркон, он несколько тверже турмалина, но уступает рубинам, сапфирам и тем более алмазам. Однако следует иметь в виду, что близкую к топазу твердость имеют шпинель, хризоберилл и схожие с ним представители берилловой группы.
Незаменимым прибором при диагностике топазов является рефрактометр, с помощью которого определяют показатели преломления, являющиеся своеобразным паспортом камня. В ряде случаев идентификации может быть проведена по характеру плеохроизма или способности топаза электризоваться. Последнее свойство с успехом позволяет специалисту отличить от топаза все перечисленные выше камни-имитаторы, за исключением турмалина и алмаза.



б) Циркон. С химической точки зрения циркон является силикатом циркония. Название драгоценного камня происходит от персидского слова zargun. В переводе с персидского гаг означает «золото», а gun – «цвет». Следователвно, циркон на этом языке означает «золотоцветный». Помимо наиболее красивых золотисто-желтых и красных цирконов встречаются коричневые, желтовато-зеленые и небесно-голубые камни. Их цвет определяется примесями железа, меди, цинка, кальция, титана и некоторыми редкоземельными элементами.
Встречаются, впрочем, бесцветные и даже черные цирконы. Золотисто-красные камни называют гиацинтами. Согласно древнегреческому мифу. Гиацинт был убит диском, который бросил на состязаниях бог света Аполлон. Упавшие на землю капли крови юноши превратились в цветы гиацинты. Окаменев, они стали драгоценными камнями. В старинных русских рукописях драгоценный камень циркон-гиацинт упоминался как иакинф, иацинт или якинт.
Соломенно-желтые и дымчатые цейлонские цирконы европейские ювелиры не так давно именовали «цейлонскими жаргонами» или просто «жаргонами».
В ювелирном деле нередко используются коричневые цирконы, которые после обжига приобретают великолепной голубой цвет. Такие камни называют старлитами.
Голубовато-зеленые камни являют пример ослепительно-яркой окраски, редко встречаемой у других драгоценных камней. Не лишены великолепия и густо-красные камни, хотя они и несколько мрачноваты, а камни столь красивой золотисто-желтой окраски не дает ни один другой минерал.
Цирконы были давно известны на Цейлоне и нередко попадали в руки посещавших этот солнечный остров путешественников, которые по большей части не понимали, с каким камнем они имеют дело; до тех пор пока на рынке не появились голубые камни, этот минерал в целом не привлекал к себе внимания.
Бесцветные цирконы гранятся главным образом бриллиантовой огранкой. Цветные камни гранят различно в зависимости от назначения, но наиболее обычна смешанная огранка (бриллиантовая огранка верха и ступенчатая низа).
Циркон используется не только в ювелирном деле, но и в промышленности, главным образом как источник циркония и окиси циркония. Металл цирконий применяют при выплавке стали для удаления окислов и нитридов. Окись циркония находит много применений: как огнеупор для облицовки плавильных печей, как составная часть эмалей и как абразив. Собственно минерал циркон также используется иногда как огнеупорный материал.
Бесцветные цирконы, хотя они и характеризуются алмазным блеском и сильной игрой, легко отличить от алмаза по их низкой твердости, двупреломлению (которое достаточно велико и обусловливает раздвоение противоположных ребер ограненного камня при разглядывании их через площадку) и низкому светопреломлению (что позволяет значительной части света, падающего на площадку камня с бриллиантовой огранкой, ускользать из нижней части).
Кроме того, алмаз плавает в жидкости Клеричи. Опытный глаз не спутает зеленый гранат демантоид с цирконом, настолько различны оттенки их окраски. Сомнения можно разрешить, определяя плотность, которая меньше у демантоида.


в) Беломорит. Форма кристаллов. Столбчатые, толстотаблитчатые, распространены полисинтетические двойники.
Кристаллическая структура. Силикат с бесконечным трехмерным каркасом (SiAl) O4 .
Класс симметрии. Триклинно-пинакоидальный – 1.
Спайность. Весьма совершенная по базису (Р), хорошая по концевой грани пинакоида (М) и призме (Г) (см. полевые шпаты).
Агрегаты. Зернистые, плотные.
Беломорит – это полевой шпат – альбит с ирризацией, т.е. переливчатостью, отсветами серо-голубого, сине-голубого или бледно-фиолетового цвета на плоскостях. Назван А. Ферсманом по месту нахождения – на берегу Белого моря. Древних поверий о камне нет, и только авестийская астрология его изучила и признала хорошим средством от бессонницы и камнем ясновидящих
Непрозрачный белый лунный камень с иризацией в серых и сине-голубых тонах, возникающей при отражении света от плоскости спайности под углом 12–15 градусов. Нахождение – микроклин-олигоклазовые гранитные пегматиты мусковитовой формации (гранат, турмалин, апатит, кварц, мусковит).



г) Берилл. В группу бериллов входят изумруд, аквамарин и обычный берилл. Они имеют неоспоримое право на внимание всех любителей драгоценных камней. Несравненный изумруд давно стоит в ряду наиболее дорогих драгоценных камней. Даже Плиний помещал изумруд на третье место, хотя ему были известны только сравнительно плохие камни из Египта и, возможно, с Урала. Брат изумруда, восхитительный аквамарин, который, кажется, попал к нам прямо из скрытой в глубинах теплого моря сокровищницы русалок, обладает чарами, которые нельзя отрицать.
В минералогии название «берилл» прилагается ко всем разновидностям этого минерала, название «изумруд» – к зеленой разности, а «аквамарин» – к разности цвета морской волны. Но в ювелирном деле термин «берилл» имеет более узкий смысл и используется для обозначения светлоокрашенных камней, а также камней, имеющих не зеленую, а другую окраску, так что вошло в обычай говорить о «желтом берилле» или «розовом берилле». В последнее время проводится дальнейшее разграничение понятий, причем для розовых камней используется название «морганит», а для золотисто-желтых – «гелиодор».
Название минерала пришло к нам через латинское beryllus от греческого «бериллос» – древнего слова, значение которого теряется в веках. Возможно, оно с самого начала относилось, по крайней мере частично, к тем же разновидностям этого минерала, которые и сейчас обозначаются этим названием.
Берилл, если иметь в виду название, под которым этот минерал известен науке, является алюмосиликатом бериллия и имеет формулу Be3Al2Si6O18L. Анализы часто показывают присутствие в нем небольших количеств щелочных металлов, а также гелия. Полагают, что атомы этих элементов не входят в кристаллическую решетку содержащего их берилла, а удерживаются в каналах структуры, расположенных параллельно оси симметрии шестого порядка. Алюминий может замещаться небольшими количествами хрома и окисного железа. В изумрудах было обнаружено от 1 до 2% воды. Бериллий, как указывает его название, впервые был открыт в образце минерала берилла в 1798 г. химиком Вок-леном. Одно время он был известен под названием «глициний» (от греческого «глицис» – сладкий) из-за сладкого вкуса его солей. Чистый берилл бесцветен, но благодаря почти неизменному присутствию примесей он приобретает различную окраску. Наиболее часты следующие цвета: зеленый (он столь своеобразен у этой разновидности, что соответствующий оттенок подучил название изумрудно-зеленого), от зеленоватого (цвета морской волны) до голубого у аквамарина, розовый у морганита и желтый. Цвет изумруда обычно обусловлен незначительной примесью хрома. Много лет назад Гольдшмидт обнаружил, что в зеленых норвежских бериллах содержится больше ванадия, чем хрома, и на основании этого факта пришел к выводу, что трехвалентный ванадий может играть в берилле ту же роль, что и хром. С тех пор ванадий был обнаружен в изумрудах из многих месторождений, а в зеленом берилле из Салининхи в бразильском штате Баия ванадий сопровождается заметным количеством железа и лишь следами хрома. Окрашенные одним лишь ванадием зеленые бериллы получены искусственным путем. Предлагалось название «изумруд» использовать лишь для обозначения зеленых бериллов, окрашенных примесью хрома. Такое ограничение понятия «изумруд» было бы полезным для специалистов, причем наличие или отсутствие хрома быстро определялось бы с помощью спектроскопа, но весьма вероятно, что для непрофессионалов изумруд всегда останется «сверкающей зеленой разновидностью берилла». В аквамаринах оттенки цвета, меняющиеся от голубоватого до желтовато-зеленого, обусловлены, по-видимому, главным образом примесью железа. Розоватый оттенок морганита может быть связан с присутствием лития, а с примесью окисного железа обычно связана окраска желтых бериллов.
Гелиодор содержит незначительную примесь урана и поэтому радиоактивен.
Плотность берилла варьирует от 2,67 до 2,90. Таким образом, берилл гораздо плотнее, чем кварц, и если берилл и кварц поместить в трубку с соответственно подобранной тяжелой жидкостью, первый всегда будет скапливаться ниже второго (рис. 74). Плотность колумбийских и сибирских изумрудов колеблется от 2,68 до 2,74, но в среднем равна 2,712. Бразильские бледные изумруды менее плотные, плотность их колеблется от 2,67 до 2,70, а южноафриканские изумруды более плотные, плотность их изменяется от 2,72 до 2,77, но в большинстве случаев значение плотности близко к 2,75. Плотность аквамаринов и желтых бериллов колеблется от 2,68 до 2,75. Бразильский зеленый берилл имеет плотность около 2,80, а морганит имеет самую большую плотность по сравнению с другими разновидностями берилла: от 2,72 до 2,90, в большинстве случаев около 2,82. Эти высокие значения плотности могут быть обусловлены присутствием щелочных металлов – цезия и рубидия. У синтетических изумрудов, которые были получены раньше, плотность и оптические константы были заметно ниже, чем у природных камней, но в искусственных изумрудах, полученных позднее, такое различие отсутствует. Тщательное изучение включений остается одним из лучших методов, позволяющим отличать природные и искусственные камни.
Твердость берилла варьирует от 7,5 до 8, причем изумруд несколько мягче, чем другие разновидности. Отмечается слабая спайность, параллельная базису. Подобно большинству драгоценных камней, берилл весьма хрупок и легко раскалывается и покрывается трещинами. Замутненные, непрозрачные из-за трещинок камни называют моховыми. В пламени паяльной трубки берилл плавится с трудом. Он устойчив к воздействию фтористо-водородной кислоты, а также других кислот.
Непрозрачные бериллы, не находящие применения в ювелирном деле, являются главной рудой для получения металла бериллия, который используется для приготовления специальных сплавов – главным образом с медью, а также с железом и никелем.



д) Везувиан – это минерал, силикат кальция и алюминия сложного состава. Кристаллы везувиана часто имеют столбчатую, призматическую или пирамидальную форму. При этом когда смотришь на достаточно крупные кристаллы везувиана, создается впечатление, что они составлены из соединенных вместе простых геометрических тел – кубиков, словно спаянных, смешанных друг с другом. Отсюда другое название этого минерала, образованное с помощью корней греческого языка, – идокраз (греч. crasys – «смесь»). Под таким именем везувиан известен с 1796 г. Цвет везувиана зеленовато-желтый, бурый, бутылочно-зеленый, изредка изумрудно-зеленый; окраска обусловлена примесью железа, стойкая. В ювелирном деле для огранки и вставок в украшения используются прозрачные образцы коричневого цвета с о. Шри Ланка.
Везувиан получил свое название по месту первой находки – склону вулкана Везувий (Италия). Синонимы: агат стеклянный, везувиан-жад, вилуит, гиацинтин ложный, жад американский, жад везувиановый, идокраз, изумруд вилюйский, калифорнит, нефрит американский, хризолит вулканический, хризолит итальянский, хризолит торговый.
На территории провинции Квебек в Канаде встречаются везувианы ювелирного качества массой 10–15 карат. Везувианы обнаружены также в Норвегии, Италии, Швейцарии, Пакистане и Африке.
За образцами везувиана россиянам не обязательно ехать в Италию или Америку. Начиная с 1914 г., везувианы Урала изучал русский профессор С.М. Курбатов. Результатом этих исследований стала его книга «Везувианы из русских месторождений». В начале 80-х гг. XX в. этот минерал был найден и на склонах «неудавшегося» вулкана Аюдаг в Крыму.



5. Применение и искусственное происхождение силикатов
Без силикатных материалов – различных видов цемента, бетона, шлакобетона, керамики, стекла, покрытий в виде эмалей и глазурей едва ли можно представить себе нашу повседневную жизнь. Масштабы производства силикатных материалов представляются внушительными цифрами.
Наиболее древними силикатными материалами являются керамические, получаемые из глин и их смесей с различными минеральными добавками, обожженными до камневидного состояния. В древнем мире керамические изделия были распространены по всей территории Земли. Со второй половины XIX века и до настоящего времени индустриальная керамическая промышленность неизмеримо расширила выпуск и ассортимент керамики. Универсальную классификацию керамик создать трудно, но можно выделить следующие типы.
1. Благодаря экономичности производства, высоким физико-механическим и художественно-декоративным качествам, керамические материалы широко используются как строительные и декоративные. Это кирпич, пустотелые блоки для стен, перегородок, перекрытий, облицовочные плитки, изразцы, терракотовые и майоликовые детали в архитектуре, канализационные и дренажные трубы.
2. Огнеупорная керамика используется в производстве металлов, цемента, стекла, для кладки высокотемпературных печей, футеровки их внутренних поверхностей.
3. Химически стойкие керамики заменяют или защищают металлы в производствах, связанных с агрессивными средами, например в химической промышленности.
4. Тонкая керамика включает в себя изделия из фарфора и фаянса. К ним относятся бытовая и химическая посуда, художественные изделия, изоляторы разных типов.
Процессы производства керамики многообразны и в общих чертах сводятся к: 1) обработке сырья, 2) приготовлению керамической массы, 3) формованию и сушке массы, 4) обжигу, 5) отделке изделий. В современном производстве эти операции обеспечиваются специальным оборудованием, порой очень сложным, а сами процессы проводятся в оптимальных технологических режимах, разработанных на серьезной научной основе учеными различных профилей.
Примером искусственного силикатного материала является портландцемент, один из наиболее распространенных видов минеральных вяжущих веществ. Цемент используется для связывания строительных деталей при получении массивных строительных блоков, плит, труб и кирпича. Цемент является основой таких широко применяемых строительных материалов, как бетон, шлакобетон, железобетон. Строительство любого масштаба не может существовать без цемента. В школьном курсе по химии даны основные представления о химическом составе и технологии цемента, поэтому остановимся лишь на некоторых уточняющих деталях. Прежде всего цементным клинкером называется продукт обжига смеси глины и известняка, а цементом – мелкоизмельченный клинкер с минеральными добавками, регулирующими его свойства. Цемент применяется в смеси с песком и водой. Его вяжущие свойства обусловлены способностью цементных минералов взаимодействовать с H2O и SiO2 и при этом затвердевать, образуя прочную камневидную структуру. При схватывании цемента происходят сложные процессы: гидратация минералов с образованием гидросиликатов и гидроалюминатов, гидролиз, образование коллоидных растворов и их кристаллизация. Исследования процессов твердения цементного раствора и минералов цементного клинкера сыграли большую роль в становлении науки о силикатах и их технологии.
Заключение
Для того чтобы понять роль силикатов в жизни человека, остановимся сначала на строении земного шара. По современным представлениям земной шар состоит из ряда оболочек. Наружная оболочка Земли, земная кора, или литосфера, образована гранитной и базальтовой оболочками и тонким осадочным слоем. Гранитная оболочка в основном состоит из гранита – плотных сростков из полевых шпатов, слюды, амфиболов и пироксенов, а базальтовая – из таких гранитоподобных, но более тяжелых силикатных пород, как габбро, диабазы и базальты. Осадочные горные породы образуются при разрушении других пород под влиянием условий, характерных для поверхности Земли. Составной частью осадочного слоя являются, в частности, глины, основа которых – силикатный минерал каолинит. Литосфера на 95 мас. % образована силикатами. Ее средняя мощность в области материков составляет 30–40 км. Затем располагается симатическая оболочка, или верхняя мантия, среди минералов которой, вероятно, преобладают силикаты железа и магния. Эта оболочка охватывает земной шар сплошь и распространяется до глубины 1200 км. Далее от 1200 до 2900 км располагается промежуточная оболочка. Ее состав спорен, но и в ней предполагается существование силикатов. Под этой оболочкой на глубине от 2900 до 6370 км находится ядро. В последнее время высказано предположение, что ядро имеет также силикатный состав. При движении от поверхности Земли к ее центру возрастают плотность и основность слагающих пород (увеличивается соотношение между содержанием оксидов металлов и кремнезема), давление и температура.
Древнейшие орудия труда были изготовлены человеком из кремня – плотного агрегата из халцедона, кварца и опала (800–60 тыс. лет до н. э.). Позднее для этого стали использовать яшмы, горный хрусталь, агаты, обсидиан (вулканическое силикатное стекло), нефрит.
Для силикатных минералов нет общепринятой систематики (минералогической номенклатуры), их названия чаще всего происходят от внешнего вида кристаллов, их физических свойств, места нахождения или имени ученого, их открывшего. Плагиоклаз в переводе с греческого означает косо раскалывающийся, а пироксен – тугоплавкий, что отвечает свойствам этих минералов. Минералы кварца в зависимости от природы примесей имеют широкий спектр окраски, которая и определяет их названия: аметист – фиолетовый, цитрин – желтый, горный хрусталь – лед. Модификации кремнезема стишовита и коэсита и минерала биотита произошли от фамилий ученых, их открывших, С.М. Стишова, Л. Коэса и Ж.Б. Био, а минерал каолинит получил свое название от горы Каолинг в Китае, где издавна добывалась глина для производства фарфора.
Природные силикаты и сам кремнезем играют важную роль в качестве сырья и конечных продуктов в промышленных процессах. Алюмосиликаты – плагиоклазы, калиевый полевой шпат и кремнезем используются как сырье в керамической, стекольной и цементной промышленности. Для изготовления несгораемых и обладающих электроизоляционными свойствами текстильных изделий (ткани, шнуры, канаты) широко используются асбесты, относящиеся к гидросиликатам – амфиболам. Некоторые виды асбестов обладают высокой кислотостойкостью и применяются в химической промышленности. Биотиты, представители группы слюд, используются как электро- и теплоизоляционные материалы в строительстве и приборостроении. Пироксены применяются в металлургии и каменно-литейном производстве, а пироксен LiAl[Si2O6] – для получения металлического лития. Пироксены являются составной частью доменных шлаков и шлаков цветной металлургии, которые, в свою очередь, также используются в народном хозяйстве. Такие горные породы, как граниты, базальты, габбро, диабазы, являются прекрасными строительными материалами.
Список используемой литературы
1. Статья «Силикаты в природе и практике человека», М.М. Шульц, Санкт-Петербургский государственный университет.
2. Статья «Основы геологии», авторы: Н.В. Короновский, А.Ф. Якушова, МГУ геологический факультет.
3. Веб-сайт http://www.catalogmineralov.ru
4. Большая Советская Энциклопедия.
5. Интернет-энциклопедия http://ru.wikipedia.org