| Скачать .docx | Скачать .pdf |
Реферат: Роль макрофагов в воспалительном процессе
Содержание
1.Введение
2.Кроветворение
2.1. Эмбриональный гемопоэз
2.2. Постэмбриональный гемопоз
2.3.Регуляция гемопоэза
3. Моноциты
4. Воспаление
4.1. Медиаторы воспаления
4.2. Стадии воспаления
4.2.1. Альтерация
4.2.2. Экссудация
4.2.2.1. Сосудистые реакции и изменение кровообращения
4.2.2.2. Эмиграция лейкоцитов
4.2.2.3. Фагоцитоз
4.2.3. Пролиферация и завершение процесса
5. Монокины
6. Заключение
7. Список литературы
1. Введение
Воспаление является одним из сложнейших процессов часто встречающихся в патологии человека и нередко являющихся причиной многих нарушений жизнедеятельности организма человека и животных.
Воспаление является важной проблемой и предметом изучения всех отраслей медицины и относится к тем феноменам дискуссии о сущности которых на протяжении веков ведут медики, биологи философы. Проблема воспаления стара, как стара и сама медицина.
Однако до сих пор нет единого представления о том, где же место воспаления в биологии, медицине и патологии. Поэтому пока не существует исчерпывающего определения этого процесса.
Но наиболее полным я нахожу именно это определение:
Воспаление – типовой патологический процесс, сформировавшийся в эволюции как защитно-приспособительная реакция организма на воздействие патогенных (флогогенных) факторов, направленная на локализацию, уничтожение и удаление флогогенного агента, а также на устранение последствий его действия и характеризующийся альтерацией, экссудацией и пролиферацией.
В этом реферате я бы хотела посмотреть на воспаление с точки зрения клеточных реакций, в частности, роли лейкоцитов в этом процессе, взаимосвязи между лейкоцитами различных типов.
Как известно, заправилами и регуляторами клеточной миграции, пролиферации, роста сосудов являются моноциты, поэтому, основной акцент в реферате я сделала именно на их роли. Воспаление – типовой патологический процесс, сформировавшийся в эволюции как защитно-приспособительная реакция организма на воздействие патогенных (флогогенных) факторов, направленная на локализацию, уничтожение и удаление флогогенного агента, а также на устранение последствий его действия и характеризующийся альтерацией, экссудацией и пролиферацией.
2. Кроветворение
2.1. Эмбриональный гемопоэз
Кроветворением, или гемопоэзом, называют развитие крови. Различают эмбриональный гемопоэз, который происходит в эмбриональный период и приводит к развитию крови как ткани, и постэмбриональный гемопоэз, который представляет собой процесс физиологической регенерации крови.
Развитие эритроцитов называют эритропоэзом, развитие гранулоцитов — гранулоцитопоэзом, тромбоцитов — тромбоцитопоэзом, моноцитов — моноцитопоэзом, развитие лимфоцитов и иммуноцитов — лимфоцито- и иммуноцитопоэзом.
Эмбриональный гемопоэз
В развитии крови как ткани в эмбриональный период можно выделить 3 основных этапа, последовательно сменяющих друг друга – мезобластический, гепатолиенальный и медуллярный.
Первый, мезобластический этап – это появление клеток крови во внезародышевых органах, а именно в мезенхиме стенки желточногомешка, мезенхиме хориона и стебля. При этом появляется первая генерация стволовых клеток крови (СКК). Мезобластический этап протекает с 3-й по 9-ю неделю развития зародыша человека.
Второй, гепатолиенальный этап начинается с 5—6-й недели развития плода, когда печень становится основным органом гемопоэза, в ней образуется вторая генерация стволовых клеток крови. Кроветворение в печени достигает максимума через 5 мес и завершается перед рождением. СКК печени заселяют тимус, селезенку и лимфатические узлы.
Третий, медуллярный (костномозговой) этап — это появление третьей генерации стволовых клеток крови в красном костном мозге, где гемопоэз начинается с 10-й недели и постепенно нарастает к рождению. После рождения костный мозг становится центральным органом гемопоэза.
Рассмотрим подробнее особенности гемопоэза в стенке желточного мешка, в печени, в тимусе, селезенке, лимфатических узлах и в костном мозге.
Кроветворение в стенке желточного мешка
В мезенхиме стенки желточного мешка обособляются зачатки сосудистой крови, или кровяные островки. В них мезенхимные клетки округляются, теряют отростки и преобразуются в стволовые клетки крови. Клетки, ограничивающие кровяные островки, уплощаются, соединяются между собой и образуют эндотелиальную выстилку будущего сосуда. Часть стволовых клеток дифференцируется в первичные клетки крови (бласты). Большинство первичных кровяных клеток митотически делится и превращается в первичные эритробласты, характеризующиеся крупным размером – мегалобласты. Это превращение совершается в связи с накоплением эмбрионального гемоглобина (HbF) в цитоплазме бластов. В некоторых первичных эритробластах ядро подвергается кариорексису и удаляется из клеток, в других ядро сохраняется. В результате образуются безъядерные и ядросодержащие первичные эритроциты, отличающиеся большим размером по сравнению с нормоцитами и поэтому получившие название мегалоцитов. Такой тип кроветворения называется мегалобластическим. Он характерен для эмбрионального периода, но может появляться в постнатальном периоде при некоторых заболеваниях.
Наряду с мегалобластическим в стенке желточного мешка начинается нормобластическое кроветворение, при котором из бластов образуются вторичные эритробласты, из которых образуются вторичные эритроциты (нормоциты).
Развитие эритроцитов в стенке желточного мешка происходит внутри первичных кровеносных сосудов, т.е. интраваскулярно. Одновременно экстраваскулярно из бластов, расположенных вокруг сосудистых стенок, дифференцируется небольшое количество гранулоцитов — нейтрофилов и эозинофилов.
Часть СКК остается в недифференцированном состоянии и разносится током крови по различным органам зародыша, где происходит их дальнейшая дифференцировка в клетки крови или соединительной ткани. После редукции желточного мешка основным кроветворным органом временно становится печень.
Кроветворение в печени
Печень закладывается примерно на 3—4-й неделе эмбриональной жизни, а с 5-й недели она становится центром кроветворения. Кроветворение в печени происходит экстраваскулярно, - по ходу капилляров, врастающих вместе с мезенхимой внутрь печеночных долек. Источником кроветворения в печени являются стволовые клетки крови, из которых образуются бласты, дифференцирующиеся во вторичные эритроциты.
Одновременно с развитием эритроцитов в печени образуются зернистые лейкоциты, главным образом нейтрофильные и эозинофильные.
Кроме гранулоцитов, в печени формируются гигантские клетки — мегакариоциты, - предшественники тромбоцитов. К концу внутриутробного периода кроветворение в печени прекращается.
Кроветворение в тимусе
Тимус закладывается в конце 1-го месяца внутриутробного развития, и на 7—8-й неделе его эпителий начинает заселяться стволовыми клетками крови, которые дифференцируются в лимфоциты тимуса. Увеличивающееся число лимфоцитов тимуса дает начало T-лимфоцитам, заселяющим T-зоны периферических органов иммунопоэза.
Кроветворение в селезенке
Закладка селезенки также происходит в конце 1-го месяца эмбриогенеза. Из вселяющихся сюда стволовых клеток происходит экстраваскулярное образование всех видов форменных элементов крови, т.е. селезенка в эмбриональном периоде представляет собой универсальный кроветворный орган. Образование эритроцитов и гранулоцитов в селезенке достигает максимума на 5-м месяце эмбриогенеза. После этого в ней начинает преобладать лимфоцитопоэз.
Кроветворение в лимфатических узлах
Первые закладки лимфоузлов человека появляются на 7—8-й неделе эмбрионального развития. Большинство лимфатических узлов развивается на 9—10-й неделе. В этот же период начинается проникновение в лимфатические узлы стволовых клеток крови, из которых на ранних стадиях дифференцируются эритроциты, гранулоциты и мегакариоциты. Однако формирование этих элементов быстро подавляется образованием лимфоцитов, составляющих основную часть лимфатических узлов.
Появление единичных лимфоцитов происходит уже в течение 8—15-й недели развития, однако массовое «заселение» лимфатических узлов предшественниками T- и B-лимфоцитов начинается с 16-й недели, когда формируются посткапиллярные венулы, через стенку которых осуществляется процесс миграции клеток. Из клеток-предшественников дифференцируются сначала лимфобласты (или большие лимфоциты), а далее средние и малые лимфоциты. Дифференцировка T- и B-лимфоцитов происходит, соответственно, в T- и B-зависимых зонах лимфатических узлов.
Кроветворение в костном мозге
Закладка костного мозга осуществляется на 2-м месяце эмбрионального развития. Первые гемопоэтические элементы появляются на 12-й неделе развития; в это время основную массу их составляют эритробласты и предшественники гранулоцитов. Из СКК в костном мозге формируются все форменные элементы крови, развитие которых происходит экстраваскулярно. Часть СКК сохраняется в костном мозге в недифференцированном состоянии. Они могут расселяться по другим органам и тканям и являться источником развития клеток крови и соединительной ткани.
Таким образом, костный мозг становится центральным органом, осуществляющим универсальный гемопоэз, и остается им в течение постнатальной жизни. Он обеспечивает стволовыми кроветворными клетками тимус и другие гемопоэтические органы.
2.2. Постэмбриональный гемопоэз
Постэмбриональный гемопоэз представляет собой процесс физиологической регенерации крови, который компенсирует физиологическое разрушение дифференцированных клеток. Он подразделяется на миелопоэз и лимфопоэз.
Миелопоэз происходит в миелоидной ткани, расположенной в эпифизах трубчатых и полостях многих губчатых костей. Здесь развиваются эритроциты, гранулоциты, моноциты, тромбоциты, а также предшественники лимфоцитов. В миелоидной ткани находятся стволовые клетки крови и соединительной ткани. Предшественники лимфоцитов постепенно мигрируют и заселяют тимус, селезенку, лимфоузлы и некоторые другие органы.
Лимфопоэз происходит в лимфоидной ткани, которая имеет несколько разновидностей, представленных в тимусе, селезенке, лимфоузлах. Она выполняет функции образования T- и B-лимфоцитов и иммуноцитов (например, плазмоцитов).
Миелоидная и лимфоидная ткани являются разновидностями соединительной ткани, т.е. относятся к тканям внутренней среды. В них представлены две основные клеточные линии — клетки ретикулярной ткани и гемопоэтические клетки.
Ретикулярные, а также жировые, тучные и остеогенные клетки вместе с межклеточным веществом формируют микроокружение для гемопоэтических элементов. Структуры микроокружения и гемопоэтические клетки функционируют в неразрывной связи друг с другом. Микроокружение оказывает воздействие на дифференцировку клеток крови (при контакте с их рецепторами или путем выделения специфических факторов).
Таким образом, для миелоидной и всех разновидностей лимфоидной ткани характерно наличие стромальных и гемопоэтических элементов, образующих единое функциональное целое.
СКК относятся к самоподдерживающейся популяции клеток. Они редко делятся. Выявление СКК стало возможным при применении метода образования клеточных колоний – потомков одной стволовой клетки.
Пролиферативную активность СКК регулируют колониестимулирующие факторы (КСФ), различные виды интерлейкинов (ИЛ-3 и др.). Каждая СКК в эксперименте или лабораторном исследовании образует одну колонию и называется колониеобразующей единицей (сокращенно КОЕ, CFU).
Исследование клеточного состава колоний позволило выявить две линии их дифференцировки. Одна линия дает начало мультипотентной клетке — родоначальнице гранулоцитарного, эритроцитарного, моноцитарного и мегакариоцитарного рядов гемопоэза (сокращенно КОЕ-ГЭММ). Вторая линия дает начало мультипотентной клетке — родоначальнице лимфопоэза (КОЕ-Л).
Из мультипотентных клеток дифференцируются олигопотентные (КОЕ-ГМ) и унипотентные родоначальные клетки. Методом колониеобразования определены родоначальные унипотентные клетки для моноцитов (КОЕ-М), нейтрофильных гранулоцитов (КОЕ-Гн), эозинофилов (КОЕ-Эо), базофилов (КОЕ-Б), эритроцитов (БОЕ-Э и КОЕ-Э), мегакариоцитов (КОЕ-МГЦ), из которых образуются клетки-предшественники. В лимфопоэтическом ряду выделяют унипотентные клетки — предшественницы для B-лимфоцитов и для T-лимфоцитов. Полипотентные (плюрипотентные и мультипотентные), олигопотентные и унипотентные клетки морфологически не различаются.
Все приведенные выше стадии развития клеток составляют четыре основных класса, или компартмента, гемопоэза:
- I класс — СКК - стволовые клетки крови (плюрипотентные, полипотентные);
- II класс — КОЕ-ГЭММ и КОЕ-Л - коммитированные мультипотентные клетки (миелопоэза или лимфопоэза);
- III класс — КОЕ-М , КОЕ-Б и т.д. - коммитированные олигопотентные и унипотентные клетки;
- IV класс — клетки-предшественники (бласты , напр.: эритробласт, мегакариобласт и т.д.).
Сразу отметим, что оставшиеся два класса гемопоэза составляют созревающие клетки (V класс) и зрелые клетки крови (VI класс).
Эритропоэз у млекопитающих и человека протекает в костном мозге в особых морфофункциональных ассоциациях, получивших название эритробластических островков. Эритробластический островок состоит из макрофага, окруженного одним или несколькими кольцами эритроидных клеток, развивающихся из унипотентной КОЕ-Э, вступившей в контакт с макрофагом. КОЕ-Э и образующиеся из нее клетки (от проэритробласта до ретикулоцита) удерживаются в контакте с макрофагом его рецепторами.
У взрослого организма потребность в эритроцитах обычно обеспечивается за счет усиленного размножения эритробластов. Но всякий раз, когда потребность организма в эритроцитах возрастает (например, при потере крови), эритробласты начинают развиваться из предшественников, а последние — из стволовых клеток.
В норме из костного мозга в кровь поступают только эритроциты и ретикулоциты.
Моноцитопоэз – процесс образования моноцитов, протекает в красном костном мозге и описывается последовательностью:
СКК -> КОЕ –ГЭММ -> КОЕ-ГМ -> КОЕ-М -> монобласт -> промоноцит -> моноцит
Промоноцит – сравнительно крупная клетка (диаметром 12-18 мкм) с большим светлым ядром, в котором располагается 1-2 ядрышка. Базофильная цитоплазма содкржит умеренно развитую грЭПС, полисомы, митохондрии, центриоли и крупный комплекс Гольджи, от которого отделяются незрелые азурофильные гранулы. Промоноциты делятся и постепенно дифференцируются в моноциты.
Моноциты покидают костный мозг вскоре после формирования, не образуя резервного костномозгового пула. Выделяясь в синусы костного мозга, они попадают в кровь, в которой циркулируют от 8ч до 3-4 суток, а затем через стенку сосудов мигрируют в ткани. Лишь около 5% моноцитов циркулируют в крови, остальные находятся во внесосудистом пуле. В тканях они превращаются в различные виды макрофагов и в дендритные антиген – представляющие клетки.
2.3.Регуляция гемопоэза
Кроветворение регулируется:
- факторами роста, обеспечивающими пролиферацию и дифференцировку СКК и последующих стадий их развития,
- факторами транскрипции, влияющими на экспрессию генов, определяющих направление дифференцировки гемопоэтических клеток,
- витаминами, гормонами.
Факторы роста включают колониестимулирующие факторы (КСФ), интерлейкины и ингибирующие факторы. Они являются гликопротеинами, действующими и как циркулирующие гормоны, и как местные медиаторы, регулирующие гемопоэз и дифференцировку специфических типов клеток. Почти все факторы роста действуют на СКК, КОЕ, коммитированные и зрелые клетки. Однако отмечаются индивидуальные особенности действия этих факторов на клетки-мишени.
КСФ действуют на специфические клетки или группы клеток на различных стадиях дифференцировки. Например, фактор роста стволовых клеток влияет на пролиферацию и миграцию СКК в эмбриогенезе. В постнатальном периоде на гемопоэз оказывают влияние несколько КСФ, среди которых наиболее изучены факторы, стимулирующие развитие гранулоцитов и макрофагов (ГМ-КСФ, Г-КСФ, М-КСФ), а также интерлейкины.
Большинство указанных факторов выделено и применяется для лечения различных болезней. Для получения их используются биотехнологические методы.
Дифференцировка полипотентных клеток в унипотентные определяется действием ряда специфических факторов, поэтинов — эритропоэтинов (для эритробластов), гранулопоэтинов (для миелобластов), лимфопоэтинов (для лимфобластов), тромбопоэтинов (для мегакариобластов).
Большая часть эритропоэтина образуется в почках. Его образование регулируется содержанием в крови кислорода, которое зависит от количества циркулирующих в крови эритроцитов. Снижение числа эритроцитов и соответственно парциального давления кислорода, является сигналом для увеличения продукции эритропоэтина. Эритропоэтин действует на чувствительные к нему КОЕ-Э, стимулируя их пролиферацию и дифференцировку, что в конечном итоге приводит к повышению содержания в крови эритроцитов.
Тромбопоэтин синтезируется в печени, стимулирует пролиферацию КОЕ-МГЦ, их дифференцировку и образование тромбоцитов.
Ингибирующие факторы дают противоположный эффект, т.е. тормозят гемопоэз; их недостаток может быть одной из причин лейкемии, характеризующейся значительным увеличением числа лейкоцитов в крови. Выделен ингибирующий лейкемию фактор (ЛИФ), который тормозит пролиферацию и дифференцировку моноцитов-макрофагов.
Витамины необходимы для стимуляции пролиферации и дифференцировки гемопоэтических клеток. Витамин В12 поступает с пищей и соединяется с внутренним фактором (Касла), который синтезируется париетальными клетками желудка. Образуемый при этом комплекс, в присутствии ионов Са2+, соединяется с рецепторами эпителиоцитов подвздошной кишки и всасывается. При всасывании в эпителиоциты поступает лишь витамин В12, а внутренний фактор освобождается. Витамин В12 поступает с кровью в костный мозг, где влияет на гемопоэз, и в печень, где может депонироваться. Нарушение процесса всасывания при различных заболеваниях желудочно-кишечного тракта может служить причиной дефицита витамина В12 и нарушений в гемопоэзе.
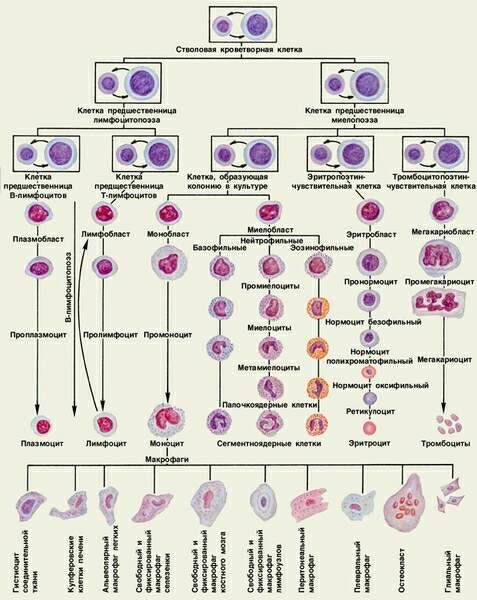
3. Моноциты
Моноциты - наиболее крупные (12-20 мкм) клетки крови. Форма ядра разнообразная, от круглой до неправильной с многочисленными выступами и углублениями поверхности. Хроматиновая сеть в ядре имеет рыхлое строение. Моноциты обладают резко выраженной способностью к окрашиванию, амебойдному движению и фагоцитозу, особенно остаток клеток, чужеродных мелких тел и т. д.
Моноциты составляют от 2 до 10 % всех лейкоцитов, способны к амебовидному движению, проявляют выраженную фагоцитарную и бактерицидную активность. Они фагоцитируют до 100 микробов, в то время как нейтрофилы - лишь 20-30. Моноциты появляются в очаге воспаления после нейтрофилов и проявляют максимум активности в кислой среде, в которой нейтрофилы теряют свою активность. В очаге воспаления моноциты фагоцитируют микробы, а также погибшие лейкоциты, поврежденные клетки воспаленной ткани, очищая очаги воспаления и подготавливая его для регенерации. За эту функцию моноциты называют дворниками организма.
Моноциты - самая большая клетка крови диаметром около 15 мкм. Поверхность ворсинчатая или гофрированная. У эмбрионов моноцит является первой клеткой, образующейся в желточном мешке. Выход моноцитов в кровь осуществляется около 72 часов. Общее количество циркулирующих моноцитов составляет 2 - 10% от всей популяции лейкоцитов. При этом только около 1% моноцитов крови пролиферируют и обладают выраженной фагоцитарной активностью.
Некоторые моноциты покидают кровь случайными, невыясненными путями, а большинство - путем адгезии на стенках синусов в печени, селезенке и железах внутренней секреции. Данная популяция моноцитов взаимодействует с подлежащими эпителиальными клетками и является идеальным "стражем" этих органов от патогенов. Моноциты проходят стенку капилляров путем диапедеза и устремляются в очаги поражения.
При переходе моноцитов из крови в ткани, большая их часть подвергается апоптозу, вследствие отсутствия в тканевом микроокружении необходимых факторов защиты от апоптоза.
Моноциты трансформируются в макрофаги, увеличиваясь в размерах в 5-10 раз, диаметром 25-50 мкм. Клетки с большим количеством ламеллоподий и микроворсинок. При этом резко возрастает фагоцитарная активность, снижается содержание гидролитических ферментов в лизосомах, уменьшается количество митохондрий. В тканях резидентные макрофаги могут находиться до нескольких месяцев и вынуждены выбирать между двумя возможностями: либо стать "фиксированными", либо вновь трансформироваться в блуждающую клетку.
Моноциты, составляющие около 5% лейкоцитов крови, находятся в циркуляции около 1 сут., а затем поступают в ткани, формируя популяцию тканевых макрофагов, количество которых в 25 больше, чем моноцитов. К ним относятся купферовские клетки печени, микроглия центральной нервной системы, остеокласты костной ткани, макрофаги легочных альвеол, кожи и других тканей. Много макрофагов во всех органах иммунной системы. Тканевые макрофаги - клетки с округлым или почковидным ядром имеют диаметр 40-50 мкм. Цитоплазма содержит лизосомы с набором гидролитических ферментов, обеспечивающих переваривание любых органических веществ и выделение бактерицидного аниона кислорода. Макрофаги функционируют как фагоциты. Они продуцируют растворимые вещества, регулирующие другие клетки иммунной системы, из которых наиболее изучен ИЛ-1, активирующий лимфоциты. На мембране макрофага экспрессированы структуры, обеспечивающие способность отличать чужеродные субстраты от собственных. Маркер макрофага - белок СОН служит рецептором липополисахаридов бактерий. Макрофаг обладает пектиноподобными молекулами, соединяющимися с маннозными и фруктозными компонентами поверхности большинства микроорганизмов, что обеспечивает их контакты, лежащие в основе фагоцитоза. Участие макрофага в иммунном ответе состоит в том, что эта клетка фагоцитирует антиген-содержащие частицы, дезинтегрирует их, превращая белки в антигенные пептидные фрагменты. Последние в комплексе с собственными антигенами МНС II класса макрофаг передает Т-лимфоциту при прямом контакте с ним. При этом макрофаг продуцирует лимфокин ИЛ-1, который вызывает пролиферацию лимфоцитов, вступивших в контакт с антигенов что обеспечивает формирование клона этих клеток, осуществляющий развитие иммунологической реакции на антиген.
Дендритные клетки составляют вторую группу АПК. Они близки к макрофагам, но не обладают фагоцитирующими свойствами. Э способствует сохранности поглощенных антигенов, которые могут быть полностью разрушены в ходе фагоцитоза. Дендритные клетки содержатся в крови, лимфе и во всех других тканях. Дендритные клетки эпителиальных тканей называют клетками Лангерганса, в лимфатических узлах и селезенке они составляют около 1 % всех клетов. Эти отростчатые мононуклеарные клетки в разных тканях имеют ней одинаковую форму и даже названия, однако все они обладают молекулами МНС II класса и способностью фиксировать антигены с формированием комплекса антиген-продукт МНС, представляемого Т-лимфоцитам.
Дендритные клетки значительно более активны, чем макрофаги и В-клетки в индукции первичного иммунного ответа: в отличие от других АПК дендритные клетки могут представлять антиген покоящимся Т-лимфоцитам. Захват антигена дендритными клетками чаще всего происходит вне лимфоидных органов. После этого они мигрируют в лимфоидные образования, где происходит их контакт с Т-лимфоцитами и развитие дальнейших событий иммунного ответа. Этому способствуют стимулирующие воздействия на лимфоцит через контакт молекул В7-1 и ИЛ-2, экспрессированных на поверхности дендритных клеток, с молекулами CD40, находящимися на поверхности Т-лимфоцита. Дендритные клетки, как и большинство других клеток человека, обладают антигеном МНС I класса, необходимого для представления антигена CD8+ цитотоксическому Т-лимфоциту. Поэтому они являются также инициаторами цитотоксических реакций. Макрофаги быстро "расползаются" по организму в ответ на инфекцию, травму или поступление пищи. В кислой среде макрофаги обладают большей активностью, чем нейтрофилы.В целом моноциты и макрофаги образуют жесткую устойчивую систему, часто называемую мононуклеарно-фагоцитарной системой или РЭС (ретикулоэндотелиальной системой).
4.Воспаление
4.1. Медиаторы воспаления
Известно, что разнообразные по происхождению повреждающие факторы вызывают во многом стереотипный в своих проявлениях процесс, включающий местные изменения в виде альтерации тканей и составляющих их клеток, высвобождения физиологически активных веществ (так называемых медиаторов воспаления), что влечет за собой реакцию сосудов микроциркуляторного русла, повышения проницаемости стенок капилляров и венул, изменения реологических свойств крови, и ведет к экссудации и пролиферации. Такая неспецифичность изменения тканей при воздействии различных повреждающих факторов связана с реализацией их влияния через общий механизм, который и формирует основные проявления В.
Установлено, что динамика воспалительного процесса, закономерный характер его развития в большей мере обусловлен комплексом физиологически активных веществ образующихся в очаге повреждения и опосредующих действие флогогенных факторов, получивших название медиаторов воспаления.
К настоящему времени обнаружено большое количество таких медиаторов, являющихся посредниками в реализации действия агентов, вызывающих воспаление. Высвобождаясь под воздействием повреждающего агента, медиаторы изменяют самые разнообразные процессы происходящие в тканях – тонус сосудов, проницаемость их стенок, эмиграцию лейкоцитов и других форменных элементов крови, их адгезию и фагоцитарную активность, вызывают боль и т.д.
Существуют различные походы к систематизации медиаторов воспаления. Их классифицируют по химической структуре, например , билогенные амины (гистамин, серотонин), полипептиды (брадикинин, каллидин, метиониллизилбрадикинин) и белки (компоненты системы комплемента, лизосомальные ферменты, катионные белки гранулоцитарного происхождения, монокины, лимфокины), производные полиненасыщенных жирных кислот (простагландины, тромбоксаны, лейкотриены).
По происхождению медиаторы разделяют на клеточные (гистамин, серотонин, гранулоцитарные факторы, монокины, лимфокины) и гуморальные или плазменные (С3 и С5 фракции комплемента, анафилотоксин, факторы свертывающей системы крови, некоторые кинины).
Гуморальные медиаторы обычно характеризуются генерализванными эффектами и спектр их действия шире, чем клеточных медиаторов, эффекты котрых во многом локальны. В свою очередь клеточные медиаторы могут быть разделены по виду клеток, высвобождающих медиаторы воспаления (факторы полиморфно-ядерных лейкоцитов, монокины, лимфокины). Медиаторы воспаления по особенностям их выхода из клеток можно классифицировать на медиаторы нецитотоксического и цитотоксического высвобождения. В первом случае отмечается стимулированный через соответствующий рецептор клетки выход медиаторов путем физиологического экзоцитоза, во втором – происходит разрушение клетки, в результате чего медиаторы выходят из нее в окружающую среду. Один и тот же медиатор (гистамин или серотонин) может поступать в нее и тем и другим путем (из либроцита или тромбоцита).
В зависимости от скорости включения в процесс воспаления различают медиаторы немедленного (кинины, анафилатоксины) и замедленного (монокины, лимфокины) типа действия. Выделяют также медиаторы непосредственного, или непрямого, действия. К первым относят медиаторы, которые в процессе самого раздражителя (гистамин, серотонин и др.), ко вторым – медиаторы, появляющиеся позднее, часто в результате действия первых медиаторов (фракции комплемента, гранулоцитарные факторы полиморфно-ядерных лейкоцитов).
Разделение медиаторов воспаления на группы в известной мере условно. При разделении медиаторов воспаления на гуморальные и клеточные не учтено функциональное и структурное единство гуморальных и клеточных механизмов защиты организма от повреждающих воздействий. Так гуморальный медиатор брадикинин или фракции С3 и С5 – комплемента высвобождающиеся в плазме крови и действующие как медиаторы воспаления, стимулируют лаброциты, высвобождая клеточных медиатор гистамин.
Основные клеточные и гуморальные медиаторы воспаления
| Название | Действие | Происхождение |
| 1 | 2 | 3 |
| Гистамин | Действует через мембранные Н1 и Н2 -рецепторы, увеличивает образование простагландинов Е2 и F2 a , тромбоксана, вызывает вазодилатацию (расширение прекапиллярных артериол) и повышение проницаемости стенки сосудов, подавляет хемотаксис и фагоцитарную активности нейтрофилов, угнетает активность лимфоцитов и выработку лимфокинов. | Лаброциты, базофильные лейкоциты. |
| Серотонин | Реализует свое действие через серотониненгические рецепторы; вызывает сужение посткапиллярных венул, увеличение проницаемости стенки сосудов, боль, зуд и тромбообразование. | Тромбоциты, лаброциты, клетки системы АРUD. |
| Кинины (брадикинин, каллидин, метиониллизилбрадикинин). | Эффекты те же, что и биогенных аминов, однако их действие доминирует на поздних стадиях воспаления. | a2 -глобулин плазмы крови. |
| Компоненты системы комплемена (С3а , С5а ). | Вызывают выделение гистамина, повышают проницаемость сосудистой стенки, обладают опсонизирующим действием, стимулируют хемотаксис полиморфноядерных лейкоцитов. | Система сывороточных белков. |
| Катионные белки гранулоцитарного происхождения. | Активируют освобождение гистамина из лаброцитов, повышают проницаемость сосудистой стенки, вызывают, оказывают бактерицидное действие. | Нейтрофильные гранулоциты. |
| 1 | 2 | 3 |
| Монокины (ИЛ-1, колониестимулирующий фактор, интерферон, фактор хемотаксиса лимфоцитов и др.). | Вызывают эмиграцию лейкоцитов, активируют синтез простагландинов и ФАТ эндотелиальными клетками, увеличивают адгезивность эндотелия, активируют тромбообразование, обладают выраженной пирогенной активностью. | Макрофаги, моноциты. |
| Лимфокины. | Регулируют способность макрофакгов к миграции. Активируют макрофагальный фагоцитоз и киллинг. Влияют на хемотаксис нейтрофилов и эозинофилов. | Лимфоциты. |
| Простагландины (ПГЕ, ПГI2 ). | Вызывают вазодилятацию, увеличивают проницаемость сосудистой стенки, стимулируют эмиграцию гранулоцитов, препятствуют тромбообразованию, оказывают фибринолитическое действие. | Полиненасыщенные жирные кислоты фосфолипидов мембран и плзмы крови. |
| Лейкотриены (ЛТВ4 и др.). | Увеличивают проницаемость сосудистой стенки, стимулируют эмиграцию лейкоцитов. | Нейтрофилы, эозинофилы, Т-лимфоциты, лаброциты. |
| Тромбоксаны | Вызывают вазоконстрикцию, стимулируют тромбообразование, способствуют агрегации клеток крови. | |
| Лизосомальные ферменты (эстеразы, кислые гидролазы). | Вторичная альтерация. Способствуют вазодилятации, повышению проницаемости сосудов, развитию отека и эмиграции лейкоцитов, микротромбообразованию. | Нейтрофильные гранулоциты, клетки поврежденных тканей. |
4.2. Стадии воспаления
4.2.1. Альтерация
Патогенетическую основу воспаления составляют три компонента, стадии – альтерация, экссудация и пролиферация. Они тесно взаимосвязаны между собой, взаимно дополняют и переходят друг в друга, между ними нет четких границ. Поэтому в зависимости от процесса, преобладающего на определенном этапе воспаления, выделяют следующие стадии.
I. Стадия альтерации (повреждения).
А. Первичная альтерация.
Б. Вторичная альтерация.
II. Стадия экссудации и эмиграции.
III. Стадия пролиферации и репарации.
А. Пролиферации.
Б. Завершение воспаления.
В. всегда начинается с повреждения ткани, комплекса обменных, физико-химических и структурно-функциональных изменений, т.е. альтерации (от лат. аlteratio - изменение). Альтерация – начиная, пусковая стадия В.
Первичная альтерация – это совокупность изменений обмена веществ, физико-химических свойств, структуры и функции клеток и тканей под влиянием прямого воздействия этиологического фактора В. Первичная альтерация как результат взаимодействия этиологического фактора с организмом сохраняется и служит причиной воспаления и после прекращения этого взаимодействия. Реакция первичной альтерации как бы пролонгирует действие причины В. Сам причинный фактор уже может не контактировать с организмом.
Вторичная альтерация – возникает под воздействием флогогенного раздражителя, так и факторов первичной альтерации. Если первичная альтерация является результатом непосредственного действия воспалительного агента, то вторичная не зависит от него и может продолжаться и тогда, когда этот агент уже не оказывает влияния (например, при лучевом воздействии). Этиологический фактор явился инициатором, пусковым механизмом процесса, а далее В. будет протекать по законам, свойственным ткани, органу, организму в целом.
Действие флогогенного агента проявляется прежде всего на клеточных мембранах, в том числе на лизосомах. Это имеет далеко идущие последствия, так как при повреждении лизосом освобождаются заключенные в них ферменты (кислые гидролазы), способные расщеплять различные вещества, входящие в состав клетки (белки, нуклеиновые кислоты, углеводы, липиды). Далее эти ферменты, при наличии этиологического фактора или уже без него, продолжают процесс альтерации, а также деструкции, в результате чего образуются продукты ограниченного протеолиза, липолиза, биологически активные вещества – медиаторы воспаления. По этой причине лизосомы называют еще “стартовой площадкой” воспаления. Можно сказать, что первичная альтерация – это повреждение, нанесенное со стороны, а вторичная альтерация – это самоповреждение.
Стадию альтерации следует рассматривать как диалектическое единство изменений вызванных действием повреждающих факторов и ответных защитных местных реакций организма на эти изменения. Различают биохимическую и морфологическую фазы альтерации. Для начала В. прежде всего имеют значение характер и выраженность биохимических и физико-химических изменений в зоне повреждения тканей, нарушения обмена веществ.
Изменения обмена веществ при развитии альтерации, в процессе В. включают в себя интенсификацию процесса распада углеводов, жиров и белков (результат воздействия лизосомных гидролаз и т.д.), усиление анаэробного гликолиза и тканевого дыхания, разобщение процессов биологического окисления, снижение активности анаболических процессов. Следствием указанных изменений являются увеличение теплопродукции, развитие относительного дефицита макроэргов, накопления a-кетоглютаровой, яблочной, молочной кислот, низкомолекулярных полисахаридов, полипептидов, свободных аминокислот, кетоновых тел.
Для характеристики метаболизма при В. издавна применяется термин “пожар обмена”. Аналогия состоит не только в том, что обмен веществ в очаге В. резко повышен, но и в том, что “горение” происходит не до конца, а с образованием недоокисленных продуктов обмена.
В. всегда начинается с усиления обмена веществ. В дальнейшем интенсивность метаболзма снижается, а вместе с этим изменяется его направленность. Если в начале В. преобладают процессы распада, то в дальнейшем – процессы синтеза. Разграничить их во времени практически невозможно. Анаболические процессы появляются очень рано, но преобладают на более поздних стадиях В., когда проявляются восстановительные (репаративные) тенденции. В результате активирования определенных ферментов усиливается синтез ДНК и РНК, повышается активность гистиоцитов и фибробластов.
Комплекс физико-химических изменений включает в себя ацидоз (вследствие нарушения тканевого окисления и накопления в тканях недоокисленных продуктов), гиперионию (накопления в очаге В. ионов К+ , Cl- , НРО4 из гибнущих клеток), дисионию (изменения соотношения между отдельными ионами, например, увеличение К+ /Са2+ коэффициента), гиперосмию, гиперонкию (обусловлена увеличением концентрации белка, его дисперсности и гидрофильности).
Структурно-функциональные изменения при В. весьма разнообразны и могут развиваться на субклеточном (митохондрии, лизосомы, эндоплазматическая сеть и др.), клеточном и органном уровнях.
4.2.2. Экссудация
4.2.2.1. Сосудистые реакции и изменения кровообращения
Экссудация (от лат. exsudatio) – выпотевание. Этот компонент В. включает в себя триаду:
а) сосудистые реакции и изменения кровообращения в очаге В.;
б) выход жидкой части крови их сосудов – собственно экссудацию;
в) эмиграцию (от лат. еmigratio - выселение) – выход лейоцитов в очаг В. и развитие фагоцитоза.
Динамика сосудистых реакций и изменения кровообращения при развитии В. стереотипа: вначале возникает кратковременный рефлекторный спазм ортериол и прекапилляров с замедлением кровотока, затем, сменяя друг друга, развивается артериальная и венозная гиперемия, престаз и стаз – остановка кровотока.
Артериальная гиперемия является результатом образования в очаге В. большого количества вазоактивных веществ – медиаторов В., которые подавляя автоматию гладкомышечных элементов стенки артериол и прекапилляров, вызывают их расслабление. Это приводит к увеличение притока артериальной крови, ускоряет ее движение, открывает ранее не функционировавшие капилляры, повышает в них давление. Кроме того, приводящие сосуды расширяются в результате “паралича” вазоконстрикторов и доминирования парасимпатических влияний на стенку сосудов, ацидоза, гиперкалийионии, снижения эластичности окружающей сосуды соединительной ткани.
Венозная гиперемия возникает вследствие действия ряда факторов, которые можно разделить на три группы: 1) факторы крови, 2) факторы сосудистой стенки, 3) факторы окружающих тканей. К факторам, связанным с кровью, относится краевое расположение лейкоцитов, набухание эритроцитов, выход жидкой части крови в воспаленную ткань и сгущение крови, образование микротромбов вследствие активации фактора Хагемана и уменьшении содержания гепарина.
Влияние факторов сосудистой стенки на венозную гиперемию проявляется набуханием эндотелия, в результате чего просвет мелких сосудов еще больше суживается. Измененные венулы теряют эластичность и становятся более податливыми сдавливающему действию инфильтрата. И, наконец, проявление тканевого факторов состоит в том, сто отечная ткань, сдавливая вены и лимфатические сосуды, способствует развитию венозной гиперемии.
С развитием престатического состояния наблюдается маятникообразное движение крови – во время систолы она движется от артерий к венам, во время дистолы – в противоположном направлении. Наконец, движение крови может полностью прекратиться и развивается стаз, следствием которого могут быть необратимые изменения клеток крови и тканей.
Выход жидкой части крови в интерстиций очага В. – собственно экссудация происходит вследствие резкого повышения проницаемости гистогематического барьера и как следствие усиления процесса фильтрации и микровезикулярного транспорта. Выход жидкости и растворенных в ней веществ осуществляется в местах соприкосновения эндотелиальных клеток. Щели между ними могут увеличиваться при расширении сосудов, а также, как полагают, при сокращении контрактильных структур и округлении эндотелиальных клеток. Кроме того, клетки эндотелия способны “заглатывать” мельчайшие капельки жидкости (микропиноцитоз), переправлять их на противоположную сторону и выбрасывать в близлежащую среду (экструзия).
Транспорт жидкости в ткани зависит от физико-химических изменений, происходящих по обе стороны сосудистой стенки. В связи с выходом белка из сосудистого русла, его количество вне сосудов увеличивается, что способствует повышению онкотического давления в тканях. При этом в очаге В. происходит под влиянием лизосомальных гидролаз расширение белковых и других крупных молекул на более мелкие. Гиперонкия и гиперосмия в очаге альтерации создают приток жидкости в воспаленную ткань. Этому способствует и повышение внутрисосудистого гидростатического давления в связи с изменениями кровообращения в очаге В.
Результатом экссудации является заполнение интерстициальных пространств и очага В. экссудатом. Экссудат отличается от трансудата тем, что содержит большее количество белков (не менее 30 г/л), протеолитических ферментов, иммуноглобулинов. Если проницаемость стенки сосудов нарушена незначительно, то в экссудат, как правило, проникают альбумины и глобулины. При сильном нарушении проницаемости из плазмы в ткань поступает белок с большей молекулярной массой (фибриноген). При первичной, а затем и вторичной альтерации проницаемость сосудистой стенки увеличивается на столько, что через нее начинают проникать не только белки, но и клетки. При венозной гиперемии этому способствует расположение лейкоцитов вдоль внутренней оболочки мелких сосудов и более или менее прочное их прикрепление к эндотелию (феномен краевого стояния лейкоцитов).
Раннюю транзиторную реакцию роста проницаемости сосудов обуславливает действие гистамина, ПГЕ, лейкотриена Е4 , серотонина, брадикинина. Ранняя транзиторная реакция в основном затрагивает венулы с диаметром не более, чем 100 мкм. Проницаемость капилляров при этом не меняется. Действие экзогенных этиологических факторов механической (травма, ранение), термической или химической природы, вызывая первичную альтерацию, приводит к длительной реакции роста проницаемости. В результате действия этиологического фактора происходит некроз эндотелиалльных клеток на уровне артериол небольшого диаметра, капилляров и венул, что ведет к стойкому возрастанию их проницаемости. Отсроченная и стойкая реакция роста проницаемости микрососудов развивается в очаге В. через часы или сутки от его начала. Она характерна для В., вызванного ожогами, излучением и аллергическими реакциями отсроченного (замедленного) типа. Одним из ведущих медиаторов этой реакции является медленно реагирующая субстанция анафилаксии (МРСА), которая есть не что иное как лейкотриены и полиненасыщенные жидкие кислоты, которые образуются их арахидоновой кислоты и фактора активации тромбоцитов (ФАТ). МРСА в очаге В. образуют и высвобождают лаброциты. Стойкий рост проницаемости микрососудов в очаге В. МРСА обуславливает, вызывая протеолиз базальных мембран микрососудов.
Биологический смысл экссудации как компонента В. состоит в отграничении очага В. через сдавление кровеностных и лимфатических микрососудов вследствие интерстиналльного отека, а также в разведении флогогенов и факторов цитолиза в очаге В. для предотвращения избыточной вторичной альтерации.
4.2.2.2. Эмиграция лейкоцитов
Эмиграция лейкоцитов (лейкодиапедез) – выход лейкоцитов из просвета сосудов через сосудистую стенку в окружающую ткань. Этот процесс совершается и в норме, но при В. приобретает гораздо большие масштабы. Смысл эмиграции состоит в том, чтобы в очаге В. скопилось достаточное число клеток, играющих роль в развитии В. (фагоцитоз и т.д.).
Миграция лейкоцитов к месту повреждения тканей или инфекции (к месту воспаления ) включает три этапа:
1. адгезия (прилипание) на эндотелии сосудов воспаленных тканей в результате заимодействия молекул адгезии на поверхности лейкоцитов и активированных эндотелиальных клеток;
2. проникновение через эпителий;
3. перемещение в направлении очага инфекции или воспаления под влиянием химического притяжения, называемого хемотаксисом . Эти процессы регулируются присутствующими на поверхности мигрирующих клеток белками (которые взаимодействуют с эндотелием, тканевыми клетками или внеклеточным матриксом), а также растворимыми сигнальными молекулами - хемокинами и другими хемоаттрактантами.
Миграция осуществляется путём диапедеза главным образом через стенку венул. Это ключевое событие в патогенезе воспаления. В основе миграции стоит явление хемотаксиса. Пусковым моментом активации моноцитов является воздействие на рецепторы клеточных мембран разнообразных хемотаксических агентов, высвобождаемых микроорганизмами или фагоцитами, а также образующихся в тканях под действием флогогенного фактора.
Последовательность выхода лейкоцитов получила название закона Мечникова, согласно которому спустя несколько часов (1, 5-2 часа) с момента действия альтерирующего фактора интенсивно эмигрируют нейтрофилы и другие сегментоядерные лейкоциты, а затем моноциты и лимфоциты.
Процессу эмиграции предшествует нарушение осевого тока движения крови внутри сосуда. В условиях замедления кровотока эритроциты, объединяясь в «монетные столбики», занимают центральную часть сосуда, а лейкоциты, имеющие более низкую удельную массу, выходят из осевого тока сначала на границу плазматического слоя, а затем начинают прилипать к эндотелиальным клеткам сосуда. Важная роль в адгезии лейкоцитов отводится так называемым эндотелиально-лейкоцитарным адгезивным молекулам (ЭЛАМ), которые экспрессируются на поверхности лейкоцитов, эндотелиальных клеток и макромолекулах межклеточного матрикса в очаге воспаления. Активаторами экспрессии ЭЛАМ на лейкоцитах и эндотелиальных клетках в зоне воспаления являются биологически активные вещества - цитокины, такие как ИЛ-1, ИЛ-8, ЛТ В4, ФАТ, ФНО-a, a-интерферон, фракции комплемента С5а и Bb, хемотаксические факторы, липополисахариды бактерий и др. Под влиянием указанных медиаторов в лейкоцитах и клетках эндотелия сосудов происходят конформационные изменения мембраны, освобождаются и экспресссируются молекулы адгезии. Большинство цитокинов в одинаковой степени влияет на адгезивность лейкоцитов и эндотелия, однако отмечается и избирательное действие медиаторов на различные клетки. Компоненты комплемента - на моноцитах и гранулоцитах.
В настоящее время известно несколько классов молекул клеточной адгезии:
1. Селектины - лектиновые молекулы клеточной адгезии, опосредующие самую раннюю стадию взаимодействия лейкоцитов и сосудистой стенки. Селектины экспрессируются рано и не обеспечивают прочного прикрепления лейкоцитов к эндотелию сосудов. Выделяют три вида селектинов: L-селектины синтезируются всеми лейкоцитами,
Е-селектины синтезируются эндотелиоцитами. Указанные селектины обеспечивают феномен краевого стояния лейкоцитов. Источником
P-селектинов являются тромбоциты и эндотелий сосудов, помимо участия в процессах маргинации лейкоцитов, они способствуют адгезии тромбоцитов.
2. Интегрины - это гетеродимерные белки, экспрессируемые различными лейкоцитами и клетками гемопоэтического ряда. Эндотелий экспрессирует лишь некоторые интегрины. В настоящее время идентифицировано пять видов интегринов. Наиболее важными для миграционного и фагоцитарного процесса являются три гетеродимера. Указанные интегрины ответственны за поздние стадии взаимодействия лейкоцитов, тромбоцитов и эндотелия сосудов.
3. Адгезивные молекулы суперсемейства иммуноглобулинов (ICAM) - трансмембранные протеины с пятью внеклеточными доменами, экспрессируемые преимущественно эндотелием. Некоторые из этих молекул синтезируются неактивированными клетками и определяют интенсивность физиологической миграции лейкоцитов. В зоне воспаления под влиянием ИЛ-1, ФНО, гамма-интерферона активируются синтез и экспрессия молекул ICAM, что обеспечивает отсроченную фазу адгезии и эмиграции лейкоцитов. В группу белков, подобных иммуноглобулинам, включены лимфоцитарные рецепторы - СD2, СD58 (LFA-3). Они экспрессируются на Т-лимфоцитах и антигенпредставляющих клетках, участвуют в презентации антигена и контакте цитотоксических лимфоцитов с клетками-мишенями.
4. Адрессины - белки эндотелиальных клеток венул лимфоидных органов. Имеют большое значение в миграции лимфоцитов в очаги хронического и аутоиммунного воспаления. При остром воспалении адрессины менее значимы.
5. Хрящевые соединительные белки. Экспрессируются всеми видами лейкоцитов, распознают гиалуроновую кислоту, что обеспечивает перемещение лейкоцитов в основном веществе соединительной ткани.
После адгезии лейкоциты выходят за пределы сосуда на стыке между эндотелиальными клетками. Это объясняется округлением эндотелиоцитов и увеличением интервалов между ними. После выхода лейкоцитов контакты восстанавливаются. Амебиодное движение лейкоцитов возможно благодаря обратимым изменениям состояния их цитоплазмы (взаимоперехода геля в золь - тиксотропии) и поверхностного натяжения мембран, обратимой “полимеризации” сократительных белков – актина и миозина и использованию энергии АТФ анаэробного гликолиза.
В большинстве случаев острого воспаления внутрисосудистые перемещения лейкоцитов и их эмиграция занимают несколько часов. Как правило, первыми в очаг воспаления выходят нейтрофилы, они обнаруживаются в воспаленной ткани уже через 6-24 часа. Несколько позднее эмигрируют моноциты и лимфоциты (24-48 часов). Такая асинхронность эмиграции клеток обусловлена неодновременным появлением молекул адгезии и хемотаксических факторов, специфичных для разных лейкоцитов.
Нужно отметить, что временные интервалы эмиграции лейкоцитов и последовательность их выхода весьма относительны и определяются типом сосуда, видом воспаления и стадией воспаления.
Так, в зоне воспалительного процесса, инициируемого возбудителями туберкулеза, листериоза, хламидиоза, токсоплазмоза, вирусной инфекцией, первоначально в очаге воспаления доминируют мононуклеары, при аллергических реакциях - эозинофилы.
Направленное движение лейоцитов объясняется накоплением в очаге В. экзо- и эндогенных хемоаттрактантов – веществ индуцирующих хемотаксис, повышением температуры (термотаксис), а также развитием условий для гальвано- и гидромаксиса.
При взаимодействии рецепторов и хемоаттрактантов возникает гиперполяризация мембраны лейкоцита, увеличивается ее проницаемость для ионов Са, инициируется синтез функционально активных фосфолипидов и циклических нуклеотидов, растет число внутриклеточных органелл, функционирование которых обеспечивает перемещение лейкоцита и секрецию содержимого гранул. Помимо ориентированного движения лейкоцитов, хемоаттрактанты индуцируют адгезию лейкоцитов к эндотелию, способствуют краевому стоянию лейкоцитов и их агрегации в просвете микрососудов.
Хемотаксис опосредуется различными группами веществ:
1. Цитотаксигенами, которые, не являясь хемоаттрактантами, генерируют факторы хемотаксиса.
2. Цитотаксинами, которые оказывают прямое воздействие на лейкоциты. Некоторые цитотаксины специфичны для нейтрофилов (например, экстракт культуры Е.coli) , а другие цитотаксины индуцируют миграцию гранулоцитов и моноцитов [35].
Хемоаттрактанты могут иметь эндогенное и экзогенное происхождение. Экзогенными хемоаттрактантами являются пептиды бактерий, особенно содержащие N-формиловые группы. Свойствами эндогенных хемоаттрактантов обладают компоненты комплемента, иммуноглобулины, иммунные комплексы, лимфокины и монокины, кинины, лейкотриен В4, продукты липоксигеназного пути превращения арахидоновой кислоты, фактор, активирующий тромбоциты, фактор Хагемана, лизосомальные ферменты и другие.
После взаимодействия хемоаттрактантов со своими рецепторами на поверхности нейтрофилов и активированных моноцитов, хаотическое движение фагоцитов прекращается. Фагоциты начинают ориентировано перемещаться по направлению к объекту эндоцитоза в соответствии с градиентами концентрации хемоаттрактантов, то есть становятся ориентированными. Процесс эмиграции может не только стимулироваться, но и подавляться. Рост содержания в очаге В. кортизола тормозит ориентированный хемотаксис нейтрофилов. Гиперкортизолемия, тормозящая миграцию ориентированных полиморфонуклеаров, направлена на предотвращение трансформации воспаления из защитной в патологическую реакцию.
4.2.2.3. Фагоцитоз
Проникнув в очаг В., фагоциты выполняют свою главную фагоцитарную функцию. Фагоцитоз – эволюционно выработанная защитно-приспособительная реакция организма, заключающаяся в узнавании, активном захвате (поглощении) и переваривании микроорганизмов, разрушенных клеток и инородных частиц специализированными клетками – фагоцитами. К ним относятся полиморфно-ядерные лейкоциты (в основном нейтрофилы), клетки системы фагоцититрующих мононуклеаров (моноциты, тканевые макрофаги), а также клетки Купфера в печени, мезангиальные клетки почек, глиальные клетки в ЦНС и др.
В самом процессе фагоцитоза можно проследить четыре стадии:
1.приближение к фагоцитируемому объекту;
2.контакт, распознавание и прилипание к объекту;
3.поглощение объекта;
4.переваривание.
Главным механизмом приближения является хемотаксис.
Во второй стадии действует несколько механизмов. Первый из них — опсонизация — покрытие объекта фагоцитоза сывороточными факторами (антителами нормальных и иммунных сывороток). Иммуноглобулины М, G и Е метят объекты фагоцитоза. Роль метки они выполняют либо сами, либо с участием компонентов комплемента. Прилипание осуществляется посредством связи опсонинов со специфическими поверхностными рецепторами фагоцитов: для Fc-фрагмента иммуноглобулинов, для компонентов комплемента (СЗ). Причем имеет место комодуляция рецепторов: в условиях блокады Fc-рецепторов (избыточное количество иммунных комплексов или агрегированного IgG) макрофаг начинает вырабатывать фактор, индуцирующий продукцию Т-клетками лимфокина, который активирует фагоцитоз, опосредованный СЗ-рецепторами.
Второй механизм — инициация сигнала для поглощения частицы. Сигналом для поглощения объекта и последующих метаболических изменений может быть освобождение под влиянием макрофагаль-ной лейкопептидазы из состава молекулы IgG тетрапептидов тафцина и ригина. Тафцин и регин, действуя как медиаторы воспаления, резко усиливают фагоцитоз, антителогенез, антителозависимую клеточ-но-опосредованную цитотоксичность, миграцию лейкоцитов и стимулирует секрецию интерлейкина-2, выполняя регуляторную функцию в иммунной системе.
Механизм поглощения, составляющий третью стадию фагоцитоза, оптимально происходит только в условиях полного и равномерного покрытия объекта фагоцитоза опсонинами и включает:
последовательную ассоциацию опсонических детерминант частиц с панелью рецепторов фагоцита, инвагинацию наружной мембраны фагоцита по типу застегивания молнии;
образование псевдоподий, охватывающих объект и сливающихся друг с другом.
Первый механизм, присущ фагоцитозу клеток и крупных частиц, второй характерен для поглощения микроорганизмов. Результат в обоих случаях один — образование фагосомы с частицей внутри. В поглощении участвует цитоскелет фагоцитов, в частности, белки клатрин и актин. В течение 1—2 минут в клетке формируется несколько фагосом. При участии цитоскелета происходит слияние ли-зосом с фагосомами с образованием фаголизосомы.
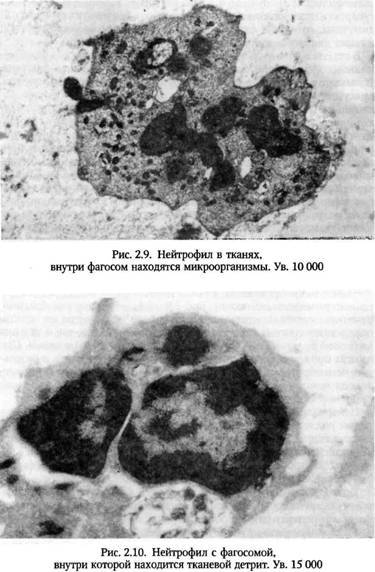
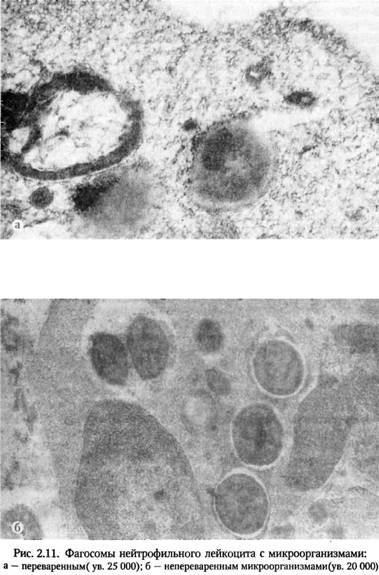
В фаголизосомах начинается переваривание поглощенного объекта. Необходимо отметить, что одни лизосомальные ферменты не могут обеспечить достаточного киллерного действия. Эффективность фагоцитоза возрастает, когда в процесс подключается так называемая кислородная система. При фагоцитозе повышается потребление кислорода, причем столь резкое, что его принято называть “респираторным взрывом”. Смысл столь резкого (до 10 раз) повышения потребления кислорода состоит в том, что он используется для борьбы с микроорганизмами. Происходит образование токсичных для микробов активных форм О2 – перекиси водорода, гидроксильных радикалов, супероксидного аниона, синглетного кислорода. Эти высокоактивные соединения вызывают перекисное окисление липидов, белков, нуклеиновых кислот, углеводов и при этом повреждают построенные из этих веществ клеточные структуры микроорганизмов. Особенно легко окисляются ненасыщенные жирные кислоты, входящие в состав клеточных мембран. Кислородный механизм пускается в ход, когда рецептор фагоцита приходит в контакт с объектом фагоцитоза. Эффективность действия такого окислителя, как Н2 О2 , еще более возрастает, когда оно сочетается с действием миелопероксидазы и одного из галоидов (иона хлора или иода). Взаимодействие Н2 О2 , миелопероксидазы и хлора приводит к окислению ионов хлора и образованию гипохлорной кислоты, которая разрушает сульфгидрильные группы микробных ферментов, пептидные элементы клеточных мембран.
Конечно, в этой ситуации фагоцит и сам подвергается агрессивному действию названных веществ, но он обладает мощным механизмом, благодаря которому избыточного накопления активных форм кислорода не происходит. Защитную роль при этом играют прежде всего два фермента: глютатионпероксидаза и глютатионредуктаза, роль которых заключается в том, что первый переносит водород на окисленный глютатион, а второй – снимает этот водород и передает его на Н2 О2 , в результате чего образуются две молекулы воды.
Определенную роль играет каталаза, выводящие из клеток избыток перекиси водорода. Супероксидный анион обезвреживается особым ферментом - супероксиддисмутазой. У фагоцитов имеются и другие не связанные с кислородом (кислороднезависимые) механизмы борьбы с микроорганизмами. К ним относятся: лизоцим, разрушающий мембраны бактерий; лактоферрин, конкурирующий за ионы железа и, наконец, дефензины (белки со структурой насыщенной аргинином), катионные белки, нарушающие структуру мембран микроорганизмов. Совместное действие механизмов обеих групп приводит к разрушению объектов фагоцитоза.
Однако наряду с завершенным фагоцитозом в микрофагах наблюдается, например, при некоторых инфекциях фагоцитоз незавершенный или эндоцитобиоз, когда фагоцитированные бактерии или вирусы не подвергаются полному перевариванию, а иногда даже начинают размножаться в цитоплазме клетки. Эндоцитобиоз объясняют недостатком или даже отсутствием в лизосомах макрофагов антибактериальных катионных белков, что снижает переваривающую способность лизосмальных ферментов. Фагоцит, поглотивший бактерии, но не способный их переварить становится переносчиком инфекции по организму, способствует ее дессиминации.
4.3. Пролиферация и завершение процесса.
Воспаление всегда начинается с повреждения и гибели клеток. Но на определенном этапе инфильтрация, нагноение и связанные с ними процессы протеолиза и некроза приостанавливаются и на передний план выступают процессы восстановления. В соответствии с этим меняются и клеточный состав воспалительного инфильтрата. Полиморфно-ядерные лейкоциты постепенно исчезают (гибнут), а доминирующими становятся мононуклеары – моноциты и лимфоциты. Роль моноцитов заключается в том, что они, как и тканевые макрофагы, поглощают переваривают погибшие клетки, а также продукты распада, возникающие при альтерации. Лимфоциты обеспечивают гуморальный иммунитет.
По мере очищения очага В. наступает пролиферация (от лат. proliferatio – размножение) – интенсификация деления фибробластов и образования ими стромы соединительной ткани (коллагеновых структур для замещения в очаге В. дефектов ткани вследствие первичной и вторичной альтерации). Продуктивную или пролиферативную стадию В. иногда называют стадией репарации, что более точно, и указывает на суть процесса в этот период, а также на биологическое значение В., связывающего между собой результат повреждающего действия чрезвычайного раздражителя с процессами репарации. Пролиферацию завершает инволюция рубца, то есть уничтожение и элиминация лишних коллагеновых структур. Основные клеточные эффекторы пролиферации – это активированные мононуклеарные фагоциты, фибробласты и иммунокомпетентные клетки. Фибробласты в очаге В. образуют и высвобождают коллаген и энзим коллагеназу, ответственный за формирование коллагеновых структур стромы соединительной ткани. Кроме то они образуют фибронектин, определяющий миграцию, пролиферацию и адгезию фибробластов. Мононуклеары и лимфоциты секретируют цитокины как стимулирующие, так и подавляющие эти функции фибробластов. Нейтрофилы, как клеточные эффекторы В., влияют на пролиферацию, секретируя тканеспецифические ингибиторы, взаимодействующие по принципу обратной связи.
Одновременно с процессом пролиферации и даже несколько опережая его, идет процесс активного погашения воспалительного процесса, что проявляется ингибицией ферментов, дезактивацией В., детоксикацией и выведением токсических продуктов. Активность клеток В. тормозится разными механизмами. Что касается ингибиторов, то в этом отношении важнейшую роль играют a2 -макроглобулин, a-антихимотрипсин, антитромбин III и a2 -антиплазмин. Они являются главными ингибиторами кининобразующих ферментов крови и таким образом устраняют их влияние: расширение и повышение проницаемости сосудов. Кроме того, она являются главными ингибиторами системы коагуляции, фибринолиза и комплемента, ингибируют элластазу и коллагеназу лейкоцитов и тем самым предохраняют от разрушения элементы соединительной ткани. В прекращении разрушительных влияний при В. важную роль играет и устранение свободных радикалов. Внутри клеток свободные радикалы нейтрализуют супероксиддисмктаза, а в экстрацеллюлярной фазе – церулоплазмин, катализирую реакцию НО2 +НО2 —Н2 О+О2 .
Изменения взаимоотношение между клетками. Они перестают вырабатывать одни медиаторы и начинают синтезировать другие. Теперь на тот же медиатор клетка может дать совсем другой ответ, потому что на ее поверхности появляются совсем другие рецепторы, а прежние проникают внутрь (интернализация). Гистамин – типичный медиатор В., но его эффект в конце В. может стать совсем иным, чем вначале. Оказалось, что это зависит от того, какие рецепторы “выставлены” на эффекторных клетках (например, на эндотелиоцитах) в данный момент. Если это Н1 , то действие будет провоспалительное, а если Н2 , то – противовоспалительное.
В инактивации клеток В., кроме местных факторов, большую роль играют также и общие факторы, в том числе эндокринные. Гормон коры надпочечников кортизол тормозит синтез вазоактивных веществ в клетках, вызывает лимфопению, уменьшает число базофилов и эозинофилов. Кроме того, он стабилизирует мембраны лизосом, угнетает выработку интерлейкина-1. Что же касается фагоцитарной активности, то она к концу В. возрастает. Благодаря этому зона В. освобождается от некротизированный клеток, чуждых и токсических веществ.
Таким образом, в конце В., в деле его завершения решающую роль играют две клетки: фибробласт и эндотелиоцит. Два процесса совершаются в этот период: заселение зоны фибробластами и неоангиогенез, т.е. образование новых кровеносных и лимфатических сосудов.
5. Монокины
Монокины – клеточные медиаторы воспаления, которые образуются моноцита-ми/макрофагами на фоне антигенной стимуляции, а некоторые монокины мо-гут продуцироваться другими клетками (лимфоцитами, гепатоцитами, гли-альными клетками и др.) (Фрейдлин И.С.,1984; Паркер Ч.В.,1989). В настоя-щее время известно более 100 биологически активных веществ, секретируе-мых моноцитами/макрофагами, классификация которых приведена ниже.
1. Протеазы: активатор плазминогена, коллагеназа, эластаза, ангиотензин конвертаза.
2. Медиаторы воспаления и иммуномодуляции: ФНО, ИЛ-1, ИЛ-3, ИЛ-6, ИЛ-8, ИЛ10,ИЛ-12, ИЛ-15, интерферон, лизоцим, фактор активации нейтро-филов, компоненты комплемента С, С2, С3, С5.
3. Факторы роста: КСФ-ГМ, КСФ-Г, КСФ-М, фактор роста фибробластов, трансформирующий фактор роста.
4. Факторы свертывающей системы и ингибиторы фибринолиза: Y,YII, IX, X, ингибиторы плазминогена, ингибиторы плазмина.
5. Адгезивные вещества: фибронектин, тромбоспондин, протеогликаны. Далее приводится характеристика некоторых монокинов, играющих важную роль в индукции воспалительной реакции.
ИЛ-1 представляет собой полипептидный цитокин с молекулярной массой 15 килодальтон, высвобождается активированными моноцитами, В-лимфоцитами, тканевыми макрофагами, микроглиальными, мезангиальными и др. клетками. ИЛ-1 впервые был описан в 1972 году I. Gery и B. Waksman. ИЛ-1 существует в двух биологических формах: растворимой и связанной с мембраной моноцитов/макрофагов Синтез ИЛ-1 ко-дируется двумя генами, следствием чего является образование двух медиато-ров - ИЛ-1 и ИЛ-1, обладающих сродством к одному и тому же рецептору . ИЛ-1 обладает комплексом биологических эффектов – является эндопиро-геном и, соответственно, обусловливает развитие лихорадки при воспалении, стимулирует выход ПЯЛ из костного мозга, увеличивает образование и осво-бождение ими коллагеназы, вызывает экспрессию эндотелиально-лейкоцитарных адгезивных молекул (ЭЛАМ) на поверхности эндотелиоци-тов и лейкоцитов, способствует краевому стоянию лейкоцитов и стимулирует процесс их эмиграции.
ИЛ-1 вызывает экзоцитоз лизосомальных ферментов и свободных кислородных радикалов фагоцитами, которые подвергают деструкции нежизнеспособные клеточные элементы и бактериальные клетки.
ИЛ-1 является фактором клеточного роста, он усиливает пролиферацию фибробластов и повышает образование коллагена.
ИЛ-1 в качестве флогогена вызывает дегрануляцию тучных клеток с высвобождением медиаторов воспаления, активирует эндотелиоциты, стимулирует продукцию простациклина. ИЛ-1 действует на гипоталамо-гипофизарную систему, стимулирует секрецию АКТГ, СТГ, играет важную роль в развитии системной иммунной реакции.
К числу монокинов помимо ИЛ-1 относятся колониестимулирующий фактор, интерферон, фактор хемотаксиса лимфоцитов, бактерицидный фактор, цитолитический фактор и др.
Колониестимулирующие факторы (КСФ) – гликопротеины, влияющие на образование, дифференциацию и функции гранулоцитов и клеток системы мононуклеарных фагоцитов (Шанин В.Ю., 1996).
Различают несколько разновидностей КСФ: гранулоцитарный КСФ, гранулоцитарно-макрофагальный КСФ и мульти-КСФ (ИЛ-3).
КСФ образуются и в условиях нормы и возбужденными в зоне воспаления клеточными элементами.
Гранулоцитарный КСФ, кодируемый геном 17-й хромосомы, обра-зуется эндотелиальными клетками, фибробластами, макрофагами. Совместно с ИЛ-3 гранулоцитарный КСФ увеличивает содержание в циркулирующей крови мегакариоцитов и юных форм гранулоцитов.
Гранулоцитарно-макрофагальный КСФ кодируется геном 5-й хромосомы, секретируется эндотелиоцитами, фибробластами и фагоцитами, увеличивает содержание моноцитов в циркулирующей крови.
Мульти-КСФ, или ИЛ-3 образуется Т-лимфоцитами, кодируется геном 5-й хромосомы, стимулирует образование гранулоцитов, макрофагов, эозинофи-лов, усиливает пролиферацию тучных клеток.
Следует отметить, что в одном из последних детальных обзоров, касающихся состояния иммунной системы в норме и патологии, представлен более широкий перечень цитокинов – факторов роста, продуцируемых эндотелием, фибробластами, адипоцитами костного мозга, макрофагами. Среди них М-СSF (моноцитколоние стимулирующий фактор), G-CSF (гранулоцитколониестимулирующий фактор). Последний цитокин действует дистантно из очага воспаления, обусловливая развитие нейтрофильного лейкоцитоза при воспалительном процессе.
ИЛ-7 продуцируется клетками стромы костного мозга, поддерживает дифференцировку и пролиферацию развивающихся В-лимфоцитов.
ИЛ-9 поддерживает пролиферацию клеток-предшественников тучных клеток в костном мозге.
ИЛ-11 продуцируется клетками стромы костного мозга, стимулирует про-цессы пролиферации и дифференцировки клеток мегакариоцитарного ряда.
При развитии тяжелых септических процессов в системный кровоток проникают в основном следующие цитокины: TNF, ИЛ-1, ИЛ-6 и G-CSF. Другие цитокины не выходят в системную циркуляцию и действуют локаль-но. ФНО - образуется тканевыми макрофагами, моноцитами и лимфоцитами в зоне острого воспаления, способствует развитию лихорадочной реакции, усиливает основные функции лейкоцитов, стимулирует выброс гистамина базофилами и тучными клетками, вызывает активацию фибробластов, глад-ких миоцитов и эндотелия сосудов в очаге воспаления, индуцирует синтез белков острой фазы. Действуя синергично с ИЛ-1 и ИЛ-6, повышает функ-циональную активность цитотоксических Т-лим-фоцитов и их способность к разрушению инфицированных вирусом клеток, что ведет к элиминации ви-руса. ФНО способствует цитолизу злокачественных клеток.
Ген, локализованный в макрофагах, кодирует продукцию так называемого наряду с прочими эффектамиa с молекулярной массой 17 кД. ФНО-aФНО- тормозит синтез и депонирование жира, в связи с чем получил название , илиbка-хексина. Ген лимфоцитов кодирует образование ФНО- лимфотоксина, имеющего ММ 25 кД. ФНО способствует развитию лихорадочной реакции, усиливает основные функции лейкоцитов, стимулирует выброс гистамина базофилами и тучными клетками, вызывает активацию фибробластов, глад-ких миоцитов и эндотелия сосудов в очаге воспаления, индуцирует синтез белков острой фазы. Действуя синергично с ИЛ-1 и ИЛ-6, повышает функ-циональную активность цитотоксических Т-лимфоцитов и их способность к разрушению инфицированных вирусом клеток, что ведет к элиминации ви-руса. ФНО способствует цитолизу злокачественных клеток.
В отличие от ИЛ-1, ФНО обладают ярко выраженной способностью вы-зывать геморрагический некроз опухоли (Маянский Д.Н., 1994). Туморнек-ротизирующий эффект обусловлен, по-видимому, усилением экспрессии эн-дотелиальных адгезивных белков под влиянием ФНО, адгезией лейкоцитов, тромбоцитов к сосудистой стенке, развитием явлений тромбоза, эмболии, на-рушением трофики, васкуляризации и оксигенации опухоли. Лимфокины - это биологически активные вещества, которые продуцируются сенсибилизи-рованными лимфоцитами при специфической антигенной стимуляции. Сле-дует отметить, что часть цитокинов (ИЛ-2, ИЛ-3, ИЛ-6, ИЛ-8, ИЛ-10 и др.) может продуцироваться лимфоцитами, а также клетками моноцитарно-макрофагальной системы. В связи с этим они могут быть отнесены как к группе лимфокинов, так и к группе монокинов.
6. Заключение
В заключении хотелось бы отметить особую роль моноцитов/макрофагов в очаге воспаления.
Моноциты, эмигрировавшие в ткани, превращаются в тканевые макрофаги. В зоне воспаления происходит накопление макрофагов за счет эмиграции моноцитов из кровеносного русла, а также за счет мобилизации тканевых макрофагов. Макрофаги обеспечивают фагоцитоз не только инфекционных возбудителей воспалительного процесса, но и клеточный детрит, тем самым очищая зону альтерации и подготавливая ее к последующей регенерации и репарации. Мононуклеарные фагоциты участвуют в обеспечении неспецифической защиты организма посредством фагоцитоза, секреции гуморальных факторов, таких как лизоцим, a-интерферон, ФНО, компоненты комплемента. В очаге воспаления макрофаги приобретают более выраженные антимикробные свойства благодаря фагоцитозу антимикробных компонентов, продуцируемых нейтрофилами (миелопероксидазы и катионных белков). Таким образом, макрофаги приобретают способность галоидировать белки. Микробицидная функция макрофагов реализуется через продукты «респираторного взрыва», секреции монокинов, лизосомальных ферментов. Окислительные реакции сопровождаются накоплением в очаге воспаления высокотоксичных продуктов ПОЛ, вызывающим дальнейшую деструкцию клеток, сосудов и элементов соединительной ткани.
При наличии этиологического агента в виде бактериального возбудителя моноциты/макрофаги являются антигенпрезентирующими клетками, обеспечивающими запуск иммунного ответа организма. В процессе представления антигена активированные макрофаги секретируют и освобождают такие цитокины, как ФНО, интерлейкины (ИЛ-1, ИЛ-3, ИЛ-6, ИЛ-8, ИЛ-10, ИЛ-12, ИЛ-15), компоненты комплемента, хемотаксические факторы [44]. Выделение зрелых форм интерлейкинов из клеток начинается уже через 2 часа после антигенной стимуляции и продолжается в течение 24-48 часов. Моноциты/макрофаги в зоне воспаления являются источником лизосомальных протеаз - коллагеназы, эластазы, ангиотензин конвертазы, активатора плазминогена; адгезивных веществ - фибронектина, тромбоспондина, протеогликанов; факторов роста - колониестимулирующих факторов, фактора роста фибробластов; эндогенных пирогенов.
Под действием пусковых медиаторов макрофагов в очаге воспаления происходит активация различных типов лейкоцитов, клеток соединительной ткани, эндотелия сосудов, паренхиматозных клеток, что приводит к синтезу и секреции биологически активных соединений, оказывающих повреждающие, защитные и системные эффекты.
Интенсивная эмиграция лимфоцитов в зону воспаления в большинстве случаев осуществляется после эмиграции нейтрофилов и моноцитов. Стимулированные лимфоциты выделяют биологически активные вещества - лимфокины, обеспечивающие развитие иммунного ответа, аллергических реакций, процессов пролиферации и репарации.
Все лейкоциты в зоне воспаления довольно быстро подвергаются жировой дегенерации, превращаются в гнойные тельца и удаляются вместе с гноем. В очаге воспаления возможны два пути гибели лейкоцитов.
Первый - грубое повреждение мембраны, нарушение целостности клетки и ее некроз, что возможно в очаге первичной и вторичной альтерации под влиянием самого повреждающего агента и различных цитотоксических медиаторов воспаления.
Второй - более мягкий, запрограммированный путь клеточной гибели, или апоптоз. При апоптозе наблюдаются уменьшение ядра лейкоцита, конденсация ядерного хроматина, фрагментация ДНК, подавление транскрипции, снижение синтеза рибосомной РНК и белков. Стареющие нейтрофилы теряют способность секретировать лизосомальные ферменты, и это исключает дальнейшее повреждение ткани. Макрофаги активно фагоцитируют апоптозные нейтрофилы. Поглощение апоптозных нейтрофилов обеспечивается взаимодействием тромбоспондина, секретируемого макрофагом и рецепторами нейтрофила. Путем апоптоза могут удаляться из очага воспаления не только нейтрофилы, но и эозинофилы и лимфоциты.
Как видно, моноциты являются дирижерами клеточного ансамбля воспаления, играют важнейшую роль в удалении микроорганизмов и очищении очага, но в конце их неизбежно ждёт смерть за правое дело.
7. Список литературы
1.Журнал «Цитокины и воспаление». 2007. Т. 6, № 3. С. 44-48
2.http://www.rae.ru/monographs/28-724
3. Абелев Г.И. «Воспаление»
4.Зайко Н.Н., Быць Ю.В. Патологическая физиология. – Киев “Логос”, 1996. – 647 с.
5.Адо А.Д., Новицкий В.В. Патологическая физиология. Изд-во Томского Университета. – Томск, 1994. – 464
6.Зайко Н.Н. Патологическая физиология. – Элиста АОЗГ “Эссен”, 1994.
7.Литвицкий П.Ф. Патофизиология. Курс лекций. – М.: медицина, 1995. – 745 с.
8. Серов В.В., пауков В.С. Воспаление. М., медицина, 1995. – 640 с.
9. Шанин В.Ю. Типовые патологические процессы. – С.-П., 1996. – 278 с.

Государственное образовательное учреждение высшегопрофессионального образования Санкт-Петербургский Государственный Медицинский Университет
имени академика И.П.Павлова
Кафедра патологической физиологии
РЕФЕРАТ
на тему:
«Роль лейкоцитов в патофизиологии воспаления»
Выполнила: студентка 318 группы
лечебного факультета
Умёнушкина Е.А..
Научный руководитель:
Евстигнеев А.С.
Санкт-Петербург
2010