| Скачать .docx |
Курсовая работа: Извлечение таллия из растворов переработки пылей свинцового производства
Задание
Тема: “Извлечение таллия из растворов переработки пылей свинцового производства”
1 Выполнить металлургический расчет с составлением материального баланса по всем операциям с получением таллия
2 Выполнить расчет процесса экстракции (число ступеней экстракции, геометрические размеры экстрактора)
3 Графическая часть: экстрактор
Исходные данные:
Состав раствора, г/дм3: Zn – 65,Cd – 8,2,Tl – 0,35, In – 0,05,Fe – 0,01,H2SO4 – 18
Извлечение таллия:
- при экстракции 95-98%,
- при реэкстракции 99-99,5%.
Соизвлечение кадмия при экстракции 0,5%, плотность индиевого рафината 1,05 кг/дм3.
Производительность по раствору 150 м3/сут.
Содержание
Введение......................................................................................................... 3
1. Металлургические расчеты...................................................................... 6
1.1. Расчет технологического процесса..................................................... 6
1.2. Расчет процесса экстракции............................................................... 10
1.2.1. Расчет числа ступеней экстракции................................................. 10
1.2.2. Расчет экстрактора (смеситель-отстойник ящичного типа)....... 11
1.2.3. Расчет необходимого количества экстракторов.......................... 13
2. Мероприятия по технике безопасности................................................ 14
Список литературы...................................................................................... 15
Содержание таллия в земной коре 3.10-4% (по массе). Известны некоторые минералы таллия, но большая часть его находится в рассеянном состоянии в виде изоморфной примеси в сульфидных минералах свинца, цинка, меди, железа и в таких силикатах, как полевой шпат, слюда, лепидолит, где таллий замещает калий и рубидий. Наибольшие концентрации таллия обнаружены в сульфидах железа (пиритах и марказитах), где его содержание достигает 0,1-0,5%.
Основным сырьевым источником таллия в настоящее время служат отходы и полупродукты получаемые при переработке сульфидных руд. При окислительном и агломерационном обжиге сульфидных концентратов часть таллия уносится с газами и концентрируется в пыли электрофильтров и других пылеулавливающих устройствах. Это объясняется летучестью TlO2 и Tl2S.
При агломерационном обжиге свинцового концентрата более 50% таллия уносится с газами. Пыль электрофильтров обычно содержит десятые доли процента таллия. В процессе шахтной плавки в шлаки переходит до 20% таллия, остальное количество примерно поровну распределяется между свинцом и пылью. При рафинировании свинца большая часть таллия (70-80%) переходит в медистые съемы, 10-15% переходит в щелочной плав, получающийся при очистке свинца от мышьяка и сурьмы.
При обжиге цинковых концентратов большая часть таллия возгоняется и вместе с кадмием попадает в циклонную и котельную пыль. Пыли выщелачивают вместе с огарками, при этом ~ 85% таллия переходит в сернокислые растворы, при очистке которых таллий цементируется вместе с медью и кадмием и извлекается из кеков попутно с кадмием.
При окислительном обжиге медных концентратов весь таллий остается в огарке. В процессе отражательной плавки таллий распределяется между штейном и шлаком.
В процессе конвертирования медных штейнов 50-75% таллия переходит в шлаки, а в процессе фьюмингования шлаков 90-99% таллия концентрируется в возгонах.
Исходные материалы обычно содержат от сотых до десятых долей процента таллия. Из них таллий выщелачивают разбавленной серной кислотой. Для более полного извлечения проводят предварительную сульфатизацию гранулированного материала в кипящем слое при 300-400 0С.
Для получения таллиевых концентратов таллий выделяют из растворов в виде гидрооксида таллия (III), сульфида, хромата, хлорида таллия (I), извлекают ионным обменном или сорбцией, жидкостной экстракцией, цементацией. Выбор способа зависит от концентрации таллия в растворе и содержание сопутствующих элементов.
В курсовой работе таллий извлекают методом экстракции.
Экстракционные способы позволяют существенно упростить технологию извлечения таллия.
На отечественных предприятиях используют способ экстракции таллия из сернокислых растворов раствором иода в трибутилфосфате (ТБФ 50% -ный раствор в керосине). При контакте органической фазы с таллийсодержащим раствором некоторая часть йода переходит в раствор в виде ионов иода вследствии присутствия в растворе восстановителей: As (III), Fe (II) (если необходимо в раствор вводят восстановитель Na2SO3). Образующийся в растворе TlJ переходит в органическую фазу, образуя комплекс TlJ3.3ТБФ:
Tl+водн + J-водн + (J2.3ТБФ) орг ↔ TlJ3.3ТБФ
При небольшой концентрации ионов иода в растворе кадмий, медь, мышьяк, сурьма и цинк экстрагируются в малой степени. Индий необходимо предварительно извлечь из раствора, например, экстракцией Д2ЭГФК (ди-2-этилгексин фосфорной кислотой).
Таллий реэкстрагируют из органической фазы раствором 350 г/л H2SО4 с добавлением пероксида водорода для окисления ионов иода до элементарного иода, что приводит к разрушению комплекса и регенерации экстрагента:
2 (TlJ3.3ТБФ) + H2SО4 + Н2О2 + 3ТБФ = Tl3SO4 + 3(J2.3ТБФ) + 2 Н2О
При соответствующих отношениях объемов органической и водной фаз на стадиях экстракции и реэкстракции из исходных растворов, содержащих 0,2-0,6 г/л таллия, получают реэкстракты с концентрацией таллия 20-35 г/л, из которых выделяют черновой таллий цементацией на цинке [1].
Технологическая схема извлечения таллия из сернокислых растворов приведена на рисунке 1.
1. Металлургические расчеты
1.1. Расчет технологического процесса
Пересчитаем содержание компонентов раствора на заданную производительность 150 м3/сутки (150000 дм3/сутки).
Zn 65.150000 / 1000 = 9750 кг
Cd 8,2.150000 / 1000 = 1230 кг
Tl 0,35.150000 / 1000 = 52,5 кг
In 0,05.150000 / 1000 = 7,5 кг
Fe 0,01.150000 / 1000 = 1,5 кг
Н2SО4 18.150000 / 1000 = 2700 кг
1) Экстракция индия
Рассчитаем необходимые массы Д2ЭГФК и керосина при экстракции индия
Объем раствора на экстракцию 150000 дм3, содержание индия 0,05 г/дм3. при экстракции О: В = 1: 30. Плотность электролита 0,8 кг/дм3.
Объем экстрагента:
150000 / 30 = 5000 дм3
Масса экстрагента
5000.0,8 = 4000 кг
Экстрагент используется в виде 20% раствора в керосине, тогда масса Д2ЭГФК составит
4000.0,2 = 800 кг
Масса керосина
4000 – 800 = 3200 кг
В растворе, поступающего на экстракцию содержится 7,5 кг In. Извлечение индия в экстракт 99%. Тогда содержание индия в экстракте составит
7,5.0,99 = 7,43 кг
Рассчитаем массу исходного раствора
ρраствора = 65 + 8,2 + 0,35 + 0,05 + 0,01 + 18 + 1000 = 1092 г/дм3 = 1,1 кг/дм3
mраствора = V. ρраствора = 150000.1,1 = 165000 кг
По результатам расчетов составляем таблицу 1 материального баланса экстракции индия.
Таблица 1 - Материального баланса экстракции индия
| Загружено | Получено | ||||
| Наименование | Всего, кг | В нем In, кг | Наименование | Всего, кг | В нем In, кг |
Раствор Д2ЭГФК Керосин |
165000 800 3200 |
7,50 - - |
Экстракт Рафинат |
4007,43 164992,57 |
7,43 0,07 |
| Итого | 169000 | 7,50 | Итого | 169000 | 7,50 |
2) Экстракция таллия
Плотность индиевого рафината ~1,05 кг/дм3
VРАФ = m/ρ = 164992,57 / 1,05 = 157136 дм3
Содержание таллия в исходном растворе
52,5.103 / 157136 = 0,3 г/дм3
В реэкстракте содержание таллия 20-35 г/дм3 (примем 30 г/дм3) следовательно, обогащение
30 / 0,3 = 100 раз
На реэкстракции О: B = 10: 1, следовательно при экстракции О: B = 1: 10
Рассчитаем объем экстрагента
157136 / 10 = 15714 дм3
Экстрагент используется в виде 50% раствора ТБФ в керосине + 80 г/дм3 J2. При плотности экстрагента 0,8 кг/дм3 его масса составит
mэкстрагента = 15714.0,8 = 12571,2 кг
рассчитаем добавку J2 на экстракцию
15714.80 = 1257120 г = 12,57,12 кг
30% J2 надо восстановить сульфитом натрия по реакции
1257,12.0,30 = 377,13 mNa2SO3
J2 + Na2SO3 + Н2О = Na2SO4 + 2НJ
2.126,90 126
mNa2SO3 = (377,13.126) / (2.126,90) = 187,23 кг
Na2SО3 подается в виде раствора с содержанием 250 г/дм3. Примем плотность раствора 1 кг/дм3.
250 г - 1 дм3
187,23.103 - х
х = 187,23.103 / 250 = 748,92 дм3
масса раствора
mраствора = V. ρ = 748,92.1. = 748,92 кг
содержание Tl в исходном растворе 0,3 г/дм3 или 52,5 кг
извлечение таллия при экстракции 95-98%, следовательно, в экстракте содержание таллия
52,5.0,95 = 49,88 кг
Соэкстракцией кадмия пренебрегаем
Масса экстракта составит
mэкстракта=m(50%ТБФ в керосине) +mTl+mJ=12571,2+ 49,88 + 1257,12 = 13878,2 кг
по результатам расчета составляем таблицу 2 материального баланса экстракции таллия
Таблица 2 – Материальный баланс экстракции таллия
| Загружено | Получено | ||||
| Наименование | Всего, кг | В нем Tl, кг | Наименование | Всего, кг | В нем Tl, кг |
Раствор 50% р-р ТБФ в керосине J2 Р-р Na2SO3 |
164992,57 12,571,2 1257,12 748,92 |
52,5 - - - |
Экстракт Рафинат |
13878,2 165691,61 |
49,88 2,62 |
| Итого | 179569,81 | 52,5 | Итого | 179569,81 | 52,5 |
3) реэкстракция таллия
Условия О: В = 10: 1
Объем экстракта (ρ = 0,8 кг/дм3)
13878,2 / 0,8 = 17347,75 дм3
Объем реэкстрагента составит
17347,75 / 10 = 1734,78 дм3
Реэктсрагент используется в виде 350 г/дм3 Н2SО4 + 3% Н2О (от массы экстракта)
Масса Н2SО4
350.1734,78 = 607173 г = 607 кг
В пересчета на 96% Н2SО4
607 / 0,96 = 632 кг
Плотность реэкстрагента 1,21 кг/дм3, тогда
mреэкстрагента = 17,34,78.1,21 = 2099,1 кг
масса воды в реэкстрагенте
2099,1 – 632 = 1467,1 кг
Масса Н2О2
13878,2.0,03 = 416,35 кг
В пересчете на 30% Н2О2
416,35 / 0,3 = 1387,83 кг
Содержание таллия в экстракте 79,88 кг. Извлечение при реэкстракции 99%, тогда содержание таллия в реэкстракте
mTl = 49,88.0,99 = 49,38 кг (60,98 кг Tl2SО4)
масса реэкстракта составит
mреэкстракта = mреэкстрагента + mTl = 2099,1 + 1387,83 + 49,38 = 3536,31 кг
Составляем таблицу 3 материального баланса реэкстракции.
Таблица 3 – Материальный баланс реэкстракции Tl
| Загружено | Получено | ||||
| Наименование | Всего, кг | В нем Tl, кг | Наименование | Всего, кг | В нем Tl, кг |
Экстракт Реэкстрагент: Н2SО4 (96%) Н2О Н2О2 |
13878,2 632 1467,1 1387,83 |
49,88 - - - |
Реэкстракт Экстрагент |
3536,31 13828,82 |
49,38 0,5 |
| Итого | 17365,13 | 49,88 | Итого | 17365,13 | 49,88 |
Цементация таллия на Zn пластине
60,98 mZn mTl mZnSO4
Tl2SO4 + Zn = 2 Tl + ZnSO4
504,74 65,38 2. 204,37 161,38
mZn = 60,98.65,38 / 504,74 = 7,90 кг
mTl = 60,98.2. 204,37 / 504,74 = 49,38 кг
mZnSO4 = 60,98.161,38 / 504,74 = 19,5 кг
1.2. Расчет процесса экстракции
1.2.1. Расчет числа ступеней экстракции
Рассчитаем число ступеней экстракции при экстракции таллия 50% раствором ТБФ в керосине + 80 г/дм3 J2, содержание таллия в исходном растворе 0,3 г/дм3, извлечение в органическую фазу 95%, О: В = 1: 10. По литературным данным КР = 50.
Vводн = 157136 дм3
Vорг = 157136 / 10 = 15714 дм3
Начальная концентрация таллия
m0 = 0,3 / 204,37 = 1,47.10-3 моль/дм3,
где 204,37 – мольная масса таллия.
Конечная концентрация таллия при извлечении 95% равна
0,3.0,05 = 0,015 г/дм3 или
m1 = 0,015 / 204,37 = 0,73.10-4 моль/дм3
число ступеней экстракции определим по формуле
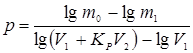 ,
,
где р - теоретическое число ступеней экстракции,
m0 – начальная концентрация экстрагируемого вещества в водной фазе, моль/дм3,
m1 – конечная концентрация экстрагируемого вещества в водной фазе, моль/дм3,
V1 – объем водной фазы, дм3
V2 – объем органической фазы, дм3
КР – коэффициент распредления
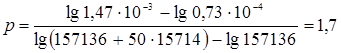
Практическое число ступеней экстракции
рпрак = р / 0,9 = 1,7 / 0,9 = 1,9
Принимаем 2 ступени экстракции
1.2.2. Расчет экстрактора (смеситель-отстойник ящичного типа)
Для расчета геометрических размеров экстрактора надо вычислить общий объем потока водной и органической фаз по формуле
![]() ,
,
где VВ – объем водной фазы, м3/сут
VО - объем органической фазы, м3/сут
Тогда
![]() м3/ч
м3/ч
Объем камер определяем по формулам
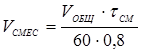
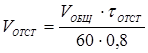 ,
,
где VСМЕС и VОТСТ – объемы смесительной и отстойной камер, м3
VОБЩ - общий поток водной и органической фаз, м3/ч
τСМ и τОТСТ – время смешивания и время отстаивания, мин
0,8 – коэффициент заполнения экстрактора
τСМ = 6 мин, τОТСТ = 10 мин
тогда
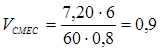 м3
м3
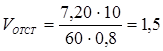 м3
м3
Соотношение размеров смесительной камеры обычно принимают
ВС: lС: НС = 1: 1: 1,5,
где ВС – ширина смесительной камеры,
lС - длина смесительной камеры,
НС - высота смесительной камеры.
Тогда
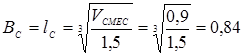 м
м
НС = 1,5 ВС = 1,5.0,84 = 1,26 м
Соотношение размеров отстойной камеры: высоту и ширину отстойной камеры можно принять равными высоте и ширине смесительной камеры, тогда
VОТСТ = ВС. НС. z
Следовательно, длина отстойной камеры
z = VОТСТ / (ВС. НС) = 1,5 / (0,84.1,26) = 1,42 м,
общая длина аппарата
lОБЩ = lC + z = 0,84 + 1,42 = 2,26 м
1.2.3. Расчет необходимого количества экстракторов
Объем одного экстрактора вычисляется по формуле
V1 = (Вс + НС + lОБЩ). рПРАКТ
V1 = (0,84 + 1,26 + 2,26).2 = 4,78 м3
Необходимое количество экстракторов будет найдено из соотношения
n = VОБЩ / V1
n = 7,2 / 4,78 = 1,5
Принимаем 2 экстрактора.
Схема экстрактора приведена на рисунке 2.
2. Мероприятия по технике безопасности
При получении таллия используются следующие вредные вещества:
1) Сернокислые растворы
Общий характер действия на организм. Раздражает и прижигает слизистые оболочки верхних дыхательных путей. При попадании на кожу вызывает ожоги.
Первая помощь. Ингаляция содового раствора. При попадании на кожу обильное промывание водой.
Предельно допустимая концентрация (ПДК) – 0,002 мг/л.
Индивидуальные защитные приспособления. Промышленный фильтрующих противогаз марки В с дополнительным противодымным фильтром. Защитные очки и маска, резиновая одежда и обувь при сливе растворов, резиновые перчатки, сапоги, передники.
2) Перекись водорода Н2О2
При постоянной работе с Н2О2 нередко наблюдаются воспалительные заболевания кожи. Индивидуальные защитные приспособления: перчатки, спецодежда.
3) керосин
Керосин сильно раздражает слизистые оболочки и кожу. При работе с керосином наблюдаются головные боли, головокружения, расстройство пищеварения, слабость. При непосредственном соприкосновении с жидким керосином действие может выражаться в дерматитах.
ПДК (в пересчета на углерод) – 300 мг/м3.
При высоких концентрациях фильтрующие противогазы малопригодны. Должны использоваться шланговые, изолирующие с принудительной подачей чистого воздуха. Защита кожи рук пастами типа “биологических перчаток”.
Меры предупреждения заключаются в максимальном устранении выделения паров, аэрозоля и контакта кожи с керосином [3].
1. Зеликман А.Н., Коршунов Б.Г. Металлургия редких металлов. – М.: Металлургия, 1991
2. Вредные вещества в промышленности. Неорганические и элементорганические соединения (под ред. Н.В. Лазарева). – Л.:Ленгосхимиздат, 1954
3. Вредные вещества в промышленности. Органические вещества (под ред. Н.В. Лазарева и Э.Н. Левиной). – Л.: Химия, 1976